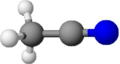
Acetonitril
| Acetonitril | |||
|---|---|---|---|
| Numele IUPAC | |||
| etanonitril | |||
| Denumiri alternative | |||
| cianură de metil cianometan metan carbonitril | |||
| Caracteristici generale | |||
| Formula moleculară sau brută | C 2 H 3 N | ||
| Masa moleculară ( u ) | 41,05 | ||
| Aspect | lichid incolor | ||
| numar CAS | |||
| Numărul EINECS | 200-835-2 | ||
| PubChem | 6342 | ||
| ZÂMBETE | CC#N | ||
| Proprietăți fizico-chimice | |||
| Densitate (g / cm 3 , în cs ) | 0,78 [1] | ||
| Solubilitate în apă | complet la 20 ° C | ||
| Temperatură de topire | −45 ° C (228 K) [1] | ||
| Temperatura de fierbere | 82 ° C (355 K) [1] | ||
| Δ eb H 0 (kJ mol −1 ) | 34.2 | ||
| Presiunea de vapori ( Pa ) la 293 K. | 9700 | ||
| Proprietăți termochimice | |||
| Δ f H 0 (kJ mol −1 ) | 40.6 | ||
| Δ f G 0 (kJ mol −1 ) | 86,5 | ||
| S 0 m (J K −1 mol −1 ) | 149.6 | ||
| C 0 p, m (J K −1 mol −1 ) | 91,5 | ||
| Proprietăți toxicologice | |||
| LD 50 (mg / kg) | 269 mg / kg oral, șoarece [2] | ||
| Informații de siguranță | |||
| Punct de flacără | 2 ° C (275 K) [1] | ||
| Limite de explozie | 3 - 17% vol. [1] | ||
| Temperatură de autoaprindere | 525 ° C (798 K) [1] | ||
| Simboluri de pericol chimic | |||
   | |||
| Pericol | |||
| Fraze H | 225 - 332 - 302 - 312 - 319 - 331 - 301 [1] | ||
| Sfaturi P | 210 - 240 - 302 + 352 - 305 + 351 + 338 - 403 + 233 [1] | ||
Acetonitrilul este compus chimic cu formula CH3 CN. În condiții normale, este un lichid volatil incolor, cu un miros slab dulce, miscibil în apă în toate proporțiile. Este cel mai simplu dintre nitrilii și se obține în principal ca produs secundar al sintezei acrilonitrilului . [3] [4] Scheletul N - C - C este liniar, iar distanța C - N este mică, 1,16 Å . [5] Molecula are un moment dipolar considerabil (μ = 3,92 D ) [6] și ca lichid are o constantă dielectrică considerabilă (ε r = 38,8), ceea ce o face un bun solvent și pentru complexele metalice și substanțele anorganice din general. Este miscibil cu toți solvenții organici obișnuiți, cu excepția hidrocarburilor saturate . Este utilizat în principal ca solvent aprotic polar în sinteze organice , în purificarea butadienei și în producerea malononitrilului . [3] [4]
Sinteză
Acetonitrilul a fost preparat pentru prima dată de chimistul francez Jean Baptiste Dumas în 1847. [7] Este obținut industrial ca subprodus al oxidării amoniului propilenei pentru sinteza acrilonitrilului; uneori acetonitrilul obținut nu este colectat și purificat, ci este utilizat direct ca combustibil pentru plantă. [4] La scară de laborator, poate fi obținut prin deshidratarea acetamidei cu P 2 O 5 .
Utilizări
În industria chimică, acetonitrilul este utilizat în principal în purificarea butadienei și în producția de malononitril ; este adesea folosit ca solvent în sinteza antibioticelor. [3]
În laborator este utilizat ca solvent de polaritate medie, miscibil cu apa și diferiți solvenți organici, dar nemiscibil cu hidrocarburi saturate. Este lichid într-un interval foarte larg de temperatură, are o constantă dielectrică ridicată (38,8) și un moment dipolar de 3,84 D , [4] și poate solubiliza o varietate de compuși atât ionici, cât și nepolari. Este folosit în mod util ca fază mobilă în tehnici analitice precum HPLC și HPLC-MS .
În chimia organică, precum și un solvent poate fi utilizat ca component (bloc de construcție) la doi atomi de carbon [8] pentru sinteza altor compuși, cum ar fi acet amidina , tiamina și acidul 1-naftalenacetic . [9] Reacția cu clorură de cianogen duce la malononitril . [4]
În chimia coordonării, pe lângă faptul că este un solvent, acetonitrilul este utilizat și ca ligand, fiind o moleculă cu caracteristici de bază . Ca liant are caracteristica de a fi ușor de înlocuit în reacțiile de substituție a ligandului . [10] [11] [12]
Toxicitate
Acetonitrilul este un compus toxic , deși într-o măsură mai mică decât alți nitrili, cum ar fi propionitrilul și butironitrilul . [2] Compusul este toxic prin inhalare, ingestie și contact cu pielea. Irită puternic ochii și provoacă tulburări în sistemul cardiovascular și sistemul nervos central. Intoxicația cu acetonitril poate apărea chiar la câteva ore după contaminare, deoarece organismul îl metabolizează în diverse produse, inclusiv cianură de hidrogen și ion tiocianat . Inhalarea unor cantități mari cauzează dureri de cap, greață, dureri abdominale, scăderea tensiunii arteriale și insuficiență respiratorie care poate duce la moarte. Nu există date care să indice efecte cancerigene. [1]
Notă
- ^ a b c d e f g h i GESTIS 2016
- ^ a b Patnaik 2007
- ^ a b c Chenier 2002
- ^ a b c d și Pollak și Romeder 2002
- ^ Karakida și colab. 1974
- ^ PA Steiner și W. Gordy, Journal of Molecular Spectroscopy , vol. 21, 1966, p. 291.
- ^ Dumas 1847
- ^ DiBiase și colab. 1984
- ^ Wexler 2005
- ^ Oro și Sola 2001
- ^ Company și colab. 2012
- ^ Ojima și colab. 2014
Bibliografie
- ( EN ) PJ Chenier, Survey of Industrial Chemistry , ediția a 3-a, New York, Kluwer, 2002, ISBN 0-306-47246-5 .
- ( EN ) A. Company, J. Lloret, L. Gomez și M. Costas, Alkane C - H Oxigenare catalizată de complexe metalice de tranziție , în P. Pérez (editat de), Alkane CH Activation by Single-Site Metal Catalysis , Dordrecht , Springer, 2012, ISBN 978-90-481-3697-1 .
- ( EN ) SA DiBiase, JR Beadle și GW Gokel, Sinteza nitrililor α, β-nesaturați din acetonitril: Ciclohexilideneacetonitril și cannamonitril , în Org. Sintetizator. , vol. 62, 1984, p. 179, DOI : 10.15227 / orgsyn.062.0179 .
- ( EN ) Dumas, Action de acid phosphorique anhydre sur les sels ammoniacaux , în Comptes rendus , vol. 25, 1847, pp. 383-384.
- GESTIS, Acetonitril , pe gestis-en.itrust.de , 2016. Adus pe 13 ianuarie 2017 . Pagina Acetonitril din baza de date GESTIS.
- ( EN ) K. Karakida, T. Fukuyama și K. Kuchitsu, Structuri moleculare ale cianurii de hidrogen și ale acetonitrilului, studiate prin difracție cu electronii de gaz , în Buletinul Societății Chimice din Japonia , vol. 47, nr. 2, 1974, pp. 299-304, DOI : 10.1246 / bcsj.47.299 .
- ( EN ) I. Ojima, AT Vu și D. Bonafoux, Clasa de produs 5: Complexe organometalice ale rodiului, în M. Lautens (eds), Știința sintezei: Metode Houben-Weyl de transformări moleculare , vol. 1, Stuttgart, Georg Thieme, 2014, ISBN 3-13-112131-9 .
- ( EN ) LA Oro și E. Sola, Aspecte mecaniciste ale activării și catalizei dihidrogenului prin complexe dinucleare , în M. Peruzzini și R. Poli (ed.), Recent Advances in Hydride Chemistry , Amsterdam, Elsevier, 2001, ISBN 0- 444 -50733-7 .
- ( EN ) P. Patnaik, Un ghid cuprinzător al proprietăților periculoase ale substanțelor chimice , ediția a III-a, Wiley-Interscience, 2007, ISBN 0-471-71458-5 .
- (RO) P. Pollak și G. Romeder, nitrili, în Enciclopedia Ullmann de Chimie Industrială , Wiley-VCH, 2002, DOI : 10.1002 / 14356007.a17_363 .
- ( EN ) P. Wexler (eds), Encyclopedia of Toxicology , vol. 1, ediția a II-a, Elsevier, 2005, ISBN 0-12-745354-7 .
Elemente conexe
Alte proiecte
-
 Wikționarul conține dicționarul lema « acetonitril »
Wikționarul conține dicționarul lema « acetonitril » -
 Wikimedia Commons conține imagini sau alte fișiere pe acetonitril
Wikimedia Commons conține imagini sau alte fișiere pe acetonitril
| Controlul autorității | LCCN (EN) sh85000464 · GND (DE) 4141247-3 |
|---|