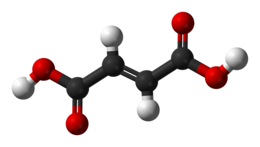
Acid fumaric
| Acid fumaric | |
|---|---|
| Numele IUPAC | |
| Acid E- butendenic | |
| Denumiri alternative | |
| acid trans-butendenic acid trans-1,4-butendenic | |
| Caracteristici generale | |
| Formula moleculară sau brută | C 4 H 4 O 4 |
| Masa moleculară ( u ) | 116.07 |
| Aspect | solid cristalin alb |
| numar CAS | |
| Numărul EINECS | 203-743-0 |
| PubChem | 444972 |
| DrugBank | DB01677 |
| ZÂMBETE | C(=CC(=O)O)C(=O)O |
| Proprietăți fizico-chimice | |
| Densitate (g / cm 3 , în cs ) | 1,635 g / cm3 (20 ° C) |
| Constanta de disociere a acidului (pKa) la 291 K. | pKa1 = 3,03, pKa2 = 4,44 |
| Solubilitate în apă | 6,3 g / l la 20 ° C |
| Temperatură de topire | 287 ° C (560 K) |
| Temperatura de fierbere | 290 ° C (563 K) |
| Informații de siguranță | |
| Punct de flacără | 273 ° C (cupă deschisă: 546 K) |
| Simboluri de pericol chimic | |
 | |
| Atenţie | |
| Fraze H | 319 |
| Sfaturi P | 305 + 351 + 338 [1] |
Acidul fumaric (de asemenea acid trans-butendic ) este un acid natural găsit în fructe și legume și a fost izolat în rădăcinile plantei erbacee sălbatice Fumaria officinalis ( Fumariaceae ) din care derivă numele.
Acidul fumaric este izomer al acidului maleic (acid cis-butendenic). Cele două substanțe sunt izomeri stabili și distincti, deoarece rotația în jurul unei duble legături carbon-carbon este împiedicată, deoarece tranziția dintre izomerii cis (Z) și trans (E) posedă o energie de activare considerabilă.
Caracteristicile celor doi acizi sunt foarte diferite, de exemplu acidul maleic este toxic, în timp ce fumarul este o biomoleculă fundamentală și este utilizat ca medicament și în produsele alimentare.
Este produs industrial atât prin fermentare, cât și prin sinteză.
Sinteză
Acidul fumaric a fost preparat mai întâi din acid succinic . [2] O cale tradițională de sinteză implică oxidarea furfuralului (obținută din transformarea porumbului) folosind un clorat în prezența unui catalizator pe bază de vanadiu . [3] În prezent, sinteza industrială a acidului fumaric se bazează în principal pe izomerizarea catalitică a acidului maleic în soluții apoase la pH scăzut. Acesta din urmă este accesibil în volume mari ca produs al hidrolizei anhidridului maleic , produs de oxidarea catalitică a benzenului sau butanului. [4]
Biologie
Acidul fumaric se găsește în plantele din genul fumaria (de exemplu Fumaria officinalis ), în ciupercile porcini (în special în Boletus fomentarius var. Pseudo-igniarius ), în licheni și în Cetraria islandica .
Fumaratul, prin urmare forma sa anionică, este un intermediar în ciclul acidului citric utilizat de celule pentru a produce energie sub formă de adenozin trifosfat (ATP) din alimente. Se formează prin oxidarea succinatului dehidrogenazei succinatului . Apoi fumaratul este transformat din fumarat în malat. Pielea umană produce în mod natural acid fumaric atunci când este expusă la lumina soarelui. [5]
Utilizări
Medicament
Este utilizat pentru tratamentul psoriazisului . Se administrează în doze de 60-105 mg pe zi și poate fi crescut până la 1290 mg. De asemenea, a fost aprobat pentru tratamentul sclerozei multiple . Efectele secundare pot include tulburări gastro-intestinale și renale sau roșeață a pielii. În 2014 a existat un caz de LMP (leucoencefalopatie multifocală progresivă) la un pacient cu leucopenie . [ fără sursă ]
Industria alimentară
A fost folosit ca stabilizator pentru diverse produse și ca regulator al acidității în produsele alimentare din 1946, înlocuind în general acidul tartric și uneori acidul citric . Este notat cu inițialele E297 . [6]
Alte utilizări
Acidul fumaric este utilizat la fabricarea rășinilor poliesterice și a alcoolilor zahărului și ca mordant pentru coloranți. De la începutul secolului al XXI-lea a fost folosit pentru a sintetiza una dintre primele structuri metal-organice care prezintă aplicații comerciale datorită remarcabilei sale proprietăți mecanice și de adsorbție, în combinație cu o toxicitate scăzută în comparație cu alte MOF bine studiate. [7]
Notă
- ^ Foaie informativă cu acid fumaric pe IFA-GESTIS Arhivat 16 octombrie 2019 la Internet Archive .
- ^ (EN) J. Volhard, Darstellung von Maleïnsäureanhydrid , în Justus Liebigs Annalen der Chemie, vol. 268, nr. 1-2, 1 ianuarie 1892, pp. 255–256, DOI : 10.1002 / jlac.18922680108 / abstract . Adus la 30 iunie 2016 .
- ^ Milas, NA "Acid fumaric" Sinteza organică 1943, volumul colectiv 2, pagina 302. Versiune online
- ^ Brevetul britanic nr. 775.912, publicat la 29 mai 1957, de Monsanto Chemical Company.
- ^ Ingrediente active utilizate în produsele cosmetice: sondaj de siguranță , Consiliul Europei. Comitetul de experți în domeniul produselor cosmetice
- ^ Actualii aditivi aprobați de UE și numerele lor E , la food.gov.uk.
- ^ (EN) Pascal G. Yot, Louis Vanduyfhuys și Elsa Alvarez, Performanța de stocare a energiei mecanice a unui cadru metal-organic fumarat de aluminiu , în Chem. Știință , vol. 7, nr. 1, 17 decembrie 2015, pp. 446-450, DOI : 10.1039 / c5sc02794b . Adus la 30 iunie 2016 .
Elemente conexe
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere despre acidul fumaric
Wikimedia Commons conține imagini sau alte fișiere despre acidul fumaric
linkuri externe
- ( EN ) Acid fumaric / acid fumaric (altă versiune) , în Encyclopedia Britannica , Encyclopædia Britannica, Inc.
| Controlul autorității | GND ( DE ) 4155633-1 |
|---|