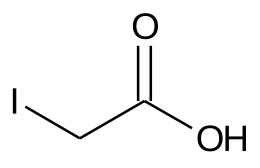
Acid Idoacetic
| Acid Idoacetic | |
|---|---|
| Caracteristici generale | |
| Formula moleculară sau brută | C 2 H 3 O 2 I |
| Masa moleculară ( u ) | 185,96 g / mol |
| Aspect | alb solid |
| numar CAS | |
| Numărul EINECS | 200-590-1 |
| PubChem | 5240 |
| ZÂMBETE | C(C(=O)O)I |
| Proprietăți fizico-chimice | |
| Solubilitate în apă | 600 g / l (20 ° C) |
| Temperatură de topire | 80 ° C (353 K) |
| Informații de siguranță | |
| Simboluri de pericol chimic | |
  | |
| Pericol | |
| Fraze H | 301 - 314 |
| Sfaturi P | 260 - 301 + 310 - 303 + 361 + 353 - 305 + 351 + 338 - 405 - 501 [1] [2] |
Acidul idoacetic este un acid carboxilic . Structura sa este similară cu cea a unei molecule de acid acetic în care unul dintre atomii de hidrogen din gruparea metil a fost înlocuit cu un atom de iod . La temperatura camerei apare ca un solid alb cu miros înțepător. Este un compus toxic și coroziv.
La determinarea secvenței de aminoacizi a proteinelor este necesar să se rupă punțile disulfidice (care se formează între două reziduuri de cisteină ) pentru a separa un lanț polipeptidic de celălalt și pentru a permite lanțului polipeptidic să fie complet liniar. De fapt, reziduurile unei polipeptide care se găsesc între două reziduuri Cys unite printr-o punte disulfură pot fi inaccesibile enzimelor și reactivilor utilizați pentru secvențiere.
Acidul idoacetic este adesea folosit ca agent alchilant pentru a proteja reziduurile de aminoacizi ale cisteinei care s-au format astfel. Reacția se numește „carboxi-metilare” și este covalentă, deci ireversibilă:
Acest lucru previne oxidarea oxigenului de la reformarea punților disulfură.
Cu toate acestea, proteina capătă o sarcină negativă suplimentară pentru fiecare cisteină care este alchilată. În studiile biochimice sau de biologie moleculară, tratarea probelor biologice proaspete (culturi celulare, țesuturi omogenizate, ser etc.) în soluții tampon speciale și / sau soluții de denaturare cu o concentrație finală de acid iodoacetic în ordinea a 10-50 milimolari (mM), și prin incubarea ulterioară la 37 ° C timp de 1 sau 2 ore, este posibil să se obțină alchilarea completă a tuturor grupărilor tiolicil libere ale proteinelor.
Prin acest proces este posibil să se stabilească proporția substraturilor reduse și oxidate și starea redox a proteinelor din probele biologice. De fapt, prin electroforeza nativă (fără adăugarea de dodecil sulfat de sodiu sau SDS ) în gel de poliacrilamidă (PAGE) , este posibilă separarea tuturor speciilor cu starea lor redox respectivă. De fapt, electroforeza PAGE separă proteinele în funcție de numărul de sarcini electrice totale ale proteinelor. Electroforeza normală (SDS-PAGE), pe de altă parte, separă proteinele pe baza masei moleculare, deoarece SDS (detergent) maschează sarcinile electrice.
O altă aplicație biochimică a acidului iodoacetic este cea a otravă cu glicoliză . De fapt, alchilează reziduul de cisteină în situl catalitic al gliceraldehidei-3-fosfat dehidrogenazei (GAPDH) și conduce la blocarea utilizării glucozei în interiorul celulei.
Notă
- ^ Foaie de acid Idoacetic pe IFA-GESTIS
- ^ Eliminați produsul și recipientul în conformitate cu legile în vigoare.
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere despre acid iodoacetic
Wikimedia Commons conține imagini sau alte fișiere despre acid iodoacetic