Actinoizi
| Numar atomic | Nume | Simbol |
|---|---|---|
| 89 | Actinium | B.C |
| 90 | Toriu | Th |
| 91 | Protactiniu | Pa |
| nouăzeci și doi | Uraniu | U |
| 93 | Neptunium | Np |
| 94 | Plutoniu | Pu |
| 95 | Americium | A.m |
| 96 | Ciudăţenie | Cm |
| 97 | Berkelio | Bk |
| 98 | Californium | Cf |
| 99 | Einsteinium | Ex |
| 100 | Fermius | Fm |
| 101 | Mendelevio | Md |
| 102 | Nobelium | Nu |
| 103 | Laurentius | Lr |

Seria de actinoizi (anterior actinide ) se referă la cele cincisprezece elemente chimice cuprinse între actinium și laurentium pe tabelul periodic , cu numere atomice cuprinse între 89 și 103 inclusiv. [1] [2] [3]
Numele derivă din primul element al seriei, actinium și, de obicei, elementul generic din această categorie este indicat cu simbolul An . Toți actinoizii fac parte din blocul f al tabelului periodic, adică umplu orbitalul 5f; Laurentius constituie o excepție, deoarece face parte din blocul d. Această divergență provoacă confuzie cu privire la dispunerea corectă a elementelor actinoide în tabelul periodic.
Pentru caracteristicile chimice, acestea sunt foarte asemănătoare cu elementele din seria lantanidelor : actinoizii cu cel mai mare număr atomic nu sunt disponibili în natură datorită timpului de înjumătățire foarte scurt: aproape toți actinoizii sunt puternic radioactivi . Mai mult, plutoniul este, de asemenea, extrem de otrăvitor .
De asemenea, au o bună electropozitivitate : aceasta înseamnă că tind să renunțe la electroni pentru a deveni cationi (comportamentul tipic al metalelor ).
Proprietățile lor chimice sunt atât de similare încât la început întreaga serie a fost considerată ca un singur element: de fapt, au o electronegativitate foarte asemănătoare (1,3); au tendința de a face electronul unic al învelișului 6 să treacă în învelișul subiacent 5f; au o densitate destul de mare și pot produce mai mulți alotropi . Cu toate acestea, ele diferă între ele dacă examinăm numerele de oxidare : dacă pentru lantanide este +3, nu se poate spune același lucru pentru actinoizii, care au un număr mai mare și doar actinoizii grei revin să aibă numărul de oxidare +3.
La fel ca lantanii ( Ln ), actinoizii ( An ) sunt, de asemenea, reprezentați uneori în afara tabelului periodic, în același mod și din aceleași motive: ocuparea electronică a orbitalelor de tip f, dar și o claritate mai mare în tabelul periodic (pentru a preveni răspândirea acestuia) excesiv).
Istorie

Ca și în cazul lantanoizilor, actinoizii formează o familie de elemente cu proprietăți similare în care coexistă două grupuri suprapuse: elementele transuranice care urmează uraniul și elementele transplutonice, adică cele care se succed către plutoniu deplasându-se către dreptul în perioadă . În comparație cu lantanidele care, cu excepția prometiului , se găsesc în natură în cantități destul de apreciabile, elementele acestei serii sunt destul de rare și sintetizate în principal în laborator. Cele mai abundente, precum și cele mai ușor de preparat, sunt uraniul și toriul , urmate de americium , actiniu , protactiniu și neptuniu . [4]
Descoperirea majorității acestor elemente este destul de recentă, datând din secolul trecut. Existența unor elemente transuranice a fost sugerată de Enrico Fermi , pe baza experimentelor sale nucleare, încă din 1934. [5] [6] În orice caz, la momentul respectiv erau cunoscute doar patru lantanide și încă nu se presupunea că ar putea forma o familie precum lantanidele. Opinia predominantă a fost aceea care a dominat în domeniul cercetării științifice până în anii 1940 , și anume că erau elemente regulate aparținând perioadei a 7-a . Încet, sinteza altor elemente sau compuși transuranici a subminat această teorie larg răspândită, determinând chimiștii să revizuiască configurația tabelului periodic. Cele mai importante experimente sunt cele efectuate la Berkeley , California, între 1941 și 1944 și care au dovedit existența americiului, curiozității, berkeliului și multe altele.
În ciuda descoperirii senzaționale până la sfârșitul anilor 1950 , comunitatea științifică nu și-a exprimat o opinie comună cu privire la plasarea corectă a actinoizilor în sistemul periodic. De fapt, până atunci existau așa-numita „ipoteză attinidică” (ipoteză actinidică), adică un set de diverse propuneri cu privire la modul de „clasificare” a elementelor nou descoperite. [7] [8] [9]
De la actiniu la uraniu
Primii actinoizi descoperiți au fost uraniul și respectiv toriul. Uraniul (al cărui simbol chimic este U ) a fost identificat în 1789 de chimistul german Martin Heinrich Klaproth în cadrul uraninitului mineral, cunoscut și sub numele de pitchblende. Klaproth a decis să numească elementul uraniu cu referire la planeta Uranus , descoperită cu doar opt ani mai devreme. [10] Omul de știință a reușit, de asemenea, să precipite un compus galben (potrivit unor cercetători moderni, acesta era diuranat de sodiu) prin dizolvarea unei probe de pitchblendă în acid azotic și neutralizarea soluției obținute cu puțin hidroxid de sodiu . Reducând compusul rezultat în pulbere și folosind cărbune , a extras o substanță neagră pe care a confundat-o inițial cu un metal. [11] Doar 60 de ani mai târziu, francezul Eugène-Melchior Péligot a identificat compusul Klaproth ca oxid de uraniu (UO 2 ). Péligot a izolat, de asemenea, prima probă de uraniu metalic prin încălzirea tetraclorurii de uraniu cu potasiu și calcularea masei sale atomice cu o valoare de aproximativ 120 u [12] , corectat de Dmitrij Mendeleev în 1872 cu valoarea de 240 u, conform legilor periodicității. Calculele lui Mendeleev au fost confirmate în 1882 de K. Zimmerman. [13] [14]
Toriu oxid (THO 2) a fost în loc descoperit de Friedrich Wöhler într - un mineral găsit în Norvegia în 1827. [15] Jöns Jacob Berzelius analizat și adus la lumină detalii mai interesante ale acestui material în 1828. Ca Péligot, Berzelius se va face mai târziu. Redus tetraclorură de toriu cu potasiu și a izolat metalul pentru prima dată, dându-i numele de toriu cu referire la Thor , zeul norvegian al fulgerului și simbolul Th . [16] [17]
Când graba pentru noi elemente părea să se fi oprit, în 1899, André-Louis Debierne , un asistent al lui Marie Curie , a descoperit actiniul ( Ac ) analizând deșeurile de pitchblendă rămase după ce au fost îndepărtate urmele din minereul de radiu și poloniu. . Debierne a descris substanța ca fiind similară cu titanul și, după un studiu atent, a devenit convins că era, dimpotrivă, mai asemănătoare cu toriul (1900). Descoperirea lui Debierne de actiniu a fost pusă la îndoială în 1971, iar cercetările specifice din 2000 au arătat că publicațiile lui Debierne din 1904 le contrazic pe cele din 1899-1900. Concluzia este că Debierne nu a izolat un element nou, deși a prezis indirect existența acestuia. Există, de asemenea, îndoieli cu privire la originea numelui. In prezent, cu o oarecare certitudine, se crede că Victor Goldschimidt, în 1937, a dat elementului actiniu nume, derivat din greaca ακτίς, ακτίνος (Aktis, aktinos) , cu semnificația „rază de lumină“ , sau de asemenea , „beam“, deoarece a fost descoperit doar din analiza radiațiilor emise de nuclizii copiilor sau radioizotopii produși de decăderea acestuia. Studii recente sugerează că actiniul propriu-zis nu a fost sintetizat înainte de 1950.
Protactiniu ( Pa ) a fost izolat în 1900 de William Crookes , deși există mai multe îndoieli cu privire la acesta. Pe de altă parte, este sigur că a fost identificat în 1913 de Kasimir Fajans și Oswald Helmuth Göhring în timpul studiilor lor asupra decăderii izotopului 238 U. Cei doi oameni de știință au numit noul element cortium , din latina brevis , adică „scurt „referindu-ne la timpul de înjumătățire de doar 1,17 minute. De-a lungul anilor numele a fost schimbat în protactiniu (din grecescul πρῶτος + ἀκτίς care înseamnă „prima rază”), adoptat de comunitatea științifică și literatura începând din 1918 când două grupuri de oameni de știință, unul condus de austriaca Lise Meitner și Germanul Otto Hahn și celălalt condus de Frederick Soddy și John Cranston în Marea Britanie, au descoperit independent izotopul 231 Pa. În 1949 numele a fost redus la protattinium (deși unele texte actuale poartă ambii termeni). Mai multe informații despre proprietățile și comportamentul chimic al protactiniei au apărut în 1960, când Maddock și colaboratorii săi din Marea Britanie au produs aproximativ 130 de grame de protactiniu din 60 de tone de deșeuri rămase după extracția uraniului din principalul său minereu.
Descoperirea neptuniului și experimentele de la Berkeley
În 1934, în Statele Unite, Enrico Fermi și cercul său de colaboratori desfășurau experimente la nivel nuclear, dintre care multe se vor dovedi cruciale pentru construirea centralelor nucleare și a armelor de distrugere în masă . În timpul acestor teste, au apărut noi izotopi care nu fuseseră studiați până acum. Cu toate acestea, descoperirea nu a provocat senzație și mult timp așa-numitele transuranici au rămas un mister.
Neptunul (indicat cu Np și cu numele derivat de pe planeta Neptun , care în sistemul solar îl urmărește pe Uranus) a fost descoperit de Edwin McMillan și Philip Abelson în 1940 în Berkeley, California. [18] La facilitățile universitare, cei doi oameni de știință au izolat un nou element care produce izotopul 239 Np (cu un timp de înjumătățire estimat de 2,4 zile) prin bombardarea uraniului cu neutroni lent. A fost primul element transuraniu care a fost sintetizat în laborator.[19] Cei doi chimiști au decis să-l numească neptuniu cu referire la elementul anterior, uraniu, menținând astfel un fel de „nume cosmologic” (același lucru este valabil și pentru plutoniu).
| Element | Descoperire | Metodă |
|---|---|---|
| Neptunium | 1940 | Bombardând 238 U cu neutroni |
| Plutoniu | 1941 | Bombardarea a 238 U cu deutoni |
| Americium | 1944 | Bombardând 239 Pu cu neutroni |
| Ciudăţenie | 1944 | Bombardând 239 Pu cu particule α |
| Berkelio | 1949 | Bombardând 241 Am cu particule α |
| Californium | 1950 | Bombardarea 242 Cm cu particule α |
| Einsteinium | 1952 | Produs de explozii nucleare |
| Fermius | 1952 | Produs al exploziilor nucleare |
| Mendelevio | 1955 | Prin bombardarea a 253 Es cu particule α |
| Nobelium | 1965 | Bombardând 243 Am cu N sau 238 U cu particule α |
| Laurentius | 1961-1971 | Bombardarea 252 Cf cu B |
Anii 1940 au fost o perioadă plină de descoperiri în domeniul chimic. În urma succesului lui McMillan și Abelson cu tehnica de bombardare a uraniului în 1941 și mai târziu din 1944 până în anii 1950 , Glenn Seaborg și echipa sa de la Universitatea Berkely au sintetizat câteva elemente noi:
- plutoniu (de la numele planetei Pluto și cu simbolul Pu );
- americium ( Am ) din continentul Americii, analog elementului de mai sus din tabelul periodic, europium;
- curio ( Cm ), în onoarea soților Pierre și Marie Curie ;
- berkelio (în italiană transcris și ca berchelio , Bk ), din orașul Berkeley , în California;
- californium ( Cf ), își ia numele din statul în care a fost descoperit, California;
- einstenio ( Es ), în cinstea fizicianului Albert Einstein ;
- fermio ( Fm ), în cinstea fizicianului Enrico Fermi ;
- nobelio ( Nu ), în onoarea lui Nobel.
În anii următori, a fost sintetizat și elementul 106, denumit recent seaborge ( Sg ) în onoarea lui Seaborg. În cele din urmă, cercetătorii au identificat peste 100 de tipuri diferite de radioizotopi.
Așa cum am subliniat, toate aceste elemente transuranice sunt produse în laborator și nu se găsesc în cantități apreciabile în natură, cu câteva excepții. Cu toate acestea, ar trebui luate în considerare numeroasele teste nucleare efectuate atât pe uscat, cât și în atmosfera superioară. De fapt, precipitațiile radioactive care au urmat diferitelor explozii nucleare care au avut loc înainte de anii 1980 au eliberat urme mai mult sau mai puțin semnificative ale acestor elemente în mediu.
În acest fel, Enrico Fermi și colaboratorii săi, folosind primul reactor nuclear, au obținut cantități semnificative de plutoniu-239, utilizate ulterior pentru armele nucleare. [22]
Izotopi
Începând cu 2010, au fost identificate treizeci și unu de izotopi de actiniu și opt stări izomerice excitate ale unora dintre nuclizii săi. Trei dintre acești izotopi, 225 Ac, 227 Ac și 228 Ac, au fost găsiți în natură (ținând seama și de efectele post-test nucleare) în timp ce toți ceilalți sunt artificiali; numai izotopii naturali găsesc aplicații industriale. Actinium-225 este un membru al seriei de radioizotopi de neptuni. A fost descoperit în 1947 ca produs de fisiune al uraniului-233, este un emițător de radiații α, care au un timp de înjumătățire (t ½ ) de aproximativ 10 zile. Actinium-225 este mai puțin disponibil decât actinium-228, dar este mai promițător ca radiotrasor. Actinium-227 (cu un timp de înjumătățire de 21-22 de ani) poate fi găsit în toate minereurile de uraniu, dar în cantități foarte mici. Un gram de uraniu conține numai 2 × 10 −10 g din 227 î.Hr.
Actinide minore
Prin actinide minore înțelegem toți actinoizii, cu excepția plutoniului și uraniului (numiți actinide majore ), care alcătuiesc combustibilul nuclear uzat.
Proprietate
Actinoizii au proprietăți foarte asemănătoare cu cele ale lantanilor. Cojile de electroni 6d și 7s sunt umplute în actiniu și toriu, iar 5f este umplut pe măsură ce numărul atomic crește. 4f este plin de lantanide. Primele dovezi experimentale ale completitudinii orbitalului 5f în actinide au fost obținute de McMillan și Abelson în 1940, când au izolat neptuniul. La fel ca și lantanoizii, aceste elemente suferă și o reducere a razei (numită contracție actinidică , similar contracției lantanoide ).
| Proprietate | B.C | Th | Pa | U | Np | Pu | A.m | Cm | Bk | Cf | Ex | Fm | Md | Nu | Lr |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Sarcină | 89 | 90 | 91 | nouăzeci și doi | 93 | 94 | 95 | 96 | 97 | 98 | 99 | 100 | 101 | 102 | 103 |
| Masă atomică | [227] | 232.0381 | 231.03588 | 238.02891 | [237] | [244] | [243] | [247] | [247] | [251] | [252] | [257] | [258] | [259] | [266] |
| Număr de izotopi naturali [25] | 3 | 9 | 5 | 9 | 4 | 5 | 5 | 8 | 2 | 5 | - | - | - | - | - |
| Izotopi naturali [25] [26] | 225, 227 ÷ 228 | 226 ÷ 232, 234 ÷ 235 | 231, 233 ÷ 236 | 232 ÷ 240 | 237 ÷ 240 | 238 ÷ 240, 242, 244 | 241 ÷ 245 | 242 ÷ 249 | 249 ÷ 250 | 249 ÷ 253 | - | - | - | - | - |
| Izotop cu viață mai lungă | 227 | 232 | 231 | 238 | 237 | 244 | 243 | 247 | 247 | 251 | 252 | 257 | 258 | 259 | 266 |
| Timpul de înjumătățire al celui mai uzat izotop | 21,8 ani | 14 miliarde de ani | 32 500 de ani | 4,47 miliarde de ani | 2,14 milioane de ani | 80,8 milioane de ani | 7 370 de ani | 15,6 milioane de ani | 1 400 de ani | 900 de ani | 1,29 ani | 100,5 zile | 52 de zile | 58 min | 11 ore |
| Configurare electronică de bază | 6d 1 7s 2 | 6d 2 7s 2 | 5f 2 6d 1 7s 2 sau 5f 1 6d 2 7s 2 | 5f 3 6d 1 7s 2 | 5f 4 6d 1 7s 2 sau 5f 5 7s 2 | 5f 6 7s 2 | 5f 7 7s 2 | 5f 7 6d 1 7s 2 | 5f 9 7s 2 sau 5f 8 6d 1 7s 2 | 5f 10 7s 2 | 5f 11 7s 2 | 5f 12 7s 2 | 5f 13 7s 2 | 5f 14 7s 2 | 5f 14 7s 2 7p 1 |
| Stări de oxidare | 2, 3 | 2, 3, 4 | 2, 3, 4, 5 | 2, 3, 4, 5, 6 | 3, 4, 5 , 6, 7 | 3, 4 , 5, 6, 7, 8 | 2, 3 , 4, 5, 6, 7 | 2, 3 , 4, 6, 8 | 2, 3 , 4 | 2, 3 , 4 | 2, 3 , 4 | 2, 3 | 2, 3 | 2 , 3 | 3 |
| Raza metalică (nm) | 0,203 | 0.180 | 0,162 | 0,153 | 0,150 | 0,162 | 0,173 | 0,174 | 0,170 | 0,186 | 0,186 | ? 0,198 | ? 0,194 | ? 0,197 | ? 0,171 |
| Raza ionică (în nm): Un 4+ Un 3+ | - 0,126 | 0,114 - | 0,104 0,118 | 0,103 0,118 | 0,101 0,166 | 0,100 0,115 | 0,099 0,114 | 0,099 0,122 | 0,097 0,110 | 0,096 0,109 | 0,085 0,098 | 0,084 0,091 | 0,084 0,090 | 0,084 0,095 | 0,083 0,088 |
| Temperatura (° C): fuziune fierbere | 1050 3198 | 1842 4788 | 1568 ? 4027 | 1132.2 4131 | 639 ? 4174 | 639.4 3228 | 1176 ? 2607 | 1340 3110 | 986 2627 | 900 ? 1470 | 860 ? 996 | 1530 - | 830 - | 830 - | 1630 - |
| Densitate (g / cm³) | 10.07 | 11,78 | 15.37 | 19.06 | 20.45 | 19,84 | 11.7 | 13.51 | 14,78 | 15.1 | 8,84 | ||||
| Potențial standard (în V): E ° ( 4+ / 0 ) E ° ( 3+ / 0 ) | - −2.13 | −1,83 - | −1,47 - | −1,38 −1,66 | −1.30 −1,79 | −1,25 −2,00 | −0,90 −2.07 | −0,75 −2,06 | −0,55 −1,96 | −0,59 −1.97 | −0,36 −1,98 | −0,29 −1,96 | - −1,74 | - −1,20 | - −2.10 |
| Culoare [M (H 2 O) n] 4+ [M (H 2 O) n] 3+ | - Incolor | Incolor Albastru | Galben Albastru inchis | Verde Magenta | Galben verde Violet | Maro Viola | roșu Roz | Galben Incolor | Bej Galben verde | Verde Verde | - Roz | - - | - - | - - | - - |
| Starea de oxidare | 89 | 90 | 91 | nouăzeci și doi | 93 | 94 | 95 | 96 | 97 | 98 | 99 |
| +3 | Ac 3+ | Th 3+ | Pa 3+ | U 3+ | Np 3+ | Pu 3+ | Sunt peste 3 ani | Cm 3+ | Bk 3+ | Cf 3+ | Ex 3+ |
| +4 | Th 4+ | Pa 4+ | U 4+ | Np 4+ | Pu 4+ | Am 4+ ani | Cm 4+ | Bk 4+ | Cf 4+ | ||
| +5 | PaO + 2 | UO + 2 | NpO + 2 | PuO + 2 | AmO + 2 | ||||||
| +6 | UO 2+ 2 | NpO 2+ 2 | PuO 2+ 2 | AmO 2+ 2 | |||||||
| +7 | NpO 3+ 2 | PuO 3+ 2 | [AmO 6 ] 5− |
Proprietăți fizice
 | 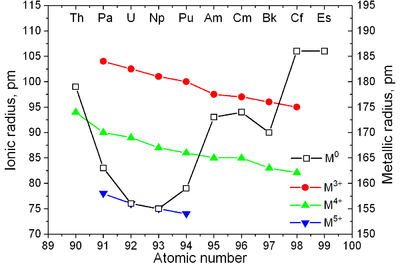 |
| Diagrama de fază a actinoizilor | Raze metalice și ionice ale actinoizilor [24] |
Actinoizii sunt metale tipice. Toate au o culoare alb-argintiu în stare metalică solidă, mai închisă când sunt lăsate în contact cu aerul. Sunt relativ foarte dense și cu plasticitate bună. În general, acestea tind să fie moi, până la punctul în care unele pot fi tăiate cu un cuțit. Rezistivitatea electrică variază de la 15 la aproximativ 150 µohm · cm .
Duritatea torului este similară cu cea a oțelului , prin urmare, dacă este încălzit, torul pur poate fi redus în foi sau transformat în fire subțiri (proprietăți tipice ale metalelor numite, respectiv, maleabilitate și ductilitate ). Toriu este aproape la jumătate mai dens ca uraniul și plutoniul, deși este mai greu decât ambele.
Toate actinidele sunt radioactive, paramagnetice și, cu excepția actiniului, au faze cristaline diferite: plutoniul are șapte, în timp ce uraniul, neptuniul și californiul au trei. Structurile cristaline ale protactiniului, uraniului, neptuniului și plutoniului nu au echivalente perfecte în lantanide și sunt în esență mai asemănătoare cu metalele de tranziție 3 d .
În general, toate actinidele sunt piroforice (sau pirofore ), sau „purtători de foc”: de fapt, dacă sunt fin divizate, se aprind spontan în aer. Punctul de topire al actinoizilor nu are o dependență specifică de numărul de electroni ai orbitalilor f . În orice caz, punctul neobișnuit de topire scăzut al neptuniului și plutoniului (aproximativ 640 ° C) poate fi explicat vorbind despre hibridizarea orbitalilor de 5 f și 6 d , cu formarea de legături direcționale în cadrul acestor metale.
| Lantanoizi | Ln 3+ , Å | Actinoizi | Un 3+ , Å | Un 4+ , Å |
|---|---|---|---|---|
| Lantanul | 1,061 | Actinium | 1.11 | - |
| Ceriu | 1,034 | Toriu | 1,08 | 0,99 |
| Praseodim | 1,013 | Protattinium | 1,05 | 0,93 |
| Neodim | 0,995 | Uraniu | 1,03 | 0,93 |
| Prometiu | 0,979 | Neptunium | 1,01 | 0,92 |
| Samariu | 0,964 | Plutoniu | 1,00 | 0,90 |
| Europium | 0,950 | Americium | 0,99 | 0,89 |
| Gadolinium | 0,938 | Ciudăţenie | 0,98 | 0,88 |
| Terbiul | 0,923 | Berkelio | - | - |
| Disprozie | 0,908 | Californium | - | - |
| Holmiu | 0,894 | Einsteinio | - | - |
| Erbiu | 0,881 | Fermius | - | - |
| Tuliu | 0,869 | Mendelevio | - | - |
| Ytterbium | 0,858 | Nobelium | - | - |
| Lutetium | 0,848 | Laurentius | - | - |
Proprietăți chimice
Aplicații
| Reactor nuclear[23] [29] [30] |
| Miezul majorității reactoarelor nucleare de a doua generație conține un set de tije metalice goale, de obicei aliaje de zirconiu, umplute cu aglomerate de combustibil nuclear. Cel mai frecvent combustibil este oxidul de uraniu-235 . Neutronii rapizi sunt încetiniți de moderatori, care conțin așa-numita apă grea. Progresul reacției este controlat prin introducerea de tije goale suplimentare în bor sau cadmiu sau un lichid absorbant, cum ar fi acidul boric. Reactoarele pentru producția de plutoniu se numesc reactoare de reproducere . |
Deși unii actinoizi au aplicații mici în viața de zi cu zi, cum ar fi detectoarele de fum (cu componente de americium [31] [32] ) sau ecranele de gaz, [33] aceste elemente sunt utilizate în principal pentru construirea armelor nucleare sau ca combustibili în reactoarele nucleare, [33] Acest lucru se datorează faptului că eliberează cantități mari de energie și, în condiții adecvate, pot iniția o reacție în lanț care se autosusține.
Din punct de vedere energetic, cel mai important izotop este cu siguranță uraniul-235. Este utilizat în reactoare termice, iar concentrația sa în uraniul normal nu depășește 0,72%. Acest izotop absoarbe neutronii termici eliberând multă energie. Este suficient să spunem că un gram de 235 U se transformă în aproximativ 1 MW pe zi. O importanță considerabilă este faptul că acest izotop emite mai mulți neutroni decât absoarbe; în atingerea masei critice, 235 U intră într-o reacție în lanț auto-susținută. De obicei, nucleul de uraniu se împarte în două fracțiuni cu eliberarea a doi sau chiar trei neutroni, de exemplu:
Alți izotopi promițători ai utilizării nucleare sunt toriu-232 și uraniu-233. [34] Emisia de neutroni în timpul fisiunii uraniului este importantă nu numai pentru menținerea reacției în lanț, ci și pentru sinteza metalelor actinoide mai grele. Uraniul-239 este transformat, prin decadere β, în plutoniu-239, care, la rândul său, poate suferi fisiune spontană. La urma urmei, trebuie să ne amintim că primul reactor nuclear nu a fost proiectat și apoi construit în scopuri energetice, ci pentru arme nucleare. Acest lucru sugerează cât de intensă este cercetarea științifică în acest domeniu.
Toxicitate
Substanțele radioactive pot compromite sănătatea oamenilor și a altor animale prin contaminarea locală pe piele, expunerea internă datorită ingestiei de izotopi radioactivi (numită otrăvire ) și expunerea externă excesivă la emisia de raze beta sau a razei de acțiune. Împreună cu radiul și elementele transuranice, actiniul este un element foarte periculos de manipulat, având în vedere radioactivitatea ridicată datorată activității specifice a radiației alfa. Caracteristica esențială a actiniului este capacitatea sa de a se acumula și de a rămâne pe suprafața oaselor pentru o lungă perioadă de timp. În faza inițială de otrăvire, actiniul se concentrează în ficat, din care apoi se răspândește în tot corpul. Doar o mică parte intră în sistemul circulator, cu atât mai puțin procentul de actiniu pe care corpul îl poate excreta prin urină. Deoarece se descompune repede, presupunând că poate fi îndepărtat rapid din corp, ar exista în continuare deteriorări grave ale organelor interne, puternic afectate de radiații. [35]

Elemente cu cel puțin un izotop stabil.
Elemente ușor radioactive: cel mai stabil izotop este cu adevărat de lungă durată, cu un timp de înjumătățire de peste 4 milioane de ani.
Elemente moderat radioactive: cel mai stabil izotop are un timp de înjumătățire între 800 și 34.000 de ani.
Elemente foarte radioactive: cel mai stabil izotop se descompune într-o zi sau în termen de 103 ani.
Elemente foarte radioactive: cel mai longeviv și stabil izotop are un timp de înjumătățire între câteva minute și o zi.
Elemente extrem de radioactive: cel mai stabil izotop are un timp de înjumătățire mai mic de un minut. Datorită instabilității ridicate, nu se știe nimic și nimic despre aceste elemente.
Protactiniu din organism tinde să se acumuleze în rinichi și oase. Doza maximă tolerabilă de către corpul nostru este de aproximativ 0,5 μg de 231 Pa. Acest izotop, care poate fi prezent în aer sub forma unui aerosol, poate fi chiar mai letal decât cianura de hidrogen . [36]
Plutoniul, atunci când intră în organism prin aer, mâncare otrăvită sau prin sânge (de exemplu printr-o rană) este depus în plămâni (dacă este inhalat) sau în oase și ficat. Doar 10% se răspândește în restul organelor și, din păcate, inevitabil rămâne acolo de zeci de ani. Reședința incredibilă a plutoniului în organism se explică prin solubilitatea redusă a acestuia în apă: dacă ar fi opusul, marea abundență de apă din corpul uman ar permite o expulzare mai mult sau mai puțin rapidă. Mai mult, unii izotopi ai plutoniului emit radiații alfa ionizante, potențial cancerigene, deoarece afectează celulele din jur. Este bine să ne amintim că particulele alfa nu sunt periculoase deoarece, în general, dacă nu sunt concentrate, nu sunt capabile să treacă prin straturi groase de materie (uneori sunt respinse de coli de hârtie). Totuși, dacă luăm în considerare faptul că distanța dintre sursa acestor radiații (atunci când se află în corp) și celulele este practic zero, devine evident de ce sunt atât de dăunătoare organismului, provocând mutații sau erori genetice. Din studiile efectuate pe animale, doza letală pentru oameni este de numai 22 mg pentru un adult mediu care cântărește 70 kg. Aceste cantități mici sunt practic invizibile la microscop și acest lucru complică efectuarea unei estimări mai mult sau mai puțin sigure a dozei letale. Se poate spune că contaminarea prin alimente este cea mai puțin periculoasă, precum și cea mai puțin probabilă, deoarece doar un procent foarte mic de plutoniu ar putea fi prins în organism, fără a fi expulzat. [37]
Utilizarea actinidelor în combustibili nucleari are beneficii incontestabile. Cu toate acestea, o problemă gravă o reprezintă radiotoxicitatea ridicată a acestor elemente atunci când sunt dispersate în mediu. [38] Utilizarea formelor chimice instabile de actinide în MOX nu respectă în mod adecvat standardele actuale de siguranță (2015). Este o adevărată provocare să dezvoltăm materiale capabile să conțină „amenințarea radioactivă” a elementelor actinoide exploatate în câmpul nuclear. Scopul este de a preveni eliberarea în mediu prin dezvoltarea de noi materiale pentru depozitare sigură. Dacă actinidele s-ar revărsa într-o zonă naturală diversă, acestea ar provoca otrăvirea acviferelor cu consecințe dezastruoase asupra lanțului alimentar și supraviețuirea speciilor vii din zonă. [39]
Notă
- ^ (RO) Tabel periodic al elementelor , pe iupac.org, IUPAC , 2003-2007. Adus la 23 februarie 2011 (arhivat din original la 17 mai 2008) .
- ^ (EN) Tabel periodic al elementelor (PDF) pe iupac.org, IUPAC , 2007.
- ^ (RO) Red Book (PDF) pe old.iupac.org, IUPAC , 2005.
- ^ Myasoedov, p. 7
- ^ Fermi, E., Producția posibilă a elementelor cu număr atomic mai mare de 92 , în Nature , vol. 133, nr. 3372, 1934, pp. 898–899, Bibcode : 1934 Nat . 133..898F , DOI : 10.1038 / 133898a0 .
- ^ Jagdish Mehra și Helmut Rechenberg, Dezvoltarea istorică a teoriei cuantice , Springer, 20 aprilie 2001, pp. 966–, ISBN 978-0-387-95086-0 . Adus pe 19 iunie 2011 .
- ^ Seaborg, GT, Cap. 118. Originea conceptului de actinidă, în KA Gschneidner, Jr., L, Eyring, GR Choppin și GH Landet (ed.), Manual despre fizica și chimia pământurilor rare , 18 - Lantanide / Actinide: chimie, Elsevier, 1994, pp. 4-6, 10-14.
- ^ JC Wallmann, The first isolations of the transuranium elements: A historical survey , in Journal of Chemical Education , vol. 36, n. 7, 1959, p. 340, Bibcode : 1959JChEd..36..340W , DOI : 10.1021/ed036p340 .
- ^ Myasoedov, p. 9
- ^ Greenwood, p. 1250
- ^ Martin Heinrich Klaproth , Chemische Untersuchung des Uranits, einer neuentdeckten metallischen Substanz , in Chemische Annalen , vol. 2, 1789, pp. 387–403.
- ^ E.-M. Péligot, Recherches Sur L'Uranium , in Annales de chimie et de physique , vol. 5, n. 5, 1842, pp. 5–47.
- ^ Ingmar Grenthe, Uranium , in The Chemistry of the Actinide and Transactinide Elements , 2006, DOI : 10.1007/1-4020-3598-5_5 .
- ^ Zimmerman, Ann., 213, 290 (1882); 216, 1 (1883); Ber. 15 (1882) 849
- ^ Golub, p. 214
- ^ Berzelius, JJ, Untersuchung eines neues Minerals und einer darin erhalten zuvor unbekannten Erde (Investigation of a new mineral and of a previously unknown earth contained therein) , in Annalen der Physik und Chemie , vol. 16, n. 7, 1829, pp. 385–415, Bibcode : 1829AnP....92..385B , DOI : 10.1002/andp.18290920702 .
- ^ Berzelius, JJ, Undersökning af ett nytt mineral (Thorit), som innehåller en förut obekant jord" (Investigation of a new mineral (thorite), as contained in a previously unknown earth) , in Kungliga Svenska Vetenskaps Akademiens Handlingar (Transactions of the Royal Swedish Science Academy) , 1829, pp. 1–30.
- ^ Mcmillan, Edwin e Philip Abelson, Radioactive Element 93 , in Physical Review , vol. 57, n. 12, 1940, pp. 1185–1186, Bibcode : 1940PhRv...57.1185M , DOI : 10.1103/PhysRev.57.1185.2 .
- ^ VA Mikhailov (a cura di), Analytical chemistry of neptunium , Moscow, Nauka, 1971.
- ^ Greenwood, p. 1252
- ^ Nobelio e laurenzio sono stati scoperti quasi contemporaneamente da un gruppo di scienziati americani e uno di sovietici
- ^ E. Fermi, The Development of the first chain reaction pile , in Proceedings of the American Philosophical Society , vol. 90, n. 1, 1946, pp. 20–24, JSTOR 3301034 .
- ^ a b Yu.D. Tretyakov (a cura di), Non-organic chemistry in three volumes , Chemistry of transition elements, vol. 3, Moscow, Academy, 2007, ISBN 5-7695-2533-9 .
- ^ a b Greenwood, p. 1263
- ^ a b John Emsley, Nature's Building Blocks: An AZ Guide to the Elements , New, New York, NY, Oxford University Press, 2011, ISBN 978-0-19-960563-7 .
- ^ Peterson, Ivars, Uranium displays rare type of radioactivity , Science News, 7 dicembre 1991.
- ^ Greenwood, p. 1265
- ^ Myasoedov, pp. 30–31
- ^ GG Bartolomei, Baybakov VD, Alkhutov MS, Bach GA, Basic theories and methods of calculation of nuclear reactors , Moscow, Energoatomizdat, 1982.
- ^ Greenwood, pp. 1256–1261
- ^ ( EN ) Smoke Detectors and Americium , su uic.com.au , Nuclear Issues Briefing Paper 35, maggio 2002. URL consultato il 26 agosto 2015 (archiviato dall' url originale il 1º gennaio 1996) .
- ^ Greenwood, p. 1262
- ^ a b Greenwood, p. 1255
- ^ ( RU ) Sergey Popov, Alexander Sergeev, Universal Alchemy , in Vokrug Sveta , vol. 2811, n. 4, 2008.
- ^ ZK Karalova, B. Myasoedov, Actinium , Analytical chemistry items, Moscow, Nauka , 1982.
- ^ ES Palshin, Analytical chemistry of protactinium , Moscow, Nauka, 1968.
- ^ BA Nadykto and LF Timofeeva (a cura di), Plutonium , Fundamental Problems, vol. 1, Sarov, VNIIEF, 2003, ISBN 5-9515-0024-9 .
- ^ MI Ojovan, WE Lee, An Introduction to Nuclear Waste Immobilisation , Amsterdam, Elsevier, 2005, ISBN 0-08-044462-8 .
- ^ BE Burakov, MI Ojovan, WE Lee, Crystalline Materials for Actinide Immobilisation , World Scientific, 2010, ISBN 1-84816-418-1 .
Bibliografia
- ( RU ) AM Golub, Общая и неорганическая химия (Chimica generale e inorganica), 1971.
- ( EN ) Norman N. Greenwood e Alan Earnshaw, Chemistry of the Elements , 2ª ed., Butterworth-Heinemann, 1997, ISBN 0-08-037941-9 .
- ( EN ) B. Myasoedov, Analytical Chemistry of Transplutonium Elements , Mosca, Nauka, 1972, ISBN 0-470-62715-8 .
- R. Bertani, DA Clemente, G. Depaoli, P. Di Bernardo, M. Gleria, B. Longato, U. Mazzi, GA Rizzi, G. Sotgiu e M. Vidali, Chimica Generale ed Inorganica , 3ª ed., CEA, 2010, ISBN 978-88-08-18462-7 .
Voci correlate
Altri progetti
-
 Wikimedia Commons contiene immagini o altri file su attinoidi
Wikimedia Commons contiene immagini o altri file su attinoidi
Collegamenti esterni
- ( EN ) Attinoidi , su Enciclopedia Britannica , Encyclopædia Britannica, Inc.
| Controllo di autorità | Thesaurus BNCF 23907 · LCCN ( EN ) sh85000700 · GND ( DE ) 4141330-1 · BNF ( FR ) cb121509511 (data) · BNE ( ES ) XX530121 (data) · NDL ( EN , JA ) 00560152 |
|---|
![{\ displaystyle \ mathrm {{} _ {~ 92} ^ {238} U + {} _ {0} ^ {1} n \ {\ xrightarrow {\}} \ {} _ {~ 92} ^ {239} U \ {\ xrightarrow [{23,5 \ min}] {\ beta ^ {-}}} \ {} _ {~ 93} ^ {239} Np \ {\ xrightarrow [{2,3 \ days}] { \ beta ^ {-}}} \ {} _ {~ 94} ^ {239} Pu \ {\ xrightarrow [{2,4 \ times 10 ^ {4} \ years}] {\ alpha}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9197c07af11e0332ebcc22d3413806cc7659f65b)






