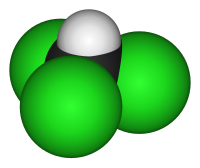
Cloroform
| Cloroform | |
|---|---|
| Numele IUPAC | |
| triclorometan | |
| Denumiri alternative | |
| freon 20 CFC 20 | |
| Caracteristici generale | |
| Formula moleculară sau brută | CHCl3 |
| Masa moleculară ( u ) | 119,38 |
| Aspect | lichid incolor |
| numar CAS | |
| Numărul EINECS | 200-663-8 |
| PubChem | 6212 |
| DrugBank | DB11387 |
| ZÂMBETE | C(Cl)(Cl)Cl |
| Proprietăți fizico-chimice | |
| Densitate (g / cm 3 , în cs ) | 1,47 |
| Solubilitate în apă | 8 g / l la 293 K |
| Temperatură de topire | −63 ° C (210 K) |
| Temperatura de fierbere | 61 ° C (334 K) |
| Δ eb H 0 (kJ mol −1 ) | 31.4 |
| Presiunea de vapori ( Pa ) la 293 K. | 21300 |
| Proprietăți termochimice | |
| Δ f H 0 (kJ mol −1 ) | −134,1 |
| Δ f G 0 (kJ mol −1 ) | −73,7 |
| S 0 m (J K −1 mol −1 ) | 201,7 |
| C 0 p, m (J K −1 mol −1 ) | 114.2 |
| Informații de siguranță | |
| Temperatură de autoaprindere | 982 ° C (1255 K) |
| Simboluri de pericol chimic | |
  | |
| Pericol | |
| Fraze H | 302-315 - 319-331 - 336-351 - 361d - 372 |
| Sfaturi P | 201 - 202 - 260 - 264-270 - 271-280 - 281-301 + 330 + 331-302 + 352-304 + 340-305 + 351 + 338-308 + 313-314 |
Cloroform, IUPAC name triclormetan, este o halogenură de alchil , de asemenea , cunoscut sub numele de freon 20 sau CFC 20. Structura chimică a acesteia molecule este similară cu cea a unei metan molecule în care trei hidrogen atomi au fost înlocuiți cu trei clor atomi.
La temperatura camerei, este transparent lichid , destul de volatil , cu o caracteristică miros . Nu este inflamabil de la sine, dar este într - un amestec cu alți inflamabili compuși .
Acesta este un compus nociv pentru om sănătate și mediu , precum și un suspectat puternic cancerigen .
Cloroform, expuse la lumină și în prezența oxigenului atmosferic, se transforma in mult mai toxice și periculoase fosgen . Din acest motiv se păstrează în chihlimbar și în recipiente bine închise.
Istorie
Cloroform a fost produs pentru prima dată în 1831 de către ambele Justus von Liebig, Eugène SOUBEIRAN și Samuel Guthrie american. Toate trei se obțin din reacția dintre hipoclorit de calciu și acetonă sau etanol , o aplicare a reacției acum cunoscută ca reacția halomorfe , cu toate acestea trei cercetători nu au știut încă structura chimică a compusului și a presupus că au sintetizat dicloretan .
In 1834 chimistul francez Jean-Baptiste Dumas a identificat formula chimică și a dat numele compusului descoperit de cloroform.
In 1847 Edinburgh obstetrician James Young Simpson folosit cloroform pentru anesthetize pacienți în timpul nasterii ; De atunci , utilizarea sa sa extins la o intervenție chirurgicală , în special în Europa . In Statele Unite , aceasta nu a înlocuit eter ca un anestezic până la începutul secolului 20 , însă a fost abandonat în curând o dată efectele sale toxice nedorite au fost cunoscute și tendința sa de a provoca fatale a fost stabilit aritmii cardiace . Atribuit cloroform a fost moartea lui Edwin Bartlett cauzate de soția sa Adelaide, The protagonistul unui celebru proces a avut loc în secolul al 19 - lea din Londra. Pornind de la 1900 de cloroform a fost înlocuit definitiv prin eter în anestezie.
Injecțiile cu cloroform în inima au fost folosite de Josef Mengele sa - l omoare pe gemenii monozigoți pe care le făcea experimentele sale. [1]
Producție
La nivel industrial, cloroform este produs prin încălzirea unui amestec de clor și metan sau clorura de metil , la o temperatură de 400-500 ° C . La această temperatură, substituție radicală reacții au loc care metan transforma în compușii clorurați corespunzători.
-
CH 4 + Cl 2 → CH 3 Cl + HCl -
CH 3 Cl + Cl 2 → CH 2 Cl 2 + HCl -
CH 2 Cl 2 + Cl 2 → CHCl 3 + HCl -
CHCl 3 + Cl 2 → CCl 4 + HCl
Produsul acestei reacții este un amestec din cele patru clormetan (mono-, di-, tri- și tetra-) , care ulterior sunt separate prin distilare .
Utilizări
La rândul său , al XIX - sec și XX, cloroformul a fost folosit ca un anestezic pentru inhalare în chirurgie și în prepararea antitusive siropuri . [2] Astăzi a fost înlocuit cu mai puțin de substanțe toxice . În unele spectacole din seria Ironside, cloroformul este injectat intravenos pentru a obține un efect anestezic temporar; aceasta este, însă, lipsită de orice semnificație.
Utilizarea principală a cloroformul astăzi este producerea de freon R-22 ( de asemenea , numit HCFC -22), [3] utilizat ca agent de răcire fluid, cu toate acestea , freonii asemenea , au fost interzise pe plan internațional , datorită efectului lor distructiv asupra ozonului stratul de sus atmosferă .
Cantități mici de cloroform se utilizează ca solvent în laboratoare - deși tendința este de a se înlocui ori de câte ori este posibil , cu mai puțin periculoase clorură de metilen - și în unele procese industriale.
Reacționează cu clorform de hidroxid de sodiu în soluție apoasă - de preferință , în prezența unui catalizator de transfer de fază - pentru a produce dichlorocarbene in situ; aceasta reacționează rapid cu activat compuși aromatici (cum ar fi fenoli ) care produc arii- corespunzătoare aldehide ( Reimer-Tiemann hidroformilare reacție ). Dichlorocarbene poate reacționa , de asemenea , cu un alchene prin adăugarea la dubla legătură și producând o dicloro substituită ciclopropan .
Deuterat cloroform, CDCI3, în care hidrogenul atom este înlocuit cu un atom de deuteriu, este unul dintre cele mai solvenților comuni utilizați în rezonanță magnetică nucleară spectroscopie (RMN).
Cloroformul este de asemenea utilizat în meserii pentru metacrilat de clei ( Plexiglas ).
Precauții
Inhalarea de cloroform are un efect deprimant asupra centrale nervos sistemului, prin urmare , efectul său anestezic. Respirație în aer ce conține 900 ppm de cloroform rapid produce confuzie, oboseală și dureri de cap. Expunerea prelungită poate provoca leziuni la nivelul ficatului (unde este metabolizat la fosgen ) și la rinichi . In unele persoane, expunerea poate provoca iritații la cutanate și reacții alergice cu febră până la 40 ° C .
Testele pe soareci au aratat ca expunerea in timpul sarcinii aerului care conține 30 la 300 ppm de cloroform sau ingestie poate duce la avorturi spontane sau nașteri ale puilor malformate. La bărbați, o alterare a spermei a fost observată. Efectul cloroformului asupra reproducerii umane este necunoscut.
Suspiciunea de cancerigen sau cancerigen , așa cum este evidențiată în monografiile publicate de Agenția Internațională pentru Cercetarea Cancerului (IARC) [PDF] , probabil asociată cu carcinomul hepatocelular , a fost interzisă în multe țări utilizarea în produse farmaceutice sau auxiliare (paste de dinți, siropuri, unguente ).
Notă
- ^ Josef Mengele: îngerul morții la Auschwitz arhivării 25 iunie 2013 la Internet Archive .
- ^ Din acest motiv, cloroformul face de multe ori un aspect în filme de epocă și romane polițiste, în cazul în care acesta este adesea folosit pentru a bate temporar pe cineva.
- ^(EN) Thermopedia, "Cloroform"
Elemente conexe
Alte proiecte
-
 Wikționar conține dicționarul Lema « cloroform »
Wikționar conține dicționarul Lema « cloroform » -
 Wikimedia Commons conține imagini sau alte fișiere pe cloroform
Wikimedia Commons conține imagini sau alte fișiere pe cloroform
linkuri externe
- Cloroform , pe Sapienza.it, De Agostini .
- (RO) Cloroform , în Enciclopedia Britannica , Encyclopaedia Britannica, Inc.
| Controlul autorității | Thesaurus BNCF 38594 · LCCN (RO) sh85024563 · GND (DE) 4123008-5 · BNF (FR) cb12430403w (data) |
|---|