Dioxid de seleniu
| Dioxid de seleniu | |
|---|---|
| Numele IUPAC | |
| dioxid de seleniu | |
| Denumiri alternative | |
| dioxid de seleniu anhidridă selenioasă | |
| Caracteristici generale | |
| Formula moleculară sau brută | SeO 2 |
| Masa moleculară ( u ) | 110,96 |
| Aspect | alb solid |
| numar CAS | |
| Numărul EINECS | 231-194-7 |
| PubChem | 24007 |
| ZÂMBETE | O=[Se]=O |
| Proprietăți fizico-chimice | |
| Densitate (g / cm 3 , în cs ) | 3.954 g / cm 3 (20 ° C) |
| Solubilitate în apă | 384 g / L (14 ° C) |
| Temperatură de topire | 340 ° C (613 K) sub presiune |
| Temperatura de fierbere | 317 ° C (590 K) sublimează |
| Proprietăți toxicologice | |
| LD 50 (mg / kg) | 68 mg / kg |
| Informații de siguranță | |
| TLV (ppm) | 0,0002 |
| Simboluri de pericol chimic | |
   | |
| Fraze H | 301 - 331 - 373 - 410 |
| Sfaturi P | 261 - 273 - 301 + 310 - 311 - 501 [1] [2] |
Dioxidul de seleniu este un oxid de seleniu cu formula brută SeO 2 și masa moleculară 110,96 uma . Prin urmare, numărul de oxidare al seleniului este +4.
Poate fi format prin arderea seleniului sau seleniurilor :
prin oxidarea seleniului cu acid sulfuric concentrat și fierbinte:
și prin descompunerea trioxidului de seleniu :
Compusul este solubil în solvenți nepolari ( benzen ), în timp ce în apă reacționează pentru a da acid selenios :
De aici și denumirea de anhidridă selenioasă .
Anhidrida reacționează cu alcalii pentru a da anionul selenit:
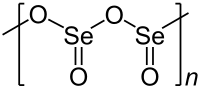
În stare solidă este un polimer al cărui lanț principal este format dintr-o alternanță de atomi de seleniu și oxigen , în stare gazoasă are o structură trimer similară cu cea a dioxidului de sulf . Volatilitatea sa la temperaturi moderat ridicate îl face adecvat pentru a fi separat de nămolul anodic al electrolizei cuprului , de fapt există procese comerciale de producție care utilizează această metodă.
Notă
Bibliografie
- I. Bertini , F. Mani, Chimie anorganică , CEDAM ISBN 88-13-16199-9
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere despre dioxid de seleniu
Wikimedia Commons conține imagini sau alte fișiere despre dioxid de seleniu