Hexafluorură de uraniu
| Hexafluorură de uraniu | |
|---|---|
| Numele IUPAC | |
| hexafluorură de uraniu | |
| Denumiri alternative | |
| HEX | |
| Caracteristici generale | |
| Formula moleculară sau brută | UF 6 |
| Greutatea formulei ( u ) | 352.02 |
| Aspect | solid incolor-gri |
| numar CAS | |
| Numărul EINECS | 232-028-6 |
| PubChem | 24560 |
| ZÂMBETE | F[U](F)(F)(F)(F)F |
| Proprietăți fizico-chimice | |
| Densitate (g / cm 3 , în cs ) | 5.09 |
| Solubilitate în apă | descompunere |
| Temperatură de topire | 64,8 ° C (338 K) la ~ 1,5 atm |
| Temperatura de fierbere | 56,5 ° C (329,7 K), sublimează |
| Presiunea vaporilor ( Pa ) la 298 K. | 16.7 |
| Proprietăți termochimice | |
| Δ f H 0 (kJ mol −1 ) | −2317 |
| S 0 m (J K −1 mol −1 ) | 228 |
| Informații de siguranță | |
| Simboluri de pericol chimic | |
   | |
| Pericol | |
| Fraze H | 330 - 300 - 373 - 411 |
| Sfaturi P | --- [1] |
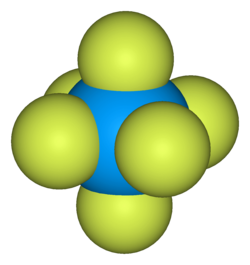
Hexafluorura de uraniu (UF 6 ) este un compus utilizat în procesele de îmbogățire a uraniului pentru producerea combustibilului nuclear și a armelor nucleare. La temperatura camerei apare ca un solid cristalin incolor până la gri (se evaporă la 20 ° C); este foarte toxic și reacționează violent cu apa , efectuând, de asemenea, o acțiune corozivă asupra multor metale.
Se obține din minereu de uraniu bogat în U 3 O 8 prin dizolvare în acid azotic pentru a da azotat de uranil UO 2 (NO 3 ) 2 . Acesta este purificat prin extracție cu solvent organic și tratat cu amoniac pentru a da diuranat de amoniu . Prin reducerea cu hidrogen, acesta este transformat în dioxid de uraniu UO 2 , ulterior transformat în tetrafluorură de uraniu UF 4 și în cele din urmă oxidat în hexafluorură de uraniu prin reacție cu fluor .
Molecula sa are geometrie octaedrică , atomul de uraniu este înconjurat de șase atomi de fluor. Din punct de vedere chimic este un acid și oxidant Lewis , capabil să formeze complexe cu alte fluoruri.
Aplicații în ciclul combustibilului nuclear
Molecula UF 6 este utilizată în ambele metode majore utilizate pentru îmbogățirea uraniului , difuzia gazului și metoda centrifugii de gaze , deoarece are un punct triplu la 64,05 ° C (147 ° F, 337 Kelvin) la o presiune ușor peste presiunea atmosferică normală. Fluorul are un singur izotop stabil în natură, prin urmare izotopologii UF 6 diferă în greutatea lor moleculară, în funcție doar de greutatea atomică a izotopului de uraniu prezent în moleculă . [2]
Toate celelalte fluoruri de uraniu sunt solide nevolatile, care sunt diferite tipuri de polimeri de coordonare .
În industria nucleară, procesul de difuzie gazoasă necesită aproximativ 60 de ori mai multă energie decât procesul de centrifugare cu gaz; chiar și așa, aceasta este doar 4% din energia care poate fi produsă din uraniul îmbogățit care se obține.
 Diagrama de fază a UF 6 . |
Pe lângă utilizarea sa în îmbogățire (creșterea concentrației unui anumit histop de uraniu), hexafluorura de uraniu a fost utilizată în metoda avansată de reprocesare a combustibilului nuclear ( volatilitatea fluorurii ) care a fost dezvoltată în Republica Cehă . În acest proces, utilizat în oxidul de combustibil nuclear , acesta este amestecat cu fluor fluor pentru a forma un amestec de fluoruri. Acesta este apoi distilat pentru a separa diferitele clase de materiale.
Depozitare în butelii care conțin DUF gazos 6
Aproximativ 95% din uraniul sărăcit produs până în prezent este stocat sub formă de hexafluorură de uraniu sărăcit, DUF 6 , în butelii de oțel în spații deschise în apropierea centralelor de îmbogățire. Fiecare cilindru conține aproximativ 12,7 tone (14 tone SUA) de UF 6 solid. Numai în SUA există 560.000 de tone de UF 6 epuizate, care au fost numărate cu precizie în 1993 . În 2005, 686.500 de tone conținute în 57.122 cilindri de depozitare au fost localizate lângă Portsmouth ( Ohio ), Oak Ridge ( Tennessee ) și Paducah ( Kentucky ). [3] [4] Necesitatea menținerii stocării pe termen lung a DUF 6 prezintă riscuri de mediu, sănătate și siguranță generală, datorită instabilității sale chimice.
Când UF 6 este expus la aerul umed, acesta reacționează cu apa atmosferică pentru a produce UO 2 F 2 ( fluorură de uranil ) și HF ( fluorură de hidrogen ), care au caracteristica comună de a fi toxice și extrem de solubile.în apă (și lichide biologice) . Cilindrii de depozitare trebuie inspectați periodic pentru a detecta semne de coroziune și scurgeri. Timpul mediu de rezistență al cilindrilor de oțel care conțin hexafluorură de uraniu a fost estimat în decenii, în timp ce timpul de înjumătățire al diferiților izotopi de uraniu este de peste zeci de mii de ani. [5]
Accidente cu hexafluorură de uraniu
Au existat mai multe incidente care implică hexafluorură de uraniu în Statele Unite . [6] [7] Guvernul SUA a transformat cantitățile de DUF 6 în oxid de uraniu solid pentru eliminare. [8] Eliminarea DUF 6 în coșurile din Statele Unite ar putea costa între 15 și 450 de milioane de dolari . [9]
Notă
- ^ Fișă informativă despre hexafluorură de uraniu pe IFA-GESTIS Arhivat 16 octombrie 2019 la Arhiva Internet .
- ^ Uranium Enrichment and the Gaseous Diffusion Process , pe usec.com , USEC Inc. Accesat la 24 septembrie 2007 (arhivat din original la 19 octombrie 2007) .
- ^ Cât de mult hexafluorură de uraniu sărăcit este stocată în Statele Unite? , în Întrebări frecvente despre UF 6 epuizate , Laboratorul Național Argonne .
- ^ Documente , la web.ead.anl.gov . Adus la 14 iulie 2010 (arhivat din original la 16 februarie 2008) .
- ^ Ce este DUF 6 ? Este periculos și ce ar trebui să facem cu el? , la ieer.org , Institute for Energy and Environmental Research, 24 septembrie 2007.
- ^ Au existat accidente care implică hexafluorură de uraniu? , în Întrebări frecvente despre UF 6 epuizate , Laboratorul Național Argonne . Adus la 14 iulie 2010 (arhivat din original la 6 martie 2008) .
- ^ Uranium Hexafluoride (UF 6 ) steril: Caracteristici, transport și depozitare la Siberian Chemical Combine (Sibkhimkombinat) Tomsk ( PDF ), pe largeassociates.com , Large and Associates, 5 noiembrie 2005. Accesat 24 septembrie 2007 (arhivat de original url la 27 septembrie 2007) .
- ^ Ce se va întâmpla cu hexafluorura de uraniu stocată în Statele Unite? , în Întrebări frecvente despre UF 6 epuizate , Laboratorul Național Argonne .
- ^ Există instalații de eliminare care funcționează în prezent și care pot accepta tot oxidul de uraniu epuizat care ar fi generat din conversia inventarului UF6 epuizat al DOE? , în Întrebări frecvente despre UF 6 epuizate , Laboratorul Național Argonne .
Elemente conexe
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere pe hexafluorură de uraniu
Wikimedia Commons conține imagini sau alte fișiere pe hexafluorură de uraniu
linkuri externe
- ( EN ) JH Levy, John C. Taylor, Paul W. Wilson, Structura fluorurilor. Partea a XII-a. Studiu de difracție cu neutron cu un singur cristal al hexafluorurii de uraniu la 293 K , în J. Chem. Soc. Dalton Trans. , 1976, pp. 219–224, DOI : 10.1039 / DT9760000219 .
- ( EN ) Brevet SUA 2535572: Prepararea UF 6 ; 26. decembrie 1950.
- ( EN ) Brevet SUA 5723837: Purificare cu hexafluorură de uraniu ; 3. martie 1998.
- (EN) Simon Cotton (Uppingham School, Rutland, Marea Britanie): Hexafluorură de uraniu .
- ( EN ) Importul hexafluorurii de uraniu sărăcit occidental (cozi de uraniu) în Rusia , pe ecoperestroika.ru .