Hexafluorură de sulf
| Hexafluorură de sulf | |
|---|---|
| Caracteristici generale | |
| Formula moleculară sau brută | SF 6 |
| Masa moleculară ( u ) | 146,06 g / mol |
| Aspect | gaz incolor și inodor |
| numar CAS | |
| Numărul EINECS | 219-854-2 |
| PubChem | 17358 |
| DrugBank | DB11104 |
| ZÂMBETE | FS(F)(F)(F)(F)F |
| Proprietăți fizico-chimice | |
| Densitate (g / cm 3 , în cs ) | 1.329 |
| Densitate (kg m −3 , în cs ) | 6.164 g / L la 1 bar (~ 5.1 ori mai dens decât aerul) |
| Solubilitate în apă | Scăzut |
| Temperatură de topire | -64 ° C (209 K) (sublimează); se descompune la 773 K (500 ° C) |
| Temperatura de fierbere | Sublim în condiții normale |
| Informații de siguranță | |
| Simboluri de pericol chimic | |
 | |
| Atenţie | |
| Fraze H | 280 |
| Sfaturi P | 410 + 403 [1] |
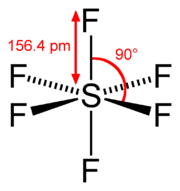
Hexafluorura de sulf este un compus anorganic cu formula SF 6 . Este un gaz transparent, inodor, netoxic și neinflamabil (în condiții standard); la 1 bar are o densitate de 6.164 g / L (este de aproximativ 5.1 ori mai densă decât aerul). Are o geometrie octaedrică , formată din șase atomi de fluor legați de un atom central de sulf . Este o moleculă hipervalentă . Este ușor solubil în apă, dar solubil în solvenți organici nepolari. În general, este transportat sub formă lichefiată.
Sinteza și reacțiile
SF 6 poate fi preparat din elemente prin expunerea S 8 (solid) la F 2 (gaz). Aceasta este metoda descoperită și utilizată de Henri Moissan și Paul Lebeau în 1901. În timpul sintezei se formează alte fluoruri care sunt eliminate prin căldură și spălarea produsului cu NaOH.
SF 6 este un gaz inert și practic nu este utilizat în reacțiile de sinteză ale altor produse.
Aplicații
- ca gaz de urmărire în experimente pentru a verifica ventilația, scurgerile sau infiltrațiile în clădiri; se folosește și în hidrogeologie ;
- în metalurgie pentru producția de aluminiu și magneziu ;
- la fabricarea semiconductoarelor datorită caracterului său inert și densității mari (aerul și poluanții mai ușori sunt astfel eliminați);
- este utilizat în acceleratoarele de particule (tendință scăzută de ionizare);
- este utilizat ca mijloc de stingere a arcului electric în întrerupătoarele MT și HV datorită rezistenței sale dielectrice ridicate (89 kV / cm) care crește odată cu presiunea [2] ;
- este folosit ca dielectric în stațiile și stațiile electrice și blindate [3] ;
- în domeniul medical pentru dezinfectarea dispozitivelor respiratorii împotriva microbilor aerobi și ca mediu de contrast în ultrasunete (sub formă de microbule injectabile);
- la fabricarea de celule fotovoltaice inovatoare numite siliciu negru ;
- în construcție, în interiorul unităților de sticlă izolatoare (termopan), pentru a îmbunătăți performanța de izolare acustică a acestora.
- în contextul propulsiei torpilelor, este utilizat în sistemul modern de propulsie SCEPS (Stored Chemical Energy Propulsion System). În acest sistem, care funcționează prin ciclul Rankine, fuziunea unei mase de litiu în stare solidă are loc în interiorul unui cazan. O anumită cantitate de hexafluorură de sulf este apoi injectată în litiul topit, ceea ce dă naștere unei reacții exoterme puternic controlate care permite apei prezente în bobinele cazanului să se evapore și să alimenteze o turbină mică. Acesta din urmă acționează elicele clasice anti-rotative ale sistemului de propulsie torpilă, permițându-i să avanseze.
Având în vedere densitatea sa ridicată, hexafluorura de sulf este utilizată ca un truc magic pentru a simula prezența „apei invizibile” pe care să plutească obiecte ușoare (cum ar fi o barcă de aluminiu).
Hexafluorura de sulf modifică vocea: inhalarea unei cantități mici de ea produce un ton mai profund, efectul opus celui obținut prin inhalarea heliului care, fiind mai puțin dens decât aerul, determină o creștere a tonului.
Aspecte de mediu
SF 6 este un gaz cu efect de seră , adică unul dintre gazele care contribuie la creșterea efectului de seră și este de 24000 de ori mai periculos pentru mediu decât dioxidul de carbon . [4]
Notă
- ^ Sigma Aldrich; rev. din 05.12.2012
- ^ Gaetano Conte, Tehnologii și proiectarea sistemelor electrice și electronice , HOEPLI.
- ^ Gaetano Conte, Tehnologii și proiectarea sistemelor electrice și electronice , Milano, HOEPLI.
- ^ Nouă cameră cu infraroșu. , în La Chimica & l'Industria , n. 9, Italian Chemical Society, noiembrie 2009, p. 67.
Bibliografie
- E. Quaia, Medii de contrast în ultrasunete: aplicații abdominale , Springer, 2007, ISBN 978-88-470-0616-4 .
Elemente conexe
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere despre hexafluorură de sulf
Wikimedia Commons conține imagini sau alte fișiere despre hexafluorură de sulf
linkuri externe
- Un obiect ușor plutește pe hexafluorură de sulf (video) , pe youtube.com .
- Experimente de voce amuzante (video) , pe youtube.com .
| Controlul autorității | LCCN (EN) sh85130381 · GND (DE) 4180408-9 |
|---|