Străin
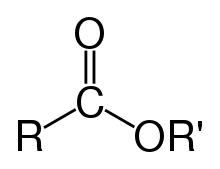
Esterii sunt compuși organici produși prin reacția unui alcool sau a unui fenol cu un acid carboxilic sau derivatul acestuia, numit „ esterificare ”. Acest termen a fost introdus de chimistul Leopold Gmelin (1788-1853). [1]
Produsele acilării alcoolilor cu alți acizi anorganici se mai numesc esteri , care dau naștere familiei esterilor anorganici , care au proprietăți chimice foarte asemănătoare cu esterii organici, dar a căror structură caracteristică este ușor diferită de aceasta. Nomenclatura esterilor urmează cea a sărurilor acizilor care reacționează, deci vom avea, de exemplu:
- CH 3 COOC 2 H 5 acetat de etil ;
- C 15 H 31 COOCH 3 palmitat de metil ;
Esterii cu greutate moleculară mică au un miros plăcut, fructat; celelalte sunt inodore. Esterii naturali cu greutate moleculară mare sunt grăsimile și cerurile , care sunt alcătuite din grăsimi superioare și alcooli monovalenți cu lanț lung.
Sinteză
- Esterificare Fischer:
OH SAU ' | -> | RC = O + H + + R'OH <- RC = O + H 2 O + H +
Este o reacție de echilibru, prin urmare, pentru a îmbunătăți cantitatea de produs obținută, alcoolul este utilizat direct ca solvent , astfel încât să fie în exces și să împingă reacția spre produse. Aceasta implică faptul că alcoolul este compus, cel mult, din trei atomi de carbon, altfel nu mai poate dizolva acidul carboxilic .
- Obținerea din cloruri de acil :
Cl SAU ' | | RC = O + R'OH -> RC = O + HCl
Reacția se desfășoară în piridină , care îndeplinește trei sarcini: acționează ca solvent, neutralizează acidul clorhidric care se formează și dizolvă clorura de acil ca un complex activat, adică facilitează formarea produsului.
- Extracția din anhidride :
RC = O | O SAU 'OH | | | RC = O + R'OH -> RC = O + RC = O
De asemenea, în acest caz, reacția se efectuează în piridină din motivele menționate mai sus; singura diferență este că acidul acetic se formează în locul acidului clorhidric.
- Obținerea cu diazometan :
Este o reacție cu randamente foarte mari, care se efectuează de obicei într-o soluție eterică; are însă neajunsurile de a constitui o sinteză numai pentru esteri metilici și de a trata un compus extrem de periculos.
Are loc în două etape:
- 1. Transferul unui proton din grupa carboxil în diazometan:
- 2. Reacția lui S n 2, în care anionul carboxilat este nucleofil, iar azotul este excelentul grup de părăsire :
Reacții tipice
Reacțiile chimice tipice ale esterilor sunt toate substituții nucleofile și tocmai acestea sunt hidroliza acidă sau retro-Fisher, hidroliza sau saponificarea bazică, alcooliza și ammonoliza .
- Hidroliza acidă (retro-Fisher):
Practic este aceeași reacție de formare a esterului, cu toate acestea efectuată cu un pH ușor acid. Prin încălzirea esterului cu acizi minerali diluați, legătura dublă C = O este protonată și se rupe, permițând unei molecule de apă să reacționeze cu esterul și reformând alcoolul original și acidul cu un proton suplimentar, care este evacuat rapid.
- Hidroliza de bază ( saponificare ):
Dacă, în locul unui acid diluat, esterul reacționează cu o bază puternică și concentrată, acesta se combină complet și definitiv cu acidul și esterul dispare din soluție, dând loc sării acidului și a alcoolului de pornire, care dat fiind pH-ul de bază al soluției nu se mai poate combina. Această reacție se mai numește și saponificare deoarece, dacă acidul în cauză este un derivat carboxilic cu lanț lung (acizi grași superiori), compusul rezultat este tocmai săpunul utilizat în mod obișnuit.
- Alcooliză sau transesterificare:
În această reacție alcoolul original al esterului este înlocuit (deplasat) de altul, care își ia locul: este o reacție de echilibru foarte asemănătoare cu hidroliza acidă, favorizată de un pH acid și apare în număr mare de reacții biochimice. Formula generală a reacției este:
Ca și în hidroliza acidă, procesul începe cu protonarea legăturii C = O a esterului, dar în loc de apă este al doilea alcool prezent în soluție care reacționează. Întrucât sunt favorizate de același mediu, reacția de alcooliză are loc în concurență cu cea de hidroliză acidă: prin urmare, pentru a avea un randament suficient este necesar să se utilizeze o concentrație foarte mare de alcool care trebuie înlocuit.
- Amonoliză:
În această reacție, amoniacul este utilizat pentru a sparge legătura C = O a esterului, obținând un alcool și o amidă .
Formula generală a reacției este:
unde R'-OH este alcoolul și R-CONH 2 este amida.
Clase de esteri
Din punct de vedere biologic, esterii pot fi împărțiți în trei clase în funcție de lungimea lanțului de atomi de carbon și tipul de alcool și acid.
- Esteri de fructe:
- Sunt cei mai mici esteri, în care atât acidul, cât și alcoolul au un lanț de mai puțin de 10 atomi de carbon; sunt foarte frecvente în esențele naturale și artificiale de fructe. De exemplu:
- CH 3 COOC 2 H 5 acetat de etil (pere, mere, coacăze și fructe de pădure).
- CH 3 COOC 5 H 11 acetat de n-amil (banană, ananas, pere).
- C 4 H 9 COOC 2 H 5 izovalerianat de etil (piersică, valeriană).
- Ceară:
- În ceruri, lanțurile de carbon, atât în acid, cât și în alcool, sunt mai lungi de 10 atomi (uneori mai mult de 30): uneori sunt de lungime egală. Unii clasifică cerurile în grupul lipidelor simple, împreună cu uleiurile și grăsimile naturale.
- C 15 H 31 COOC 16 H 33 cetil palmitat (în alb de balenă sau spermaceti ).
- C 15 H 31 COOC 30 H 61 miricil palmitat ( ceară de albine ).
- Gliceride:
- Sunt, fără îndoială, cea mai importantă clasă de esteri din punct de vedere biologic. Alcoolul este întotdeauna același, glicerolul (numit și 1,2,3-propantriol sau propantriol), un alcool trivalent. Acizii care reacționează cu glicerolul sunt cu lanț lung (de la 12 la 20 de atomi de carbon la om), mononesaturați sau polinesaturați și monocarboxilici, adică cu o singură grupă de acid carboxilic. Deci, puteți avea esteri monogliceridici , digliceride sau trigliceride, în funcție de câte grupări hidroxil ale glicerinei sunt înlocuite (una, două sau toate trei). Cele mai cunoscute componente ale gliceridelor sunt acidul palmitic , acidul stearic și acidul oleic .
- Monogliceridele și digliceridele pot fi optic active dacă moleculele lor sunt asimetrice; 1,2-digliceridele sunt interesante din punct de vedere biologic, deoarece sunt precursori chimici ai trigliceridelor și fosfolipidelor . Dar de departe cele mai importante sunt trigliceridele , care constituie cel mai mare grup de lipide simple, adică acele substanțe care nu sunt solubile în apă, dar solubile în solvenți nepolari .
Notă
Alte proiecte
-
 Wikționarul conține dicționarul lema « ester »
Wikționarul conține dicționarul lema « ester » -
 Wikimedia Commons conține imagini străine sau alte fișiere
Wikimedia Commons conține imagini străine sau alte fișiere
linkuri externe
- ( RO ) IUPAC Gold Book, „esteri” , pe goldbook.iupac.org .
- Experiențe de laborator - Esterii , pe itchiavari.org .
| Controlul autorității | Thesaurus BNCF 23190 · LCCN (EN) sh85044949 · GND (DE) 4153062-7 · BNF (FR) cb11970080s (dată) · NDL (EN, JA) 00.56205 milioane |
|---|




