Glucoză
| Glucoză | |||
|---|---|---|---|
| Numele IUPAC | |||
| 2 (R), 3 (S), 4 (R), 5 (R), 6-pentahidroxihexanal | |||
| Denumiri alternative | |||
| dextroză (forma D ) D - (+) - glucopiranoză. | |||
| Caracteristici generale | |||
| Formula moleculară sau brută | C 6 H 12 O 6 | ||
| Masa moleculară ( u ) | 180.1572 | ||
| Aspect | solid cristalin alb | ||
| numar CAS | Numărul CAS nu este valid | ||
| Numărul EINECS | 200-075-1 | ||
| Proprietăți fizico-chimice | |||
| Puterea rotativă specifică | 52,7 ° | ||
| Solubilitate în apă | 909 g / L la 25 ° C [1] | ||
| Temperatură de topire | ~ 146 ° C (~ 419 K) | ||
| Proprietăți termochimice | |||
| Δ f H 0 (kJ mol −1 ) | −1273,3 | ||
| Informații de siguranță | |||
| Fraze H | - | ||
| Sfaturi P | - [2] | ||
Glucoza , cunoscută și sub numele de glicoză sau dextroză (limitată la enantiomerul dextrorotator), este o monozaharidă aldehidică ; este cel mai răspândit compus organic în natură, atât liber, cât și sub formă de polimeri .
Caracteristici
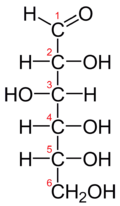
Are formula CH2OH (CHOH) 4 CHO [(C 6 H 12 O 6)], și diferă de galactoză prin configurația sa la C 4.
Este o moleculă chirală , deci există doi enantiomeri:
- enantiomerul dextrorotator ( D- glucoză sau dextroză) este cel mai răspândit în natură, prezent în stare liberă în numeroase fructe zaharoase; se găsește și în majoritatea fluidelor corporale, în ficat , sânge și splină
- enantiomerul stângaci ( L- glucoză).
Este unul dintre cele mai importante zaharuri și este utilizat ca sursă de energie atât de animale, cât și de plante. Glucoza este principalul produs al fotosintezei și este combustibilul respirației .
Se dizolvă bine în apă (909 g / L la 25 ° C) [1] și puțin în etanol . O soluție de 100 g / L în apă la 20 ° C are un pH de aproximativ 7.
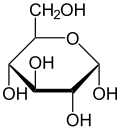
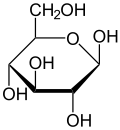
Glucoza este o aldohexoză de zahăr deoarece molecula sa este compusă din șase atomi de carbon (-esoso) și conține un grup carbonil aldehidă -CHO tipică aldehidelor (aldo-). Cea mai stabilă formă a sa este aceea în care una dintre grupările hidroxil se leagă de carbonul C1 al grupării aldehide (-CHO) pentru a forma un inel cu 6 atomi, un inel piranoză , a cărui structură este prezentată în figură. Reacția de formare a inelului este reversibilă; la pH 7 aproximativ 0,0026% din molecule sunt prezente în formă deschisă.
Glucoza este o sursă de energie omniprezentă în biologie . Motivul pentru care aceasta este și nu o altă monozaharidă, cum ar fi fructoza , face încă obiectul speculațiilor. În absența formelor de viață care o sintetizează, glucoza poate fi formată chimic din formaldehidă , deci este probabil ca aceasta să fie prezentă și bine disponibilă atunci când s-au născut primele sisteme biochimice primitive. O altă proprietate, poate mai importantă pentru formele de viață superioare, este tendința redusă (în comparație cu alte zaharuri de hexoză) de a reacționa cu grupările amino ale proteinelor . Această reacție (numită glicare sau non-enzimatic de glicozilare ) reduce sau anulează activitatea multor enzime și este responsabil pentru mai multe efecte pe termen lung ale diabetului , cum ar fi orbire si redusa rinichi functia. Reactivitatea scăzută a glucozei la glicozilare se datorează prevalenței sale rămase în forma ciclică, mai puțin reactivă.
În respirație, printr-o serie de reacții catalizate de enzime, glucoza este oxidată pentru a forma dioxid de carbon și apă ; energia produsă de această reacție este utilizată pentru a produce molecule de ATP .
O moleculă de glucoză și una de fructoză unite printr-o legătură glicozidică formează o moleculă de zaharoză , zahărul obișnuit de masă. Amidonul , celuloza și glicogenul sunt polimeri ai glucozei și sunt în general clasificați drept polizaharide .
Denumirea dextroză se datorează faptului că o soluție de D- glucoză rotește planul luminii polarizate spre dreapta (adică în sensul acelor de ceasornic).
Izomerism
Molecula de glucoză este chirală ; există, prin urmare, doi enantiomeri, unul specular de celălalt, D- glucoză și L- glucoză. Dintre cele două, numai primul ( D ) este cel folosit și produs de organismele vii.
Când molecula de glucoză se închide în buclă, o poate face în două moduri diferite; grupul -OH legat de atomul de carbon imediat după cel al oxigenului prin deplasarea inelului în sensul acelor de ceasornic poate, de fapt, să indice în jos sau în sus în raport cu planul mediu al moleculei, în primul caz vorbim de forma α, în al doilea din forma β. În soluție apoasă, cele două forme sunt transformate una în cealaltă ( mutarotație ) și în câteva ore proporțiile se stabilizează pe raportul α: β 36:64.
Pentru a stabili dacă un carbohidrat aparține seriei D sau seriei L , este necesar să se ia în considerare forma deschisă a moleculei și să se compare dispunerea substituenților din jurul penultimului atom de carbon cu dispunerea substituenților în jurul celui de-al doilea atom de carbon al D - gliceraldehidă . Glucidul este D dacă are penultimul carbon cu grupa alcoolică în dreapta, L dacă în stânga.
Sinteză
În sistemele vii
- este produsul fotosintezei clorofilei la plante și la unele procariote ;
- este produs în ficat prin descompunerea depozitelor de glicogen ;
- este produs în ficat și în glanda suprarenală gastrică printr-un proces cunoscut sub numele de gluconeogeneză .
Rolul în metabolism
Glucoza este principala sursă de energie pentru organismele vii, dar toți ceilalți carbohidrați joacă, de asemenea, un rol foarte important. Arderea glucozei prin respirație (oxidare aerobă) asigură până la 285 kilocalorii pe mol [3] (aproximativ 4 kilocalorii pe gram ).
Capacitatea ficatului de a stoca glucoza este destul de limitată (70-100 g) și orice exces de carbohidrați (în comparație cu necesitățile calorice) este transformat în grăsime și depus în țesutul adipos.
Prin glicoliză , glucoza este imediat implicată în producția de adenozin trifosfat ( ATP ), care este purtătorul de energie al celulelor. Este, de asemenea, un compus critic în sinteza proteinelor și în metabolismul lipidelor . Mai mult, deoarece celulele sistemului nervos nu sunt capabile să metabolizeze lipidele, glucoza este principala lor sursă de energie.
Glucoza este absorbită în sânge prin pereții intestinali . O parte din aceasta este direcționată direct către celulele creierului , în timp ce restul se acumulează în țesuturile ficatului și mușchii într-o formă polimerică asemănătoare amidonului , glicogenului . Aceasta din urmă este o sursă de energie auxiliară pentru corp și acționează ca o rezervă care se consumă atunci când este nevoie.
Tocmai absorbția rapidă a glucozei îl face unul dintre zaharurile simple cu cel mai mare indice glicemic , atât de mult încât este utilizat la nivel internațional ca unitate de măsură a acestui indice și stabilit la 100.
Fructoza și galactoza , alte zaharuri care se formează în urma descompunerii carbohidraților, sunt direcționate către ficat, unde sunt la rândul lor transformate în glucoză. Această cale mai lungă le face să fie zaharuri mai potrivite pentru utilizare îndelungată în timp, deoarece indicele lor glicemic este mai mic, dar eficacitatea lor este mai durabilă, datorită eliberării lente sub formă de glucoză de către ficat.
Transport transepitelial al glucozei
Asimilarea glucozei în intestin necesită intervenția diferiților transportori de glucoză , care sunt proteine membranare integrale care mediază trecerea moleculelor de monozaharide dintr-o parte a epiteliului în alta. Modelul care descrie acest proces ia în considerare trei transportoare numite SGLUT1 , Na + / K + ATPaza ( pompă de sodiu-potasiu ) și GLUT2 .
Sodiul pătrunde în celulele epiteliale printr-un SimPort Glucoză de sodiu, SGLUT1, datorită unui gradient de concentrație favorabil care trage glucoza. Diferența de concentrație este menținută datorită pompei de sodiu / potasiu care elimină constant ioni Na + din celulă. Glucoza poate ajunge apoi în sânge prin GLUT2 fără a fi nevoie de energie suplimentară, deoarece se deplasează în funcție de gradient.
Notă
- ^ a b Sigma-Aldrich, fișa cu informații despre produs de D - (+) - glucoză
- ^ Foaie informativă D-glucoză pe IFA-GESTIS Arhivat 16 octombrie 2019 la Arhiva Internet .
- ^ Noris Siliprandi; Guido Tettamanti, Biochimie medicală , Piccin, 2013.
Elemente conexe
- ATP
- Ciclul Calvin
- Ciclul Krebs
- Diabet
- Îndulcitor
- NADH
- Galactoza
- Glicoliza
- Fructoză
- Fotosinteză
- Monozaharidă
- Țesuturi dependente de glucoză
Alte proiecte
-
 Wikicitată conține citate despre glucoză
Wikicitată conține citate despre glucoză -
 Wikționarul conține dicționarul lema « glucoză »
Wikționarul conține dicționarul lema « glucoză » -
 Wikimedia Commons conține imagini sau alte fișiere despre glucoză
Wikimedia Commons conține imagini sau alte fișiere despre glucoză
linkuri externe
- Glucosio , pe Treccani.it - Enciclopedii online , Institutul Enciclopediei Italiene .
- ( EN ) Glucoză , în Encyclopedia Britannica , Encyclopædia Britannica, Inc.
- ( EN ) Aflați mai multe despre chimia și biochimia glucozei, pe EvoWiki , la evowiki.org . Adus la 12 decembrie 2004 (arhivat din original la 15 decembrie 2004) .
- Glucosio , în Treccani.it - Enciclopedii on-line , Institutul Enciclopediei Italiene.
| Controlul autorității | Tezaur BNCF 15559 · LCCN (EN) sh85055360 · NDL (EN, JA) 00.560.931 |
|---|