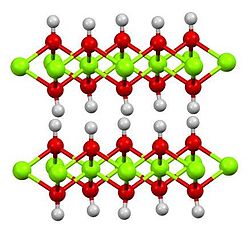
Hidroxid feros
| Hidroxid feros | |
|---|---|
| Numele IUPAC | |
| Dihidroxid de fier | |
| Denumiri alternative | |
| Hidroxid feros Hidroxid de fier (II) | |
| Caracteristici generale | |
| Formula moleculară sau brută | Fe (OH) 2 |
| Masa moleculară ( u ) | 89,86 |
| Aspect | Verde închis solid |
| numar CAS | |
| Numărul EINECS | 242-456-5 |
| PubChem | 10129897 |
| ZÂMBETE | [OH-].[OH-].[Fe+2] |
| Proprietăți fizico-chimice | |
| Densitate (g / cm 3 , în cs ) | 3,4 g / cm 3 |
| Solubilitate în apă | 0,00143 g / l (20 ° C) |
| Constanta de solubilitate la 298 K. | 1,64 × 10 −14 [1] 8 × 10 −16 [2] |
| Proprietăți termochimice | |
| Δ f H 0 (kJ mol −1 ) | −574 KJ / mol |
| S 0 m (J K −1 mol −1 ) | 92 J / (K mol) |
| Informații de siguranță | |
Hidroxidul de fier sau hidroxidul de fier (II) este un compus chimic ignifug, netoxic, lipsit de gust (lipire), inițial de culoare albă care își schimbă culoarea în verde închis sau verde-negru în maro pe măsură ce se oxidează în aer.
Mai precis, este hidroxidul în care fierul ia o stare de oxidare +2.
Sinteză
Dublu schimb
Poate fi obținut prin reacția unui compus care conține ionul hidroxil cu altul care conține ionul Fe 2+ , cum ar fi hidroxid de sodiu și clorură de fier : [3]
- 2NaOH (aq) + FeCl 2 (aq) → 2NaCl (aq) + Fe (OH) 2 ↓
sodă caustică și sulfat feros :
- 2NaOH + FeSO 4 → Fe (OH) 2 + Na2 SO4
sau hidroxid de potasiu și sulfat feros:
- 2KOH + FeSO 4 → Fe (OH) 2 + K 2 SO 4
Sinteza electrolitelor
Hidroxidul de fier poate fi obținut prin electroliza unei soluții de clorură de sodiu în apă folosind electrozi de fier.
Ionii Cl - și Na + migrează către electrozi, transformându-se în Cl gazos și Na metalic.
- Na + (aq) Cl - (aq) Na (aq) + Cl (aq)
În acest moment, sodiul dezvoltat la anod se va lega de soluția de apă pentru a forma hidroxid de sodiu și hidrogen :
- Na + H2O → NaOH (aq) + 2 ↑ ^ H
În timp ce clorul se va lega de fierul electrodului formând clorură feroasă:
- 2 Cl (aq) + Fe (s) → + FeCl 2 (aq)
Ultimul compus, intrând în contact cu hidroxidul de sodiu al catodului, se combină pentru a genera clorură de sodiu și hidroxid feros:
- 2 NaOH (aq) + FeCl 2 (aq) → Fe (OH) 2 ↓ + 2 NaCl (aq)
Electroliza poate continua prin divizarea clorurii de sodiu obținută din nou, până când apa soluției sau electrozii sunt epuizați.
Pe măsură ce reacția continuă, veți observa că precipitatul se întunecă încet de la verde la maro închis.
Purificare
Substanța obținută din hidroxid de sodiu este purificată prin spălări multiple în care se adaugă apă la soluție, hidroxidul de fier (II) este lăsat să se stabilească și apa de suprafață este aspirată și apoi procedura se repetă de mai multe ori.
depozitare
După purificare, hidroxidul feros poate fi depozitat într-un congelator obișnuit, fără a-l separa neapărat de apa în care este conținut.
Degradare
Dacă este expus la apă, lumină și în special aer , (în prezența oxigenului ) se degradează în substanțe secundare, cum ar fi hidroxidul feric . Pentru a-și păstra caracteristicile, este suficient să mențineți compusul la temperaturi scăzute și să nu fie expus direct la aer.
Utilizări
Hidroxidul de fier este utilizat pentru purificarea apei din compuși de seleniu . [4]
Microbiologie
Bacteriile ferofixante oxidează cationul Fe ++ al hidroxidului feros cu oxigenul prezent în apa în care trăiesc pentru energie.
- 4Fe (OH) 2 + 2H 2 O + O 2 → 4Fe (OH) 3 + căldură
Conversia la magnetit
Printr-un proces chimic numit reacția Schikorr , hidroxidul feros este transformat în magnetit cu eliberarea de apă și hidrogen gazos:
- 3Fe (OH) 2 → Fe 3 O 4 + H 2 O + H 2 ↑
Notă
- ^ Chimie generală a lui Pauling - Vezi și Constanta de solubilitate .
- ^ Copie arhivată , la bilbo.chm.uri.edu . Adus la 23 februarie 2015 (arhivat din original la 26 februarie 2015) . - Vezi și intrarea Constanta de solubilitate .
- ^ http://online.scuola.zanichelli.it/chimicafacile/files/2011/03/Formazione-idrossidi.pdf
- ^ https://www.sciencedirect.com/science/article/pii/S0160412097000329