Introducere în viruși
Această intrare este o prezentare nespecializată a subiectului. Informații mai detaliate în intrarea principală.
Un virus este un mic agent infecțios care se reproduce în interiorul celulelor gazdelor vii. Când este infectată, celula gazdă este forțată să producă rapid mii de copii identice ale virusului original. Spre deosebire de majoritatea ființelor vii, virușii nu au celule care se divid; noii viruși se adună în celula gazdă infectată. Dar, spre deosebire de agenții infecțioși mai simpli, cum ar fi prionii , aceștia conțin gene care le permit să mute și să evolueze. Au fost descoperite peste 4 800 de specii de virus. [1] Originea lor este neclară: unele s-ar putea să fi evoluat din plasmide - bucăți de ADN care se pot deplasa între celule - în timp ce altele s-ar putea să fi evoluat din bacterii .
Virușii constau din două sau trei părți. Toate conțin gene, instrucțiunile celulelor, realizate din ADN sau ARN , molecule lungi cu multe gene. Toți virușii sunt, de asemenea, acoperiți într-o manta proteică pentru a proteja genele. Unii viruși pot avea, de asemenea, un plic de grăsime care acoperă stratul proteic și îi face vulnerabili la săpun. Un virus cu acest „plic viral” îl folosește - împreună cu receptori specifici - pentru a intra într-o nouă celulă gazdă. Virușii au forme diferite, de la forme elicoidale simple și icosaedrice la structuri mai complexe. Virușii au dimensiuni cuprinse între 20 și 300 nanometri ; ar fi nevoie de 33.000 până la 500.000 dintre ele, una lângă alta, pentru a se întinde până la 1 centimetru (0,4 in ). [2]
Virușii se răspândesc în multe feluri. La fel cum mulți sunt foarte specifici în ceea ce privește specia gazdă sau țesutul pe care îl atacă, fiecare specie de virus se bazează pe o anumită metodă de propagare. Virușii vegetali sunt deseori răspândiți din plante în plante de către insecte și alte organisme, cunoscute sub numele de vectori. Unele virusuri de la oameni și alte animale se răspândesc prin expunerea la fluidele corporale infectate. Virușii precum gripa se răspândesc prin aer prin picături de umezeală atunci când oamenii tusesc sau strănut. Virușii precum norovirusul [3] se transmit pe calea fecal-orală , care implică contaminarea mâinilor, a alimentelor și a apei. Rotavirusul se răspândește adesea prin contact direct cu copiii infectați. Virusul imunodeficienței umane, HIV , este transmis de fluidele corporale transferate în timpul actului sexual . Altele, precum virusul dengue , sunt răspândite de insecte care suge sânge.
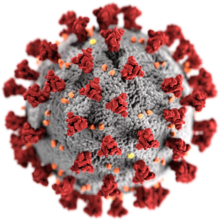
Virușii, în special cei care au ARN, pot muta rapid și pot da naștere la noi tipuri împotriva cărora gazdele lor au o protecție redusă. Virusul gripal, de exemplu, se schimbă des, motiv pentru care este necesar un nou vaccin în fiecare an. Schimbări majore pot provoca pandemii, cum ar fi în 2009, când gripa porcină s-a răspândit în majoritatea țărilor. Adesea, aceste mutații apar atunci când virusul a infectat alte animale, cum ar fi liliecii în cazul coronavirusului și porcine și păsări în gripă , înainte de a se răspândi la oameni.
Infecțiile virale pot provoca boli la oameni, animale și plante. La oameni și animale, acestea sunt de obicei eliminate de sistemul imunitar , oferind gazdei imunitate pe tot parcursul vieții la virusul respectiv. Antibioticele nu au efect, dar medicamentele antivirale pot trata infecțiile care pun viața în pericol. Vaccinurile care produc imunitate pe tot parcursul vieții pot preveni unele infecții.
Descoperire

În 1884, microbiologul francez Charles Chamberland a inventat filtrul Chamberland (sau filtrul Chamberland-Pasteur), care conține pori mai mici decât bacteriile. Astfel, el ar putea trece o soluție care conține bacterii prin filtru și le poate îndepărta complet. La începutul anilor 1890, biologul rus Dmitri Ivanovsky a folosit această metodă pentru a studia ceea ce a devenit cunoscut sub numele de virusul mozaicului tutunului . Experimentele sale au arătat că extractele din frunzele zdrobite ale plantelor de tutun infectate rămân infecțioase după filtrare. [4]
În același timp, alți oameni de știință au arătat că, deși acești agenți (numiți mai târziu virusuri ) erau diferiți de bacterii și de aproximativ o sută de ori mai mici, totuși ar putea provoca boli. În 1899, microbiologul olandez Martinus Beijerinck a observat că agentul s-a înmulțit doar în divizarea celulelor. El l-a numit „fluid viu contagios” ( latină : contagium vivum fluidum ) sau „germen viu solubil”, deoarece nu a putut găsi particule asemănătoare germenilor. [5]
La începutul secolului al XX-lea, bacteriologul englez Frederick Twort a descoperit viruși care infectează bacteriile [6], iar microbiologul franco-canadian Félix d'Herelle a descris viruși care, adăugați la bacteriile care cresc pe agar-agar , ar duce la formare a unor zone întregi de bacterii moarte. Numărarea acestor zone moarte i-a permis să calculeze numărul de viruși în suspensie. [7]
Invenția microscopului electronic în 1931 a dus la primele imagini de viruși. [8] În 1935, biochimistul și virusologul american Wendell Meredith Stanley a examinat virusul mozaicului tutunului și a constatat că acesta este în mare parte pe bază de proteine. [9] Puțin mai târziu, acest virus a fost separat în proteine și bucăți de ARN. [10] O problemă pentru oamenii de știință timpurii a fost că nu știau cum să crească viruși fără a folosi animale vii. Punctul de cotitură a venit în 1931, când patologul american Ernest William Goodpasture și soția sa, virologa Alice Miles Woodruff, au cultivat influența virusului și mai mulți alții în ouă de pui fertilizate. [11] Unele virusuri nu au putut fi cultivate în ouăle de pui. Problema a fost rezolvată în 1949, când John Franklin Enders , Thomas Huckle Weller și Frederick Chapman Robbins au dezvoltat poliovirusul în culturile celulare ale animalelor vii. [12] Au fost descoperite peste 4.800 de specii de virus. [1]
Origine
Virușii coexistă cu viața, oriunde se manifestă. Probabil au existat de când au evoluat celulele vii. Originea lor rămâne neclară, deoarece nu se fosilizează, astfel încât tehnicile moleculare au fost cea mai bună modalitate de a face ipoteza cum au apărut. Aceste tehnici se bazează pe disponibilitatea ADN-ului sau ARN-ului vechi, dar majoritatea virușilor depozitați și depozitați în laboratoare au mai puțin de 90 de ani. [13] [14] Metodele moleculare au fost eficiente numai în reconstituirea strămoșilor de viruși care au evoluat în secolul al XX-lea. [15] Este posibil să fi apărut în mod repetat noi grupuri de viruși în fiecare etapă a evoluției vieții.[16] Există trei teorii principale despre originea virușilor:[16] [17]
- Teoria regresivă
- Este posibil ca virusurile să fi fost celule mici care odată „parazitau” celule mai mari. În cele din urmă, genele de care nu mai aveau nevoie atunci când trăiau ca paraziți s-ar pierde. Bacteriile Rickettsia și Chlamydia sunt celule vii care, la fel ca virușii, se pot reproduce numai în celulele gazdă. Acest lucru susține această teorie, deoarece dependența lor de a fi paraziți ar fi putut duce la pierderea genelor care le-au permis cândva să trăiască singuri. [18]
- Teoria originii celulare
- Este posibil ca unele virusuri să fi evoluat din bucăți de ADN sau ARN care „au scăpat” din genele unui organism mai mare. ADN-ul evadat poate provine din plasmide - bucăți de ADN care se pot mișca între celule - în timp ce altele ar fi putut evolua din bacterii. [19]
- Teoria coevolutiei
- Este posibil ca virușii să fi evoluat din molecule complexe de proteine și ADN în același timp în care celulele au apărut pentru prima dată pe pământ și ar fi depins de viața celulară timp de multe milioane de ani. [20]
Niciuna dintre aceste teorii nu este pe deplin satisfăcătoare: cea regresivă nu explică de ce cel mai mic dintre paraziții celulari nu seamănă în niciun fel cu virușii. Ipoteza „materialului genetic scăpat” nu explică structurile particulelor virale. Ipoteza coevoluției, sau „virușii mai întâi”, contrazice definiția virușilor, deoarece depind de celulele care îi găzduiesc. [20] Mai mult, se recunoaște că virusurile sunt vechi și că au o origine înainte de diversificarea vieții în cele trei domenii . [21] [22] Această descoperire a determinat virologii moderni să reconsidere și să reevalueze aceste trei ipoteze clasice. [22][16]
Structura
O particulă virală, numită și virion , este alcătuită din gene formate din ADN sau ARN care sunt înconjurate de un strat protector de proteine numit capsidă . [2] Capsidul este alcătuit din multe molecule proteice identice mai mici, numite capsomeri . Dispunerea capsomerilor poate fi icosaedrică (20 de laturi), elicoidală sau mai complexă. Există o coajă interioară în jurul ADN-ului sau ARN-ului, numită nucleocapsidă , formată din proteine. Unii viruși sunt înconjurați de o bulă lipidică (grăsime) numită pericapsidă , care îi face vulnerabili la săpun și alcool. [23]
Dimensiuni
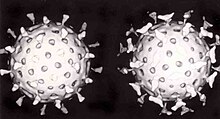
Virușii se numără printre cei mai mici agenți infecțioși și sunt prea mici pentru a fi văzuți prin microscopie cu lumină , majoritatea putând fi văzuți doar prin microscopie electronică . Dimensiunile lor variază de la 20 la 300 nanometri; ar fi nevoie de 30.000 până la 500.000 dintre ele, una lângă alta, pentru a se întinde până la un centimetru (0,4 in). [2] Pentru comparație, bacteriile au de obicei în jur de 1 000 nanometri (1 micrometru ) în diametru, iar celulele gazdă ale organismelor superioare au de obicei câteva zeci de micrometri. Unii viruși precum megavirusurile și pandoravirusurile sunt viruși relativ mari. La aproximativ 1000 nanometri, acești viruși, care infectează amibă , au fost descoperiți în 2003 și 2013. [24] [25] Există aproximativ zece ori mai mari (și, prin urmare, de o mie de ori mai mari în volum) ale virusului gripal și descoperirea acestora virușii „gigantici” au uimit oamenii de știință. [26]
Genele
Genele virusurilor sunt alcătuite din ADN (acid dezoxiribonucleic) și, în multe virusuri, ARN (acid ribonucleic). Informațiile biologice conținute într-un organism sunt codificate în ADN-ul sau ARN-ul său. Majoritatea organismelor folosesc ADN, dar mulți viruși au ca material genetic ARN-ul. ADN-ul sau ARN-ul virușilor constă dintr-o singură catenă sau o helică dublă. [27]
Virușii se reproduc rapid, deoarece au doar câteva gene. De exemplu, virusul gripal are doar opt gene, iar rotavirusul are unsprezece; prin comparație, oamenii au 20 000-25 000. Aceste gene codifică proteinele structurale, care formează particula virusului sau proteinele nestructurale, care se găsesc numai în celulele infectate cu virus. [28] [29]
Toate celulele și mulți viruși produc proteine care sunt enzime numite ADN polimeraze și ARN polimeraze care fac noi copii ale ADN și ARN. Enzimele virus polimerază sunt adesea mult mai eficiente în producerea ADN și ARN decât enzimele echivalente ale celulei gazdă, [30] dar enzimele virale ARN polimerază sunt predispuse la erori, determinând virușii să mute la ARN și să formeze noi tulpini. [31]
La unele specii de viruși ARN, genele nu se află pe o moleculă continuă de ARN, ci sunt separate. Virusul gripal, de exemplu, are opt gene separate din ARN. Când două tulpini diferite de virusuri gripale infectează aceeași celulă, aceste gene se pot amesteca și produc noi tulpini ale virusului într-un proces numit reasortare . [32] [33]
Sinteza proteinei

Organite : (1) nucleol (2) nucleu (3) ribozom (4) veziculă (5) reticul endoplasmatic dur (ER) (6) aparat Golgi (7) citoschelet (8) ER neted (9) mitocondrie (10) vacuol ( 11) citoplasmă (12) lizozom (13) centrioli în centrosom (14) un virus la scară aproximativă.
Proteinele sunt esențiale pentru viață. Celulele produc noi molecule de proteine din aminoacizi, pe baza informațiilor codificate în ADN. Fiecare tip de proteină este un fel de specialist care îndeplinește de obicei o singură funcție, deci dacă o celulă trebuie să facă ceva nou, trebuie să producă o nouă proteină. Virușii forțează celula să producă noi proteine de care nu are nevoie celula, dar care sunt necesare pentru ca virusul să se reproducă. Sinteza proteinelor constă din două etape principale: transcrierea și traducerea genelor . [34]
Transcrierea este procesul în care informațiile din ADN, numite cod genetic , sunt utilizate pentru a face copii ale ARN-ului numit ARN mesager (ARNm). Acestea migrează prin celulă și transportă codul către ribozomi, unde este folosit pentru a produce proteine. Aceasta se numește traducere, deoarece structura aminoacizilor proteinei este determinată de codul mARN. Informațiile sunt apoi traduse din limba acizilor nucleici în limba aminoacizilor. [34]
Unii acizi nucleici ai virusurilor ARN funcționează direct ca ARNm fără alte modificări. Din acest motiv, acești viruși sunt numiți viruși ARN cu sens pozitiv. [35] În alte virusuri ARN, ARN este o copie complementară a ARNm și acești viruși se bazează pe enzima celulei sau pe propria enzimă pentru a produce ARNm. Acestea sunt numite viruși ARN cu sens negativ . La virusurile obținute din ADN, metoda de producție a ARNm este similară cu cea a celulei. Speciile de virus numite retrovirusuri se comportă complet diferit: au ARN, dar în interiorul celulei gazdă se face o copie ADN a ARN-ului lor cu ajutorul enzimei revers transcriptază . Acest ADN este apoi încorporat în ADN-ul gazdei și copiat în ARNm prin căile normale ale celulei. [36]
Ciclu de viață
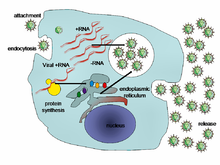
Când un virus infectează o celulă, virusul o forțează să producă mii de alți viruși. Aceasta face acest lucru prin faptul că celula copia ADN-ul sau ARN-ul virusului, creând proteine virale, care se asamblează pentru a forma noi particule de virus. [37]
Există șase etape de bază, care se suprapun în ciclul de viață al virusurilor din celulele vii: [38]
- Atașamentul este legarea virusului de molecule specifice de pe suprafața celulei. Această specificitate limitează virusul la un tip de celulă foarte limitat. De exemplu, virusul imunodeficienței umane (HIV) infectează numai celula T umană, deoarece proteina sa de suprafață, gp120 , poate reacționa doar cu CD4 și alte molecule de pe suprafața celulei T. Virușii vegetali se pot atașa numai la celulele vegetale. nu poate infecta animalele. Acest mecanism a evoluat pentru a favoriza acei viruși care infectează numai celulele în care sunt capabili să se reproducă.
- Intrarea urmează atașamentului; virușii intră în celula gazdă prin endocitoză sau prin fuziune cu celula.
- Neacoperirea are loc în interiorul celulei atunci când capsida virală este îndepărtată și distrusă de enzimele virale sau de enzimele gazdă, expunând astfel acidul nucleic viral.
- Replicarea particulelor de virus este etapa în care o celulă folosește ARN messenger viral în sistemele sale de sinteză a proteinelor pentru a produce proteine virale. Capacitățile de sinteză a ARN sau ADN ale celulei produc ADN-ul sau ARN-ul virusului.
- Asamblarea are loc în celulă atunci când proteinele virale nou create și acidul nucleic se combină pentru a forma sute de particule noi de virus.
- Eliberarea are loc atunci când virusii noi scapă sau sunt eliberați din celulă. Majoritatea virușilor realizează acest lucru prin spargerea celulelor, un proces numit liză . Alți viruși precum HIV sunt eliberați mai ușor printr-un proces numit „înmugurire” [39] ( înmugurire ).
Efecte asupra celulei gazdă
Virușii au o gamă largă de efecte structurale și biochimice asupra celulei gazdă. [40] Acestea se numesc efecte citopatice . [41] Majoritatea infecțiilor cu virusuri ajung să provoace moartea celulei gazdă. Cauzele morții includ liza celulară (explozie), modificări ale membranei de suprafață a celulei și apoptoza („sinuciderea” celulei). [42] Moartea celulară este adesea cauzată de încetarea activității sale normale din cauza proteinelor produse de virus, care nu sunt toate componentele particulei virusului. [43]
Unii viruși nu provoacă modificări aparente în celula infectată. Celulele în care virusul este latent [44] (inactiv) prezintă semne mici de infecție și adesea funcționează normal. [45] Acest lucru provoacă infecții persistente, iar virusul este deseori inactiv de multe luni sau ani. Acesta este adesea cazul herpesului simplex . [46] [47]
Unii viruși, cum ar fi virusul Epstein-Barr (herpesvirusul uman 4), cauzează adesea proliferarea celulară fără a provoca malignitate [48] ; dar alții, cum ar fi virusul papilom , sunt o cauză stabilită a cancerului. [49] Când ADN-ul unei celule este deteriorat de un virus, astfel încât celula nu se poate repara singură, aceasta declanșează adesea apoptoza. Unul dintre rezultatele apoptozei este distrugerea ADN-ului deteriorat de către celula însăși. Unii viruși au mecanisme de limitare a apoptozei, astfel încât celula gazdă să nu moară înainte ca virusii descendenți să fie produși; HIV , de exemplu, face acest lucru. [50]
Viruși și boli
Există multe modalități prin care virusurile se răspândesc de la gazdă la gazdă, dar fiecare specie de virus folosește doar una sau două. Multe virusuri care infectează plantele sunt transportate de organisme ; astfel de organisme se numesc vectori . Unele virusuri care infectează animale, inclusiv oameni, sunt răspândite și de vectori, de obicei insecte care suge sânge, dar transmiterea directă este mai frecventă. Unele infecții virale, cum ar fi norovirusul și rotavirusul , se răspândesc prin alimente și apă contaminate, din mâini și obiecte obișnuite fomite [51] și prin contact intim cu o altă persoană infectată, în timp ce altele sunt transmise prin aer (influența virusului). Virusuri precum HIV, hepatita B și hepatita C sunt adesea transmise de sex neprotejat sau de ace hipodermice contaminate. Pentru a preveni infecțiile și focarele, este important să știm cum se răspândește fiecare tip de virus. [52]
În oameni
Bolile umane cauzate în mod obișnuit de viruși includ răceala obișnuită , gripa , varicela și răni . Bolile grave precum Ebola ] și SIDA sunt, de asemenea, cauzate de viruși. [53] Multe virusuri cauzează boală mică sau deloc și se spune că sunt „benigne”. Cele mai dăunătoare virusuri sunt descrise ca virulente . [54] Virușii provoacă diferite boli în funcție de tipul de celulă pe care o infectează. Unele virusuri pot provoca infecții pe tot parcursul vieții sau infecții cronice în care virusurile continuă să se reproducă în organism, în ciuda mecanismelor de apărare ale gazdei. [55] Acest lucru este frecvent în infecțiile cu virusul hepatitei B și virusul hepatitei C. Persoanele infectate cronic cu un virus sunt cunoscute ca purtătoare. Acestea acționează ca rezervoare importante pentru virus. [56] [57]
Endemic
Dacă procentul de purtători într-o anumită populație atinge un anumit prag, boala se spune că este endemică . [58] Înainte de apariția practicii de vaccinare , infecțiile cu virusuri erau frecvente și focarele au apărut în mod regulat. În țările cu un climat temperat, bolile virale sunt de obicei sezoniere. Focarele de poliomielită , cauzate de poliovirus , au avut loc adesea în lunile de vară. [59] În schimb, răcelile, gripa și infecțiile cu rotavirus sunt de obicei o problemă în lunile de iarnă. [60] [61] Alte virusuri, cum ar fi rujeola , cauzează în mod regulat focare la fiecare trei ani. [62] În țările în curs de dezvoltare, virusurile care provoacă infecții respiratorii și enterice sunt frecvente pe tot parcursul anului. Virușii transportați de insecte sunt o cauză frecventă a bolilor în aceste medii. Zika și dengue, de exemplu, sunt transmise de țânțarii Aedes femele, care mușcă oamenii în special în timpul sezonului de reproducere a țânțarilor. [63]
Pandemie și „emergente”


Deși pandemiile virale sunt evenimente rare, HIV - a evoluat din virusurile găsite la maimuțe și cimpanzei - a fost o pandemie din cel puțin anii 1980. [65] Au existat patru pandemii cauzate de virus în secolul al XX-lea. în 1918, 1957 și 1968 au fost severe. [66] Înainte de eradicare, variola a fost cauza pandemiei timp de peste 3.000 de ani. [67] De-a lungul istoriei, migrația umană a favorizat răspândirea infecțiilor pandemice; mai întâi pe mare și în timpurile moderne și pe calea aerului. [68]
Cu excepția variolei, majoritatea pandemiilor sunt cauzate de viruși în evoluție recentă. Acești viruși „emergenți” sunt de obicei mutanți ai virușilor mai puțin dăunători care au circulat anterior atât la oameni, cât și la alte animale. [69]
Sindromul respirator acut sever (SARS) și Sindromul respirator din Orientul Mijlociu (MERS) sunt cauzate de noi tipuri de coronavirusuri . Se știe că alte coronavirusuri provoacă infecții ușoare la om [70], astfel virulența și răspândirea rapidă a infecțiilor cu SARS - care în iulie 2003 au provocat aproximativ 8.000 de cazuri și 800 de decese - a fost neașteptată și majoritatea țărilor nu au fost pregătite. [71]
Un coronavirus înrudit a apărut în Wuhan , China în noiembrie 2019 și s-a răspândit rapid în întreaga lume. Se crede că provine de la lilieci și denumit ulterior SARS-CoV-2 , declanșează infecții cu virus care cauzează o boală numită COVID-19 , cu severitate ușoară până la fatalitate [72] și care a dus la o pandemie în 2020 . [64] [73] [74] S- au impus restricții fără precedent în timp de pace în călătoriile internaționale [75] și stingeri de timp impuse în mai multe orașe importante din întreaga lume. [76]
La plante

Există multe tipuri de virusuri vegetale , dar de multe ori acestea provoacă doar o scădere a randamentului agricol și nu este viabil din punct de vedere economic să încercăm să le controlăm. Virușii vegetali sunt răspândiți adesea de la o plantă la alta prin organisme numite „ vectori ”. Acestea sunt de obicei insecte, dar s-a dovedit că unii ciuperci , viermi nematode și organisme unicelulare sunt vectori. Când controlul infecției cu virusul plantelor este considerat economic (fructe perene, de exemplu), eforturile se concentrează pe uciderea vectorilor și eliminarea gazdelor alternative, cum ar fi buruienile. [77] Virușii vegetali sunt inofensivi pentru oameni și alte animale, deoarece se pot reproduce numai în celulele vegetale vii. [78]
Bacteriofagii
Bacteriofagii sunt viruși care infectează bacteriile și archaea . Comitetul internațional pentru taxonomia virusurilor recunoaște oficial 28 de genuri de bacteriofagi aparținând a 11 familii. [79] Sunt importante în ecologia marină : când bacteriile infectate izbucnesc, compușii de carbon sunt eliberați în mediu, stimulând reînnoirea creșterii organice. Bacteriofagii sunt utili în cercetarea științifică, deoarece sunt inofensivi pentru oameni și pot fi studiați cu ușurință. Virușii pot fi o problemă în industriile care produc alimente și medicamente prin fermentare și depind de bacterii sănătoase. Unele infecții bacteriene devin dificil de controlat cu antibiotice, astfel că există un interes tot mai mare în utilizarea bacteriofagilor pentru tratarea infecțiilor la om. [80]
Rezistența gazdei
Imunitatea înnăscută a animalelor
Animalele, inclusiv oamenii, au multe apărări naturale împotriva virușilor. Unele sunt nespecifice și protejează împotriva multor viruși, indiferent de tip. Această imunitate înnăscută nu este îmbunătățită prin expunerea repetată la viruși și nu păstrează o „memorie” a infecției. Pielea animalelor, în special suprafața sa, care este formată din celule moarte, împiedică multe tipuri de viruși să infecteze gazda. Aciditatea conținutului stomacului distruge mulți viruși care au fost înghițiți. Când un virus traversează aceste bariere și intră în gazdă, alte mijloace de apărare înnăscute împiedică răspândirea infecției pe tot corpul. Un hormon special numit interferon este produs de organism atunci când sunt prezenți viruși, ceea ce împiedică reproducerea virusurilor prin uciderea celulelor infectate și a vecinilor acestora. În interiorul celulelor, există enzime care distrug ARN-ul de la viruși. Aceasta se numește interferență ARN . Unele celule sanguine înghit și distrug alte celule infectate cu virus. [81]
Imunitatea adaptativă a animalelor
Imunitatea specifică virusului se dezvoltă în timp și celulele albe din sânge numite limfocite joacă un rol central în ea. Limfocitele păstrează o „memorie” a infecțiilor virale și produc multe molecule speciale numite anticorpi . Acești anticorpi se atașează de viruși și împiedică virusul să infecteze celulele. Anticorpii sunt foarte selectivi și atacă doar un singur tip de virus. Organismul produce mulți anticorpi diferiți, în special în timpul infecției inițiale. Când infecția dispare, unii anticorpi rămân și continuă să fie produși, oferind de obicei gazdei imunitate pe tot parcursul vieții la virus. [82]
Rezistența plantelor
Plantele au mecanisme de apărare elaborate și eficiente împotriva virușilor. Una dintre cele mai eficiente este prezența așa-numitelor gene de rezistență (R). Ogni gene R conferisce resistenza a un particolare virus scatenando aree localizzate di morte cellulare intorno alla cellula infetta, che spesso possono essere viste ad occhio nudo come grandi macchie. Questo previene la diffusione dell'infezione. [83] L'interferenza dell'RNA è anche una difesa efficace nelle piante. [84] Quando sono infette, le piante spesso producono disinfettanti naturali che distruggono i virus, come acido salicilico , ossido nitrico e molecole reattive all'ossigeno . [85]
Resistenza ai batteriofagi
Il modo principale in cui i batteri si difendono dai batteriofagi è la produzione di enzimi che distruggono il DNA estraneo. Questi enzimi, chiamati endonucleasi di restrizione , distruggono il DNA virale che i batteriofagi iniettano nelle cellule batteriche. [86]
Prevenzione e cura delle malattie virali
Vaccini
I vaccini simulano un'infezione naturale e la sua risposta immunitaria associata, ma non causano la malattia. Il loro uso ha portato all'eradicazione del vaiolo ea un drastico declino della malattia e della morte causata da infezioni come polio , morbillo , parotite e rosolia . [87] Il loro utilizzo ha portato all'eradicazione del vaiolo ea un drastico declino delle malattie e dei decessi causati da infezioni come polio ], morbillo , parotite e rosolia . [88] Vi sono vaccini per prevenire oltre quattordici infezioni virali dell'uomo [89] e altri sono utilizzati per prevenire le infezioni virali degli animali. [90] I vaccini possono essere costituiti da virus vivi o uccisi. [91] I vaccini vivi contengono forme indebolite del virus, ma questi vaccini possono essere pericolosi se somministrati a persone con immunità debole . In queste persone il virus indebolito può causare la malattia che si vorrebbe prevenire. [92] La biotecnologia e le tecniche di ingegneria genetica sono utilizzate per produrre vaccini "progettati" (in laboratorio) che hanno solo le proteine capsidiche del virus. Il vaccino per l'epatite B appartiene a questa categoria. [93] Questi vaccini sono più sicuri perché non possono in alcun caso provocare la malattia. [91]
Farmaci antivirali
Dalla metà degli anni 1980, lo sviluppo di farmaci antivirali è aumentato rapidamente, soprattutto a causa della pandemia dell'AIDS. I farmaci antivirali sono spesso analoghi aciclici , che si mascherano da elementi costitutivi del DNA ( nucleosidici ). Quando inizia la replicazione del DNA del virus, vengono utilizzati alcuni dei falsi blocchi di costruzione. Questo impedisce la replicazione del DNA perché i farmaci mancano delle caratteristiche essenziali che permettono la formazione di una catena di DNA. Quando la produzione di DNA si arresta il virus non può più riprodursi. [94] Esempi di analoghi aciclici sono aciclovir per le infezioni da herpes virus e lamivudina per le infezioni da HIV e virus dell'epatite B . L'aciclovir è uno dei farmaci antivirali più antichi e più frequentemente prescritti. [95]
Altri farmaci antivirali si rivolgono a diversi stadi del ciclo di vita virale. L'HIV dipende da un enzima chiamato HIV-1 proteasi che rende il virus infettivo. Esiste una classe di farmaci chiamati inibitori della proteasi , che si legano a questo enzima e ne impediscono il funzionamento. [96] .
L'epatite C è causata da un virus RNA. Nell'80% delle persone infette, la malattia diventa cronica, e rimangono infettive per il resto della loro vita a meno che non vengano curate. Esiste un trattamento efficace che utilizza il farmaco analogo aciclico ribavirina . [97] I trattamenti per i portatori cronici del virus dell'epatite B sono stati sviluppati con una strategia simile, utilizzando lamivudina e altri farmaci antivirali. In entrambe le malattie, i farmaci impediscono al virus di riprodursi e l'interferone uccide le cellule infette rimaste. [98]
Le infezioni da HIV sono di solito trattate con una combinazione di farmaci antivirali, ognuno dei quali ha come bersaglio un diverso stadio del ciclo di vita del virus. Ci sono farmaci che impediscono al virus di attaccarsi alle cellule, altri che sono analoghi del nucleoside e alcuni avvelenano gli enzimi del virus di cui ha bisogno per riprodursi. Il successo di questi farmaci è la prova dell'importanza di sapere come i virus si riproducono. [96]
Ruolo nell'ecologia
I virus sono l'entità biologica più abbondante negli ambienti acquatici; [99] un cucchiaino di acqua di mare contiene circa dieci milioni di virus, [100] e sono essenziali per la regolazione degli ecosistemi di acqua salata e di acqua dolce. [101] La maggior parte sono batteriofagi, [102] che sono innocui per piante e animali. Infettano e distruggono i batteri delle comunità microbiche acquatiche e questo è il più importante meccanismo di riciclaggio del carbonio nell'ambiente marino. Le molecole organiche rilasciate dalle cellule batteriche dai virus stimolano la crescita di batteri e alghe fresche. [103] I microrganismi costituiscono oltre il 90% della biomassa del mare. Si stima che i virus uccidano circa il 20% di questa biomassa ogni giorno e che ci siano quindici volte più virus negli oceani di quanti siano i batteri e gli archei. Sono i principali responsabili della rapida distruzione delle nocive fioriture algali , [104] che spesso uccidono altre forme di vita marina. [105] Il numero di virus negli oceani diminuisce più al largo e più in profondità nell'acqua, dove ci sono meno organismi ospiti. [106]
I loro effetti sono di vasta portata; aumentando la quantità di respirazione negli oceani, i virus sono indirettamente responsabili della riduzione della quantità di anidride carbonica nell'atmosfera di circa 3 gigatonnellate di carbonio all'anno. [106]
Anche i mammiferi marini sono suscettibili di infezioni virali. Nel 1988 e nel 2002, migliaia di foche marine sono state uccise in Europa dal virus del cimurro focino . [107] Molti altri virus, tra cui calicivirus, herpesvirus, adenovirus e parvovirus, circolano nelle popolazioni di mammiferi marini. [106]
Note
- ^ a b King AM, Lefkowitz EJ, Mushegian AR, Adams MJ, Dutilh BE, Gorbalenya AE, Harrach B, Harrison RL, Junglen S, Knowles NJ, Kropinski AM, Krupovic M, Kuhn JH, Nibert ML, Rubino L, Sabanadzovic S, Sanfaçon H, Siddell SG, Simmonds P, Varsani A, Zerbini FM, Davison AJ, Changes to taxonomy and the International Code of Virus Classification and Nomenclature ratified by the International Committee Taxonomy of Viruses (2018) ( PDF ), in Archives of Virology , vol. 163, n. 9, settembre 2018, pp. 2601-31, DOI : 10.1007/s00705-018-3847-1 , PMID 29754305 . URL consultato il 27 marzo 2020 ( archiviato il 27 marzo 2020) .
- ^ a b c Collier pp. 33–55
- ^ Il norovirus, a volte indicato come il virus del vomito invernale, è la causa più comune di gastroenterite . L'infezione è caratterizzata da diarrea non sanguinolenta, vomito e mal di stomaco. Possono verificarsi anche febbre o mal di testa. I sintomi si sviluppano di solito da 12 a 48 ore dopo l'esposizione, e il recupero avviene di solito entro 1-3 giorni. Le complicazioni sono rare, ma possono includere disidratazione , soprattutto nei giovani, negli anziani e in coloro che hanno altri problemi di salute.
- ^ Shors p. 6
- ^ Collier p. 3
- ^ Shors p. 827
- ^ D'Herelle F, On an invisible microbe antagonistic toward dysenteric bacilli: brief note by Mr. F. D'Herelle, presented by Mr. Roux. 1917 , in Research in Microbiology , vol. 158, n. 7, 2007, pp. 553-54, DOI : 10.1016/j.resmic.2007.07.005 , PMID 17855060 .
- ^ Da Nobel Lectures, Physics 1981–1990 , (1993) A cura di Tore Frängsmyr, Editore Gösta Ekspång, World Scientific Publishing Co., Singapore
- ^ Stanley WM, Loring HS, The isolation of crystalline tobacco mosaic virus protein from diseased tomato plants , in Science , vol. 83, n. 2143, 1936, p. 85, Bibcode : 1936Sci....83...85S , DOI : 10.1126/science.83.2143.85 , PMID 17756690 .
- ^ Stanley WM, Lauffer MA, Disintegration of tobacco mosaic virus in urea solutions , in Science , vol. 89, n. 2311, 1939, pp. 345-47, Bibcode : 1939Sci....89..345S , DOI : 10.1126/science.89.2311.345 , PMID 17788438 .
- ^ Goodpasture EW, Woodruff AM, Buddingh GJ, The Cultivation Of Vaccine and other Viruses In The Chorioallantoic Membrane of Chick Embryos , in Science , vol. 74, n. 1919, October 1931, pp. 371-72, Bibcode : 1931Sci....74..371G , DOI : 10.1126/science.74.1919.371 , PMID 17810781 .
- ^ Rosen FS, Isolation of poliovirus – John Enders and the Nobel Prize , in N. Engl. J. Med. , vol. 351, n. 15, ottobre 2004, pp. 1481-83, DOI : 10.1056/NEJMp048202 , PMID 15470207 .
- ^ Shors. p. 16
- ^ Collier pp. 18–19
- ^ Liu Y, Nickle DC, Shriner D, Jensen MA, Learn GH, Mittler JE, Mullins JI, Molecular clock-like evolution of human immunodeficiency virus type 1 , in Virology , vol. 329, n. 1, novembre 2004, pp. 101-08, DOI : 10.1016/j.virol.2004.08.014 , PMID 15476878 .
- ^ a b c Krupovic M, Dooja W, Koonin EV, Origin of viruses: primordial replicators recruiting capsids from hosts. , in Nature Reviews Microbiology , vol. 17, n. 7, 2019, pp. 449-58, DOI : 10.1038/s41579-019-0205-6 , PMID 31142823 .
- ^ Collier pp. 11–21
- ^ Collier p. 11
- ^ Collier pp. 11–12
- ^ a b Wessner DR, The Origins of Viruses , in Nature Education , vol. 3, n. 9, 2010, p. 37.
- ^ Il sistema a tre domini è una classificazione biologica introdotta da Carl Woese et al. nel 1990 che divide le forme di vita cellulare in arcaie, batteri ed eucarioti . In particolare, sottolinea la separazione dei procarioti in due gruppi, originariamente chiamati Eubacteria (ora Bacteria ) e Archaebacteria (ora Archaea ). Woese ha sostenuto che, sulla base delle differenze nei geni rRNA 16S, questi due gruppi e gli eucarioti sono sorti ciascuno separatamente da un antenato con un apparato genetico poco sviluppato, spesso chiamato progenote . Per riflettere queste linee primarie di discendenza, egli ha trattato ciascuno come un dominio, diviso in diversi regni diversi. Woese inizialmente usò il termine "regno" per riferirsi ai tre raggruppamenti filogenici primari, e questa nomenclatura fu ampiamente utilizzata fino all'adozione del termine "dominio" nel 1990.
Parti della teoria dei tre domini sono state ferocemente messe in discussione da scienziati come Radhey S. Gupta, che sostiene che la divisione primaria all'interno dei procarioti dovrebbe essere tra quelli circondati da una singola membrana e quelli con due membrane. - ^ a b Mahy WJ & Van Regenmortel MH, Desk Encyclopedia of General Virology , Oxford, Academic Press, 2009, p. 28 , ISBN 0-12-375146-2 .
- ^ Rotter ML, Arguments for alcoholic hand disinfection , in The Journal of Hospital Infection , 48 Suppl A, agosto 2001, pp. S4–S8, DOI : 10.1016/s0195-6701(01)90004-0 , PMID 11759024 .
- ^ Abergel C, Legendre M, Claverie JM, 6 , in The rapidly expanding universe of giant viruses: Mimivirus, Pandoravirus, Pithovirus and Mollivirus , FEMS Microbiol. Rev. , vol. 39, novembre 2015, pp. 779-96, DOI : 10.1093/femsre/fuv037 , PMID 26391910 .
- ^ Philippe N, Legendre M, Doutre G, Couté Y, Poirot O, Lescot M, Arslan D, Seltzer V, Bertaux L, Bruley C, Garin J, Claverie JM, Abergel C, 6143 ( PDF ), in Pandoraviruses: amoeba viruses with genomes up to 2.5 Mb reaching that of parasitic eukaryotes , Science , vol. 341, luglio 2013, pp. 281-86, Bibcode : 2013Sci...341..281P , DOI : 10.1126/science.1239181 , PMID 23869018 . URL consultato il 30 marzo 2020 (archiviato dall' url originale il 2 aprile 2020) .
- ^ Zimmer C, Changing View on Viruses: Not So Small After All , in The New York Times , 18 luglio 2013. URL consultato il 20 dicembre 2014 ( archiviato il 20 dicembre 2014) .
- ^ Shors p. 81
- ^ Shors p. 129
- ^ Genome Sequencing Consortium International Human, Finishing the euchromatic sequence of the human genome , in Nature , vol. 431, n. 7011, 2004, pp. 931-45, Bibcode : 2004Natur.431..931H , DOI : 10.1038/nature03001 , PMID 15496913 .
- ^ Shors pp. 129–31
- ^ Shors p. 652
- ^ Il riassortimento è la miscelazione del materiale genetico di una specie in nuove combinazioni in individui diversi. Diversi distinti processi contribuiscono al riassortimento, tra cui l'assortimento di cromosomi, e il crossover cromosomico.
- ^ Shors p. 654
- ^ a b de Klerk E, 't Hoen PA, 3 , in Alternative mRNA transcription, processing, and translation: insights from RNA sequencing , Trends in Genetics : TIG , vol. 31, marzo 2015, pp. 128-39, DOI : 10.1016/j.tig.2015.01.001 , PMID 25648499 .
- ^ Collier pp. 75–82
- ^ Shors p. 698
- ^ Shors pp. 6–13
- ^ Shors pp. 121–23
- ^ Il "budding" attraverso l'effetto "cell envelope-in", prendendo in prestito dalla membrana cellulare per creare l'involucro virale del virus stesso, è più efficace per i virus che hanno bisogno di un involucro in primo luogo. Ne fanno parte virus avvolti come HIV, HSV, SARS o vaiolo. Prima di germogliare, il virus può mettere il proprio recettore sulla superficie della cellula in preparazione al germogliamento del virus, formando un involucro con i recettori virali già presenti. Anche se il germogliamento non distrugge immediatamente la cellula ospite, questo processo consumerà lentamente la membrana cellulare e alla fine porterà alla morte della cellula. Questo è anche il modo in cui le risposte antivirali sono in grado di rilevare le cellule infette da virus. Il budding è stato studiato in modo più approfondito per i virus degli eucarioti. Tuttavia, è stato dimostrato che i virus che infettano i procarioti del dominio Archaea utilizzano anche questo meccanismo di rilascio dei virioni.
- ^ Collier pp. 115–46
- ^ Collier p. 115
- ^ Okamoto T, Suzuki T, Kusakabe S, Tokunaga M, Hirano J, Miyata Y, Matsuura Y,Regulation of Apoptosis during Flavivirus Infection , in Viruses , vol. 9, n. 9, 2017, p. 243, DOI : 10.3390/v9090243 , PMC 5618009 , PMID 28846635 .
- ^ Alwine JC, Modulation of host cell stress responses by human cytomegalovirus , in Curr. Top. Microbiol. Immunol. , Current Topics in Microbiology and Immunology, vol. 325, 2008, pp. 263-79, DOI : 10.1007/978-3-540-77349-8_15 , ISBN 978-3-540-77348-1 , PMID 18637511 .
- ^ La latenza del virus (o latenza virale) è la capacità di un virus patogeno di rimanere dormiente (latente) all'interno di una cellula, indicata come la parte lisogenica del ciclo di vita virale. Un'infezione virale latente è un tipo di infezione virale persistente che si distingue da un'infezione virale cronica. La latenza è la fase del ciclo di vita di alcuni virus in cui, dopo l'infezione iniziale, cessa la proliferazione delle particelle virali. Tuttavia, il genoma virale non è completamente eradicato. Il risultato è che il virus può riattivarsi e iniziare a produrre grandi quantità di progenie virali (la parte litica del ciclo di vita virale) senza che l'ospite venga reinfettato da nuovi virus esterni e rimanga all'interno dell'ospite a tempo indeterminato. La latenza del virus non va confusa con la latenza clinica durante il periodo di incubazione quando un virus non è dormiente.
- ^ Sinclair J, Human cytomegalovirus: Latency and reactivation in the myeloid lineage , in J. Clin. Virol. , vol. 41, n. 3, marzo 2008, pp. 180-85, DOI : 10.1016/j.jcv.2007.11.014 , PMID 18164651 .
- ^ Jordan MC, Jordan GW, Stevens JG, Miller G, Latent herpesviruses of humans , in Ann. Intern. Med. , vol. 100, n. 6, giugno 1984, pp. 866-80, DOI : 10.7326/0003-4819-100-6-866 , PMID 6326635 .
- ^ Sissons JG, Bain M, Wills MR, Latency and reactivation of human cytomegalovirus ( PDF ), in J. Infect. , vol. 44, n. 2, febbraio 2002, pp. 73-77, DOI : 10.1053/jinf.2001.0948 , PMID 12076064 . URL consultato il 1º aprile 2020 ( archiviato il 28 aprile 2020) .
- ^ La malignità (dal latino malum , che significa "male", e - gnus , che significa "nato") è la tendenza di una condizione medica a peggiorare progressivamente. La malignità è più familiare come caratterizzazione del cancro. Un tumore maligno contrasta con un tumore benigno non canceroso in quanto un tumore maligno non è autolimitato nella sua crescita, è in grado di invadere i tessuti adiacenti, e può essere in grado di diffondersi a tessuti lontani. Un tumore benigno non ha nessuna di queste proprietà.
- ^ Graham SV, The human papillomavirus replication cycle, and its links to cancer progression: a comprehensive review , in Clinical Science , vol. 131, n. 17, 2017, pp. 2201-21, DOI : 10.1042/CS20160786 , PMID 28798073 .
- ^ Roulston A, Marcellus RC, Branton PE, Viruses and apoptosis , in Annu. Rev. Microbiol. , vol. 53, 1999, pp. 577-628, DOI : 10.1146/annurev.micro.53.1.577 , PMID 10547702 .
- ^ Un fomite è qualsiasi oggetto inanimato che, se contaminato o esposto ad agenti infettivi (come batteri patogeni, virus o funghi), può trasferire la malattia ad un nuovo ospite. Per gli esseri umani, le cellule della pelle, i capelli, i vestiti e le lenzuola sono comuni fomiti ospedalieri. I fomiti sono associati in particolare alle infezioni nosocomiali (HAI), in quanto sono possibili vie per il passaggio di agenti patogeni tra i pazienti. Mani non lavate in modo adeguato, stetoscopi e cravatte sono fomiti comuni associati ai fornitori di assistenza sanitaria.
- ^ Shors p. 32
- ^ Shors p. 271
- ^ Berngruber TW, Froissart R, Choisy M, Gandon S,Evolution of Virulence in Emerging Epidemics , in PLOS Pathogens , 9(3): e1003209, n. 3, 2013, pp. e1003209, DOI : 10.1371/journal.ppat.1003209 , PMC 3597519 , PMID 23516359 .
- ^ Shors p. 464
- ^ Tanaka J, Akita T, Ko K, Miura Y, Satake M,Countermeasures against viral hepatitis B and C in Japan: An epidemiological point of view , in Hepatology Research : The Official Journal of the Japan Society of Hepatology , vol. 49, n. 9, settembre 2019, pp. 990-1002, DOI : 10.1111/hepr.13417 , PMC 6852166 , PMID 31364248 .
- ^ Lai CC, Liu YH, Wang CY, Wang YH, Hsueh SC, Yen MY, Ko WC, Hsueh PR, Asymptomatic carrier state, acute respiratory disease, and pneumonia due to severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2): Facts and myths , in Journal of Microbiology, Immunology, and Infection = Wei Mian Yu Gan Ran Za Zhi , marzo 2020, DOI : 10.1016/j.jmii.2020.02.012 , PMID 32173241 .
- ^ Collier p. 766
- ^ Strand LK, The Terrible Summer of 1952 … When Polio Struck Our Family , in Seminars in Pediatric Neurology , vol. 26, luglio 2018, pp. 39-44, DOI : 10.1016/j.spen.2017.04.001 , PMID 29961515 .
- ^ Moorthy M, Castronovo D, Abraham A, Bhattacharyya S, Gradus S, Gorski J, Naumov YN, Fefferman NH, Naumova EN,Deviations in influenza seasonality: odd coincidence or obscure consequence? , in Clinical Microbiology and Infection : The Official Publication of the European Society of Clinical Microbiology and Infectious Diseases , vol. 18, n. 10, ottobre 2012, pp. 955-62, DOI : 10.1111/j.1469-0691.2012.03959.x , PMC 3442949 , PMID 22958213 .
- ^ Barril PA, Fumian TM, Prez VE, Gil PI, Martínez LC, Giordano MO, Masachessi G, Isa MB, Ferreyra LJ, Ré VE, Miagostovich M, Pavan JV, Nates SV, Rotavirus seasonality in urban sewage from Argentina: effect of meteorological variables on the viral load and the genetic diversity , in Environmental Research , vol. 138, aprile 2015, pp. 409-15, Bibcode : 2015ER....138..409B , DOI : 10.1016/j.envres.2015.03.004 , PMID 25777068 .
- ^ Durrheim DN, Crowcroft NS, Strebel PM, Measles – The epidemiology of elimination , in Vaccine , vol. 32, n. 51, dicembre 2014, pp. 6880-83, DOI : 10.1016/j.vaccine.2014.10.061 , PMID 25444814 .
- ^ Mbanzulu KM, Mboera LE, Luzolo FK, Wumba R, Misinzo G, Kimera SI,Mosquito-borne viral diseases in the Democratic Republic of the Congo: a review , in Parasites & Vectors , vol. 13, n. 1, febbraio 2020, p. 103, DOI : 10.1186/s13071-020-3985-7 , PMC 7045448 , PMID 32103776 .
- ^ a b Ashour HM, Elkhatib WF, Rahman MM, Elshabrawy HA, Insights into the Recent 2019 Novel Coronavirus (SARS-CoV-2) in Light of Past Human Coronavirus Outbreaks , in Pathogens (Basel, Switzerland) , vol. 9, n. 3, marzo 2020, p. 186, DOI : 10.3390/pathogens9030186 , PMID 32143502 .
- ^ Eisinger RW, Fauci AS,Ending the HIV/AIDS Pandemic1 , in Emerging Infectious Diseases , vol. 24, n. 3, marzo 2018, pp. 413-16, DOI : 10.3201/eid2403.171797 , PMC 5823353 , PMID 29460740 .
- ^ ( ZH ) Qin Y, Zhao MJ, Tan YY, Li XQ, Zheng JD, Peng ZB, Feng LZ, [History of influenza pandemics in China during the past century] , in Zhonghua Liu Xing Bing Xue Za Zhi = Zhonghua Liuxingbingxue Zazhi , vol. 39, n. 8, agosto 2018, pp. 1028-31, DOI : 10.3760/cma.j.issn.0254-6450.2018.08.003 , PMID 30180422 .
- ^ Nishiyama Y, Matsukuma S, Matsumura T, Kanatani Y, Saito T, Preparedness for a smallpox pandemic in Japan: public health perspectives , in Disaster Medicine and Public Health Preparedness , vol. 9, n. 2, aprile 2015, pp. 220-23, DOI : 10.1017/dmp.2014.157 , PMID 26060873 .
- ^ Houghton F, Geography, global pandemics & air travel: Faster, fuller, further & more frequent , in Journal of Infection and Public Health , vol. 12, n. 3, 2019, pp. 448-49, DOI : 10.1016/j.jiph.2019.02.020 , PMID 30878442 .
- ^ Virology Journal , su Virology Journal . URL consultato il 5 aprile 2020 (archiviato dall' url originale il 3 aprile 2020) .
- ^ Weiss SR, Leibowitz JL, Coronavirus pathogenesis , Advances in Virus Research, vol. 81, 2011, pp. 85-164, DOI : 10.1016/B978-0-12-385885-6.00009-2 , ISBN 978-0-12-385885-6 , PMID 22094080 .
- ^ Wong AT, Chen H, Liu SH, Hsu EK, Luk KS, Lai CK, Chan RF, Tsang OT, Choi KW, Kwan YW, Tong AY, Cheng VC, Tsang DC, From SARS to Avian Influenza Preparedness in Hong Kong , in Clinical Infectious Diseases , vol. 64, suppl_2, maggio 2017, pp. S98–S104, DOI : 10.1093/cid/cix123 , PMID 28475794 .
- ^ Report of the WHO-China Joint Mission on Coronavirus Disease 2019 (COVID-19) ( PDF ), World Health Organization (WHO), 16–24 febbraio 2020. URL consultato il 21 marzo 2020 ( archiviato il 10 marzo 2020) .
- ^ Deng SQ, Peng HJ,Characteristics of and Public Health Responses to the Coronavirus Disease 2019 Outbreak in China , in Journal of Clinical Medicine , vol. 9, n. 2, febbraio 2020, p. 575, DOI : 10.3390/jcm9020575 , PMC 7074453 , PMID 32093211 .
- ^ Han Q, Lin Q, Jin S, You L, Coronavirus 2019-nCoV: A brief perspective from the front line , in The Journal of Infection , vol. 80, n. 4, febbraio 2020, pp. 373-77, DOI : 10.1016/j.jinf.2020.02.010 , PMID 32109444 .
- ^ Londoño E, Ortiz A, Coronavirus Travel Restrictions, Across the Globe , NYTimes.com, 16 marzo 2020. URL consultato il 6 aprile 2020 ( archiviato il 30 marzo 2020) .
- ^ US takes more big pandemic response steps; Europe COVID-19 cases soar , su CIDRAP . URL consultato il 6 aprile 2020 ( archiviato il 30 marzo 2020) .
- ^ Shors p. 822
- ^ Shors pp. 802-03
- ^ Fauquet CM, Desk Encyclopedia of General Virology , Boston, Academic Press, 2009, p. 82 , ISBN 978-0-12-375146-1 .
- ^ Shors p. 803
- ^ Shors pp. 116–17
- ^ Shors pp. 225–33
- ^ Garcia-Ruiz H,Susceptibility Genes to Plant Viruses , in Viruses , vol. 10, n. 9, 2018, p. 484, DOI : 10.3390/v10090484 , PMC 6164914 , PMID 30201857 .
- ^ Shors p. 812
- ^ Soosaar JL, Burch-Smith TM, Dinesh-Kumar SP, Mechanisms of plant resistance to viruses , in Nature Reviews Microbiology , vol. 3, n. 10, 2005, pp. 789-98, DOI : 10.1038/nrmicro1239 , PMID 16132037 .
- ^ Horvath P, Barrangou R, CRISPR/Cas, the immune system of bacteria and archaea ( PDF ), in Science (New York, NY) , vol. 327, n. 5962, gennaio 2010, pp. 167-70, Bibcode : 2010Sci...327..167H , DOI : 10.1126/science.1179555 , PMID 20056882 . URL consultato il 12 aprile 2020 ( archiviato il 27 marzo 2020) .
- ^ Shors pp. 237-55
- ^ Shors pp. 237–55
- ^ Small JC, Ertl HC,Viruses – from pathogens to vaccine carriers , in Current Opinion in Virology , vol. 1, n. 4, 2011, pp. 241-45, DOI : 10.1016/j.coviro.2011.07.009 , PMC 3190199 , PMID 22003377 .
- ^ Burakova Y, Madera R, McVey S, Schlup JR, Shi J, Adjuvants for Animal Vaccines , in Viral Immunology , vol. 31, n. 1, 2018, pp. 11-22, DOI : 10.1089/vim.2017.0049 , PMID 28618246 .
- ^ a b Shors p. 237
- ^ Thomssen R, Live attenuated versus killed virus vaccines , in Monographs in Allergy , vol. 9, 1975, pp. 155-76, PMID 1090805 .
- ^ Shors p. 238
- ^ Shors pp. 514-15
- ^ Shors p. 514
- ^ a b Shors p. 568
- ^ Applegate TL, Fajardo E, Sacks JA, Hepatitis C Virus Diagnosis and the Holy Grail ( PDF ), in Infectious Disease Clinics of North America , vol. 32, n. 2, giugno 2018, pp. 425-45, DOI : 10.1016/j.idc.2018.02.010 , PMID 29778264 .
- ^ Paul N, Han SH,Combination Therapy for Chronic Hepatitis B: Current Indications , in Curr Hepat Rep , vol. 10, n. 2, giugno 2011, pp. 98-105, DOI : 10.1007/s11901-011-0095-1 , PMC 3085106 , PMID 21654909 .
- ^ Koonin EV, Senkevich TG, Dolja VV,The ancient Virus World and evolution of cells , in Biol. Direct , vol. 1, September 2006, p. 29, DOI : 10.1186/1745-6150-1-29 , PMC 1594570 , PMID 16984643 .
- ^ Dávila-Ramos S, Castelán-Sánchez HG, Martínez-Ávila L, Sánchez-Carbente MD, Peralta R, Hernández-Mendoza A, Dobson AD, Gonzalez RA, Pastor N, Batista-García RA,A Review on Viral Metagenomics in Extreme Environments , in Frontiers in Microbiology , vol. 10, 2019, p. 2403, DOI : 10.3389/fmicb.2019.02403 , PMC 6842933 , PMID 31749771 .
- ^ Shors p. 5
- ^ Breitbart M, Bonnain C, Malki K, Sawaya NA, Phage puppet masters of the marine microbial reale , in Nature Microbiology , vol. 3, n. 7, luglio 2018, pp. 754-66, DOI : 10.1038/s41564-018-0166-y , PMID 29867096 .
- ^ Shors pp. 25–26
- ^ Suttle CA, Viruses in the sea , in Nature , vol. 437, n. 7057, settembre 2005, pp. 356-61, Bibcode : 2005Natur.437..356S , DOI : 10.1038/nature04160 , PMID 16163346 .
- ^ Harmful Algal Blooms: Red Tide: Home | CDC HSB , su cdc.gov , www.cdc.gov. URL consultato il 23 agosto 2009 ( archiviato il 27 agosto 2009) .
- ^ a b c Suttle CA, Marine viruses – major players in the global ecosystem , in Nat. Rev. Microbiol. , vol. 5, n. 10, ottobre 2007, pp. 801-12, DOI : 10.1038/nrmicro1750 , PMID 17853907 .
- ^ Hall A, Jepson P, Goodman S, Harkonen T, Phocine distemper virus in the North and European Seas – Data and models, nature and nurture , in Biological Conservation , vol. 131, n. 2, 2006, pp. 221-29, DOI : 10.1016/j.biocon.2006.04.008 .
Bibliografia
- Collier, Leslie; Balows, Albert; Sussman Max, eds. (1998). Topley and Wilson's Microbiology and Microbial Infections . Volume 1, Virology (9th ed.). Arnold. ISBN 0-340-66316-2
- Shors, Teri (2017). Understanding Viruses . Jones and Bartlett Publishers. ISBN 978-1284025927
Voci correlate
Collegamenti esterni
- Virus Pathogen Resource —Dati genomici e altri dati di ricerca sui virus patogeni umani
- Influenza Research Database —Dati genomici e altri dati di ricerca sui virus influenzali
ins voci