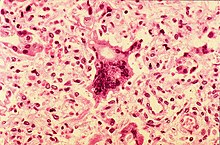
Pojar
| Pojar | |
|---|---|
| Erupție maculo-papulară de culoare roșu închis, confluentă, în special pe față | |
| Specialitate | boală infecțioasă |
| Clasificare și resurse externe (EN) | |
| Plasă | D008457 |
| MedlinePlus | 001569 |
| eMedicină | 966220 |
Rujeola (din latinescul morbus , boală [1] ) este o boală infecțioasă exantematoasă extrem de contagioasă cauzată de un virus , Paramyxovirus din genul Morbillivirus . [2] [3]
Rujeola provoacă în principal o erupție asemănătoare cu rubeola sau scarlatina , care de cele mai multe ori se rezolvă spontan [4], dar care poate duce, în cazuri relativ rare, la moarte, pierderea vederii [5] , pierderea auzului [6] , leziuni permanente ale creierului . [2] Semnele și simptomele inițiale includ, de obicei, febră , adesea peste 40 ° C, tuse , curgerea nasului și ochi roșii . [2] [7] La două-trei zile de la debutul simptomelor, se pot forma mici pete albe în gură , cunoscute sub numele de pete Köplik . O erupție cutanată roșie care începe de obicei pe față și apoi se răspândește în restul corpului începe de obicei la trei până la cinci zile după începerea simptomelor. [7] Simptomele se dezvoltă de obicei la 10-12 zile după expunerea la o persoană infectată și durează 7-10 zile. [8] [9] Complicațiile apar în aproximativ 30% din cazuri, la copii cu vârsta sub 5 ani și pot include, printre altele, diaree (8%), otită (7%), pneumonie (6%), encefalită (0,1%). [8] [10] Boala este responsabilă pentru un număr de decese variind de la 30 la 100 la 100 000 de persoane infectate și, de obicei, pentru suprainfecțiile bacteriene [4] . Rubeola (rujeola germană) și rujeola sunt diferite boli. [11]
Rujeola este o boală care se răspândește ușor prin aer, în special prin tuse și strănut de la persoanele infectate. Poate fi răspândit și prin contactul cu saliva sau secrețiile nazale. [8] Nouă din zece persoane care nu sunt imune și împărtășesc spațiul în care trăiesc cu o persoană infectată vor fi infectate. Oamenii sunt infecțioși de la patru zile înainte până la patru zile de la debutul erupției cutanate . [10]
Odată contractată, rujeola dă imunizare teoretic definitivă, deci nu te vei mai îmbolnăvi pe toată durata vieții. [4] [8] Testul antivirus, pentru utilizare în cazuri suspecte, este important pentru inițiativele de sănătate publică. [10]
Vaccinul împotriva rujeolei este eficient în prevenirea bolii. Vaccinarea a dus la o scădere cu 75% a deceselor cauzate de această boală între 2000 și 2013, iar aproximativ 85% dintre copiii din întreaga lume sunt vaccinați. Nu este disponibil un tratament specific. Îngrijirea de susținere poate îmbunătăți prognosticul . [8] Aceasta poate consta în administrarea unei soluții de rehidratare orală, alimente sănătoase și medicamente pentru combaterea febrei . [8] [9] Antibioticele pot fi utilizate dacă apare o infecție bacteriană secundară, cum ar fi pneumonia . Aportul de vitamina A este recomandat și în țările în curs de dezvoltare . [8]
În era pre-vaccinare, rujeola era endemică aproape în toată lumea și majoritatea oamenilor erau infectați în copilărie. Focarele regulate s-au produs la intervale de 2 - 5 ani la majoritatea populațiilor și puțini oameni au rămas susceptibili după vârsta de 20 de ani. [12] Astăzi, rujeola, în ciuda campaniilor de vaccinare, continuă să afecteze câteva milioane de oameni pe an, [2] în special în zonele în curs de dezvoltare din Africa și Asia [8] și se numără printre cele care pot fi prevenite prin vaccinare, boala care cauzează mai multe decese decât oricare alta boală. [13] Au existat aproximativ 96.000 de decese datorate rujeolei în 2013, o scădere față de cele 545.000 de decese înregistrate în 1990. [14] Se estimează că în anii 1980 , boala a cauzat 2,6 milioane de decese în anul. [8] Înainte ca vaccinul să fie disponibil, trei până la patru milioane de cazuri au apărut în fiecare an în Statele Unite . [10] Majoritatea deceselor implică copii sub vârsta de cinci ani. [8] Riscul de deces în rândul celor infectați este de obicei de 0,2%, [10] dar poate ajunge până la 10% la cei care suferă de malnutriție . [8] Nu se crede că afectează alte animale. [8]
Istorie


Estimările bazate pe biologia moleculară modernă plasează apariția rujeolei ca boală umană la scurt timp după 500 d.Hr. [16] (ideea anterioară că ciuma Antonină din 165-180 d.Hr. a fost cauzată de rujeolă este acum discreditată). Prima descriere sistematică a bolii și distincția acesteia de variolă și varicelă este atribuită medicului persan Rhazes (860-932), care a publicat cartea despre variolă și rujeolă . [17] Având în vedere ceea ce se știe astăzi despre evoluția rujeolei, relatarea lui Rhazes pare extraordinar de precisă și lucrările recente care examinează rata mutației virusului indică faptul că virusul rujeolei a provenit din cel al pestei bovine ( ciuma bovinelor ) ca o zoonoză între 1100 d.Hr. și 1200, o perioadă care ar fi putut fi precedată de focare limitate care implică un virus care nu a fost încă complet adaptat la oameni. [16] Acest lucru este de acord cu afirmația că rujeola necesită o populație susceptibilă mai mare de 500.000 pentru a susține o epidemie, situație care a avut loc doar în urma creșterii orașelor medievale europene. [18]
Rujeola este o boală endemică, ceea ce înseamnă că este prezentă continuu într-o comunitate, iar mulți oameni reușesc să dezvolte rezistență. La populațiile neobișnuite cu rujeola, eventuala expunere la un nou focar poate fi devastatoare. În 1529, o epidemie de rujeolă în Cuba a ucis două treimi din cei care au supraviețuit anterior variolei . Doi ani mai târziu, rujeola a fost responsabilă de moartea a jumătate din populația din Honduras și a lovit puternic Mexicul , America Centrală și civilizația inca . [19]
Între 1855 și 2005, se estimează că rujeola ar fi ucis aproximativ 200 de milioane de oameni în întreaga lume. [20] În 1850 a fost responsabilă de moartea a 20% din populația Hawaii . [21] În 1875, rujeola a ucis peste 40.000 de fijieni , aproximativ o treime din populație. [22] Se crede că șapte până la opt milioane de copii din întreaga lume au murit în fiecare an înainte de introducerea vaccinului. [23]
În 1954, virusul care a cauzat boala a fost izolat de la un băiat de 13 ani, David Edmonston, și apoi s-a adaptat și s-a propagat în cultura țesutului embrionar de pui. [24] Până în prezent, au fost identificate douăzeci și unu de genotipuri ale virusului rujeolic. [25] La Merck , Maurice Hilleman a dezvoltat primul vaccin de succes [26] și în 1963 au fost puse la dispoziție mai multe vaccinuri. [27] În 1958, a fost dezvoltat un vaccin îmbunătățit împotriva rujeolei. [28] Rujeola, ca boală endemică, a fost eliminată din Statele Unite în 2000, dar continuă să fie prezentă, transportată de călători internaționali.
Epidemiologie
| Incidența rujeolei, OMS a raportat cazuri [29] | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Regiunile OMS | 1980 | 1990 | 2000 | 2005 | 2010 | 2011 | 2012 | 2013 | 2014 | 2015 |
| Africa [30] | 1 240 993 | 481 204 | 520 102 | 316 219 | 199 174 | 195 620 | 108 004 | 171 178 | 73 914 | 52 754 |
| America [31] | 257 790 | 218 579 | 1 754 | 85 | 247 | 1 348 | 143 | 491 | 1 966 | 611 |
| Orientul Mijlociu [32] | 341 624 | 59 058 | 38 592 | 15 069 | 10 072 | 34 667 | 34 504 | 20 884 | 18 080 | 21 336 |
| Europa [33] | 851 849 | 234 827 | 37 421 | 37 338 | 30 625 | 37 101 | 27 379 | 26 436 | 14 176 | 25 958 |
| Asia de Sud-Est [34] | 199 535 | 224 925 | 78 558 | 88 973 | 54 228 | 69 546 | 46 945 | 30 101 | 41 346 | 29 927 |
| Pacificul de Vest [35] | 1 319 640 | 155 490 | 177 052 | 128 017 | 49 460 | 21 050 | 10 764 | 31 844 | 131 043 | 65 176 |
| Lume | 4 211 431 | 1 374 083 | 853 479 | 585 701 | 343 806 | 359 332 | 227 739 | 280 934 | 280 525 | 195 762 |
| Sistemul de supraveghere a rujeolei relevă o discrepanță a datelor între numărul de cazuri raportate și numărul de decese, OMS a estimat că în 2000 cazurile de rujeolă au fost 32 768 300, iar în 2015 9 719 600. [36] | ||||||||||
Rujeola este o boală extrem de contagioasă, iar prezența sa continuă într-o comunitate depinde de generația de gazde sensibile , predominant de nașterea copiilor. În comunitățile care generează insuficiente gazde noi, boala va dispărea. Acest concept a fost recunoscut de Bartlett în 1957, care s-a referit la numărul minim de suport al rujeolei ca fiind dimensiunea critică a comunității. [37] Analiza focarelor din comunitățile insulare a sugerat că dimensiunea critică pentru rujeolă este de aproximativ 250.000 de indivizi. [38] Pentru a obține imunitatea efectivului , mai mult de 95% din comunitate trebuie vaccinată datorită ușurinței cu care virusul este transmis de la persoană la persoană. [23]
În 2015, Organizația Mondială a Sănătății a estimat 134.200 de decese cauzate de rujeolă; un declin accentuat față de 651 600 de decese estimate în 2000. [36] [39] Din 2013, rujeola rămâne principala cauză a deceselor care pot fi prevenite prin vaccinare la nivel mondial. [13] În țările dezvoltate, decesul se produce într-unul sau două cazuri la 1 000 (0,1% - 0,2%). [40] La populațiile cu niveluri ridicate de malnutriție și lipsa unei îngrijiri medicale adecvate, letalitatea asociată rujeolei poate ajunge la 10%. [39] Focarele (trei sau mai multe cazuri) de rujeolă pot duce la mortalitate deosebit de mare în zonele de război, lagărele de refugiați sau în cazul în care dezastrele naturale au compromis instituțiile de sănătate. [39] Decesele se datorează în principal complicațiilor și în șase din zece cazuri din cauza pneumoniei. [12] În 2015, se estimează că numărul deceselor datorate rujeolei a fost cu 79% mai mic decât în 2000, datorită creșterii ratelor de vaccinare în rândul statelor membre ONU . [36]
Epidemii
Imunizarea împotriva rujeolei, care a început în 1960, a schimbat radical epidemiologia bolii. Rujeola nu mai este endemică în multe țări, dar focarele care rezultă, în mare parte, din cazuri importate, pot apărea în multe țări în care subseturile populației nu sunt imunizate în mod adecvat. Cu cât este mai mare acoperirea de vaccinare, cu atât impactul rujeolei este mai mic chiar și în cazul cazurilor importate. Gradul de succes al programelor naționale de vaccinare împotriva rujeolei, măsurat prin acoperirea realizată, este semnificativ asociat cu impactul rujeolei. [41] [42] Imunizarea de rutină în copilărie duce la o lărgire a intervalelor de timp dintre epidemii în timpul cărora se acumulează grupul de indivizi sensibili. Acest lucru determină o creștere a vârstei, a copiilor mai mari și a adulților tineri, a cazurilor de rujeolă în epidemiile din țările cu cea mai mare acoperire de vaccinare. [12]
| Italia, numărul de cazuri anuale și acoperirea cu vaccinare [43] [44] | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| 2016 | 2015 | 2014 | 2013 | 2012 | 2011 | 2010 | 2009 | 2008 | |
| Prima acoperire de vaccinare (%) | - | 85 | 87 | 90 | 90 | 90 | 91 | 90 | 90 |
| Numărul de cazuri | 843 | 252 | 1 694 | 2 251 | 389 | 965 | 909 | 1 103 | 1 387 |
Din 2011 până în 2016, au fost raportate peste 160.000 de cazuri în 30 de țări europene. Majoritatea au apărut la persoane nevaccinate și cu focare majore în cinci țări europene: Germania , Italia , Franța , România și Regatul Unit . La începutul anului 2014, a existat un focar de rujeolă în Vietnam, care a dus la peste 100 de decese. [45] [46]
În 2014, o revizuire efectuată de Centers for Disease Control a înregistrat un total de 911 cazuri de rujeolă între 2001 și 2011, cu un număr mediu anual de 61 de cazuri, concluzionând că „eliminarea endemică a rujeolei a fost realizată în Statele Unite. United”. [47] Cu toate acestea, în 2014, în Statele Unite a apărut un focar de rujeolă cu o prevalență mai mare decât se prevedea, având în vedere peste douăzeci de ani de acoperire a vaccinării de peste 90%. Dintre cele 23 de focare din 2014, majoritatea depindeau de nerezidenți, cu tulpini virale importate în principal din Filipine, dar un focar major, 283 de cazuri, s-a dezvoltat într-o comunitate amish care nu a fost vaccinată din motive religioase. [48] În 2015, o femeie din SUA a murit de pneumonie în urma rujeolei. A fost prima moarte din Statele Unite din cauza rujeolei din 2003. [49] Femeia fusese vaccinată împotriva rujeolei, dar lua medicamente imunosupresoare pentru o altă afecțiune. [50]
Între 29 septembrie 2014 și 27 septembrie 2015, 1392 de cazuri de rujeolă au fost raportate în Berlin , capitala Germaniei . Majoritatea cazurilor au fost raportate din ianuarie până în aprilie. Tulpina de virus a fost identificată ca fiind presupusă importată de solicitanții de azil din Bosnia și Herțegovina și Serbia . În Bosnia și Herțegovina, o epidemie de rujeolă cu mii de cazuri a fost deja intensă în februarie 2014. [51] [52]
În primele luni ale anului 2017, începând cu 16 aprilie, în Italia au fost raportate 1603 de cazuri de rujeolă, mai mult decât dublul cazurilor din întregul an anterior. [53] Epidemia, atribuită unei acoperiri precare a vaccinării, a determinat Centrele pentru Controlul Bolilor din SUA să alerteze călătorii cu privire la riscul rujeolei pentru cei care vizitează Italia. [54] [55]
Între 1987 și 2000, rata mortalității în Statele Unite din cauza rujeolei a fost de trei din 1000 de cazuri, sau 0,3%. [56] În Italia, rata mortalității este între 0,1% și 0,03% [4] . În țările în curs de dezvoltare, cu rate ridicate de malnutriție și asistență medicală slabă, ratele mortalității au fost de aproximativ 28%. [56] La indivizii imunocompromiși (de exemplu, persoanele cu SIDA ) rata letalității este de aproximativ 30%. [57] Cei mai gravi factori de risc pentru rujeolă și complicațiile acesteia includ malnutriția, [58] imunodeficiența , [58] sarcina , [58] și deficitul de vitamina A. [58] [59]
Etiologie

Rujeola este cauzată de Paramyxovirus , un virus ARN monocatenar negativ din genul Morbillivirus din familia Paramyxoviridae . [12] Virusul a fost izolat în 1954 de laureatul Nobel John Franklin Enders și Thomas Peebles, de la pacienți cu pete Köplik. [60]
Virusul rujeolei este legat de alți virusuri din aceeași familie care infectează animalele, inclusiv virusul tulburător canin și virusul pestei bovine . Primatele pot fi infectate in vitro, dar oamenii sunt singurele gazde naturale ale virusului și nu există alte rezervoare de animale cunoscute.
Acest virus este extrem de contagios și se răspândește prin tuse și strănut, cu contact personal strâns sau contact direct cu secreții. Factorii de risc pentru infecția cu virusul rujeolic includ imunodeficiența cauzată de HIV sau SIDA , [61] imunosupresia după transplantul de organe sau transplantul de celule stem hematopoietice , [62] terapia cu corticosteroizi , [58] călătoriile în zonele în care rujeola este endemică sau contactul cu călătorii din aceste zone [58] și pierderea anticorpilor , moștenite înainte de vârsta vaccinării de rutină. [63]
Mod de contagiune
Rujeola este o boală infecțioasă acută cu un indice de contagiozitate foarte ridicat (97-98%); infecția are loc prin aer, cu virusul transportat de picăturile Flugge , prin contact direct sau indirect cu fluidele corporale ale unei persoane bolnave (spermatozoizi, mucus). Pacientul este contagios cu 1-3 zile înainte de apariția simptomelor (și apoi cu 3-5 zile înainte de apariția manifestărilor cutanate) până la 7 zile după apariția ' erupției cutanate . [64]
semne si simptome
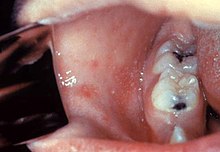
Semnele și simptomele clasice ale rujeolei încep în faza preexantematoasă cu febră mare timp de patru zile, urmate de semne de mucozită: tuse , rinită (frig, febră, strănut) și conjunctivită (ochi roșii) / fotofobie . [65] Petele Köplik care pot fi văzute în interiorul gurii sunt patognomonice ( diagnostice ) pentru rujeolă, dar sunt temporare (24-48 de ore) și, prin urmare, pot să nu fie văzute. [65] Recunoașterea acestor pete înainte ca o persoană să atingă maximum de infectivitate poate ajuta medicii să reducă răspândirea bolii. [66] Febra este frecventă și durează de obicei aproximativ o săptămână, ajungând la 40 ° C. [23] Erupția tipică de rujeolă apare la 3-4 zile de la debutul fazei preexantematoase. Erupția caracteristică a rujeolei este descrisă în mod clasic ca o erupție cutanată maculopapulară roșie generalizată care începe la câteva zile după debutul febrei . Începe din spatele urechilor și lângă linia părului, după câteva ore, se răspândește în cap și gât înainte de a acoperi cea mai mare parte a corpului, cauzând adesea mâncărime . Această erupție durează până la opt zile. Erupția este numită „pată”, schimbând culoarea de la roșu la maro închis, decolorând în 3-4 zile, înainte de a dispărea. Remisiunea exantemului poate prezenta o descuamare de tip mătreață. [67] În general, rujeola se rezolvă de obicei după aproximativ trei săptămâni. [23]
Într-o formă rară și severă de rujeolă, numită „rujeolă hemoragică”, clasificată și ca o complicație a rujeolei, există hemoragii cutanate și viscerale, petechii, hematurie , echimoze, epistaxis . [10]
Complicații
Boala are aproape întotdeauna o evoluție benignă, deși unele forme pot fi deosebit de agresive (în special la subiecții cu apărare imună scăzută), dar pot apărea complicații care sunt mai frecvente la copiii foarte mici și la adulți. Cele mai frecvente se datorează infecției bacteriene suprapuse. Complicațiile pot afecta sistemul respirator, sistemul nervos, sistemul gastro-enteric, sistemul vizual și urechea, cu posibilitatea agravării până la probleme grave cu vederea sau auzul.
Unele complicații ale rujeolei sunt relativ frecvente, aproximativ 20-30% din cazuri au una sau mai multe complicații și au o codificare specifică în sistemul internațional de codificare a bolii ICD-10 .
- B05.0 Rujeola complicată de encefalită
- B05.1 Rujeola complicată de meningită
- B05.2 Rujeolă complicată de pneumonie
- B05.3 Rujeola complicată de otita medie acută
- B05.4 Rujeola cu complicații intestinale.
Cele mai frecvente sunt complicațiile intestinale, diareea , stomatita , care pot duce la deshidratare (8%), otita medie (1-9%) și pneumonie , atât pneumonie virală directă, cât și pneumonie bacteriană secundară, (1-6%). [68] Encefalita acută [69] , panencefalita sclerozantă subacută, ulcerele corneene (care duc la cicatrizarea corneei) [70] , sindromul rujeolic atipic și purpura trombocitopenică acută sunt la rate mai mici. [2] [10] Complicațiile sunt, în general, mai severe la adulții care contractă virusul și la indivizii subnutriți sau imunocompromiși. [10] [71] În 1920, rata mortalității prin pneumonie după rujeolă a fost de aproximativ 30%. [72]
Infecție a urechii
Otita medie acută a fost cea mai frecventă complicație în unele epidemii de rujeolă, apărând la peste 25% dintre subiecții infectați. Se presupune că se datorează unei insuficiențe tranzitorii a răspunsului imun la infecție. Virusul rujeolic a fost izolat în lichidul urechii medii. [6] [73] Unele cazuri de hipoacuzie asociate rujeolei se pot atribui superinfecțiilor bacteriene, precum și labirintitei virale. [74]
Pneumonie
Este o infecție pulmonară datorată morbillivirusului care poate apărea și în cursul unei rujeole care nu este evident complicată; la sugari, este o cauză frecventă de deces. De obicei, se manifestă ca pneumonie interstițială asociată cu inflamația tuburilor bronșice ( bronșită ), în principal cu o tulburare de respirație ( dispnee și tuse ). Epiteliul sistemului respirator este afectat direct de virusul rujeolic și se observă o pierdere a ciliilor pulmonari. Din aceste leziuni rezultă o predispoziție la complicații din suprainfecția bacteriană.
O formă rară de pneumonie virală asociată rujeolei este pneumonia cu celule uriașe . Boala, cunoscută și sub numele de pneumonie a lui Hecht, se caracterizează prin prezența corpurilor de incluziune a celulelor gigantice multinucleate. De obicei asociat cu rujeola, poate fi identificat și cu tuse convulsivă și rareori cu difterie sau gripă . Apare în principal la copiii cu boli ale sistemului reticuloendotelial sau indivizii debilitați și are un prognostic slab.
Complicații neurologice
Virusul rujeolic este neurotrop. Implicarea sistemului nervos central este frecventă în rujeolă în timpul bolii, atât de mult încât modificări electro-encefalografice au fost raportate în 50% din cazurile de rujeolă necomplicate. [75]
Au fost identificate mai multe complicații neurologice ale rujeolei:
- meningită aseptică
- encefalită primară
- encefalita acută demielinizantă (ADEM)
- incluziune morbidă-encefalită corporală (MIBE)
- panencefalita sclerozantă subacută (SSP).
Meningita aseptică
O creștere a cazurilor de meningită virală asociată cu focare de rujeolă a fost observată și în țările avansate. [76] Virusul rujeolei ar trece de la căile respiratorii la lichidul coloanei vertebrale, inflamând meningele. Inflamația se poate limita la meningi sau se poate răspândi în creier ( meningoencefalită ).
Encefalita morbidă primară
Encefalita primară poate începe în faza exantematoasă a rujeolei în primele 7 zile. Se crede că se datorează invaziei directe și replicării virusului în sistemul nervos central, urmată de infiltratele de leucocite și de producerea de citokine. [77] Virusul poate fi detectat în serul cefalorahidian și în țesuturile nervoase. Se caracterizează inițial prin agitație sau somnolență, care în câteva ore poate duce la convulsii, deficite motorii și senzoriale, până la comă. S-ar produce în 0,1-0,3% din cazuri cu o rată de letalitate de aproximativ 15%. [78]
Encefalita acută demielinizantă
Encefalita acută demielinizantă sau encefalomielita acută diseminată apare în aproximativ 0,1% din cazurile raportate și 1 din 1-2.000.000 de vaccinări. Este o encefalită demielinizantă postinfecțioasă cauzată de o inflamație mediată imun în urma infecției rujeolice. Debutul apare de obicei la 2 până la 30 de zile după infecție și se caracterizează prin febră, cefalee, vărsături, gât rigid, meningită, somnolență, convulsii și comă . Disfuncțiile vezicii urinare și intestinale apar în cazurile cu afectare a măduvei osoase. Lichidul cefalorahidian prezintă proliferare celulară și concentrație crescută de proteine , dar, contrar encefalitei primare, nu permite izolarea virusului. Rata letalității este de aproximativ 5% la copii și 25% la adulți. Unele forme de leziuni neurologice reziduale apar în peste 25% din cazuri. Convulsiile (cu sau fără febră) sunt raportate în 0,6% -0,7% din cazuri. [78]
Panencefalita sclerozantă subacută (SSPE)
Panencefalita sclerozantă subacută sau leucoencefalita se datorează unui virus rujeolic mutant care provoacă inflamații cerebrale persistente (umflături și iritații).
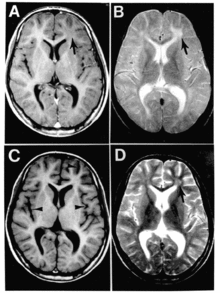
A + B: situație la prima investigație, săgețile indică leziuni inflamatorii în creier.
C + D: situație trei luni mai târziu. Leziunile sunt mai puțin proeminente, dar apare clar atrofia corticală
Panencefalita sclerozantă subacută este o boală degenerativă rară a sistemului nervos central despre care se crede că se datorează infecției persistente a virusului rujeolic în creier. Debutul apare de obicei înainte de vârsta de 20 de ani, în medie la aproximativ 7 ani de la contractarea rujeolei (min 1 lună - max 27 ani) și apare în cinci până la zece cazuri la un milion de cazuri de rujeolă raportate. [10] [79] Debutul este insidios, cu o deteriorare progresivă a comportamentului și a intelectului, urmată de ataxie , convulsii mioclonice și, în cele din urmă, moarte. SSPE a fost extrem de rar de când există programe de vaccinare, dar studii recente concluzionează că incidența sa asupra celor care au contractat rujeola înainte de vârsta de 2 ani este de ordinul 1 din 630 [80] [81] , 1 din 1000 [82] , 1 din 5 000. [83] Singurul mod în care copiii pot fi protejați înainte de a ajunge la vârsta vaccinării este de a evita expunerea lor la persoane și persoane potențial infecțioase. [80] [81]
Incluziunea morbidă-encefalită corporală (MIBE)
La persoanele cu imunodeficiență congenitală sau dobândită, în special cu limfoame sau leucemie, în cazuri rare poate apărea o formă specială de incluziune a rujeolei - encefalită corporală. Această complicație apare de obicei în decurs de un an de la infecția rujeolică și este foarte dificil de tratat, ducând la deces în câteva luni. În MIBE, clonele virale prezente în creier suferă mutații ale proteinelor din învelișul viral, similar cu mutațiile virusului din SSP. [84] [85] [86] MIBE poate fi cauzat și de virusul de vaccinare la persoanele imunodeprimate. [87] Din acest motiv și din alte motive, persoanele cu imunodeficiență congenitală sau dobândită deosebit de severă (simptomatică) nu trebuie vaccinate împotriva rujeolei. [10] [88]
Complicații oftalmice
În 2004, cercetările au estimat că rujeola a fost cauza a 15 până la 60.000 de cazuri de orbire infantilă în fiecare an. [5] Pe lângă conjunctivita care apare la aproape toți pacienții cu rujeolă în stadiul preexantematos și care se rezolvă cel mai adesea spontan, poate apărea cheratita , o infecție a corneei . În comparație cu conjunctivita, cheratita are simptome mai severe și consecințe mult mai periculoase. Simptomele includ durere, roșeață și sensibilitate la lumină. Se poate simți că ai nisip în ochi. Adesea tratată cu picături medicamentoase, cheratita provoacă temporar vederea neclară, dar dacă duce la ulcerații, deteriorarea vederii poate fi permanentă. [70] Ulcerele corneene pot apărea ca rezultat al infecției produse de virusul rujeolei sau de suprainfecția bacteriană secundară rujeolei. Ulcerele pot apărea ca puncte albe pe partea din față a ochiului și sunt de obicei tratate cu antivirale topice sau antibiotice. Când se vindecă, pot lăsa corneea plictisitoare. Cazurile în care virusul rujeolic provoacă retinopatie cu leziuni grave ale retinei sunt rare, dar documentate [89] . Retinita poate provoca pierderea temporară și, în unele cazuri, a vederii permanente. L'infiammazione, non necessariamente conseguente all'encefalite indotta dal morbillo, può attaccare anche il nervo ottico comportando una neurite ottica . I casi acuti possono essere trattati con corticosteroidi. Come per la retinite, la perdita della vista dalla neurite ottica può essere temporanea o permanente. [70] I casi di cecità e gravi complicanze oftalmiche associati al morbillo si concentrano nei Paesi in via di sviluppo dove i programmi di immunizzazione sono carenti e spesso interrotti da conflitti. Fattore aggravante è la malnutrizione, in particolare la carenza di vitamina A . [70]
Altre complicanze
- Morbillo croup : quando si manifesta con laringite e gonfiore delle mucose, associati a raucedine e mancanza di respiro già nei giorni di viremia primaria (2-3).
- Sindrome del morbillo atipico: si verifica solo in persone che hanno ricevuto vaccino inattivato (ucciso) dal morbillo (KMV), non più disponibili dal 1968, e sono successivamente esposti a virus del morbillo di tipo selvaggio. Circa 600 000 - 900 000 persone hanno ricevuto KMV negli Stati Uniti dal 1963 al 1967. KMV sensibilizza il destinatario agli antigeni del virus del morbillo senza fornire un'adeguata protezione. L'infezione successiva con il virus del morbillo porta a segni di poliserositismi di ipersensibilità. La malattia è caratterizzata da febbre, polmonite, effusioni pleuriche ed edema. L'eruzione è generalmente maculopapolare o petecchiale, ma può avere componenti orticariali, purpuri o vescicolari. L'eruzione partirebbe dai polsi o dalle caviglie. Il morbillo atipico può essere prevenuto rivaccinando con vaccino vivo contro il morbillo. Le reazioni locali, moderate o severe, con o senza febbre, possono seguire la rivaccinazione. Queste reazioni sono meno severe di quelle da morbillo. [2] [10]
- La porpora trombocitopenica acuta può manifestarsi nelle sei settimane successive all'infezione e si manifesta con petecchie e/o ecchimosi, anche se occasionalmente possono verificarsi sanguinamenti gravi. [2]
- Il morbillo in gravidanza comporta un rischio più elevato di travaglio prematuro, aborto spontaneo e neonati con basso peso alla nascita. Sono stati riportati difetti di nascita (senza schema definitivo della malformazione), senza conferma che il morbillo ne fosse la causa. [90] [91]
Ulteriori complicanze sono l' appendicite , l' epatite e la linfoadenopatia generalizzata. Molto rare l'infiammazione del muscolo cardiaco ( miocardite ) e la glomerulonefrite .
Diagnosi
La diagnosi clinica del morbillo richiede una storia di febbre da almeno tre giorni accompagnata da almeno tosse, rinite o congiuntivite. L'osservazione delle macchie di Köplik è diagnostica per il morbillo. [66] [92] [93] Un contatto con altri soggetti noti per avere la malattia aggiunge una forte evidenza epidemiologica per la diagnosi. Qualsiasi contatto con una persona infetta, tra cui lo sperma attraverso un rapporto sessuale , la saliva o il muco , può trasmettere l'infezione. [93]
Test di laboratorio
In alternativa, una diagnosi di laboratorio può essere fatta con la conferma della presenza di anticorpi IgM per il morbillo o l'isolamento del virus a RNA del morbillo dai campioni respiratori. [94] Quando non è possibile prelevare il sangue, può essere raccolta la saliva per test sulle IgA specifiche per il morbillo. [95]
Diagnosi differenziale
La diagnosi differenziale si pone soprattutto per la scarlattina , rosolia e sesta malattia . Nella sesta malattia il rash morbilliforme, che dura uno o due giorni, parte dal torace e raggiunge il viso solo successivamente. La rosolia di solito si manifesta con febbre moderata e debole, rash non confluenti sul collo e sul petto. Tipico è anche un gonfiore dei linfonodi del collo. Nella scarlattina il rash finemente screziato è più scarlatto e inizia nella regione inguinale o nelle ascelle e risale da lì alla testa, dove si concentra nell'area bocca-mento. Tipica è anche la cosiddetta lingua a fragola e una faringite (mal di gola).
In aggiunta a queste malattie si possono valutare anche: malattia di Kawasaki , mononucleosi , toxoplasmosi , infezioni da micoplasmi e reazioni allergiche. Queste malattie possono essere escluse rilevando gli anticorpi specifici. [96]
Trattamento
Non esiste un trattamento specifico per il morbillo. La maggior parte delle persone affette si riprenderà con il riposo e terapia di supporto, se non si verificheranno complicanze. [90] [97] [98] Il trattamento del morbillo è essenzialmente un trattamento di supporto mantenendo una buona idratazione e sostituendo i fluidi persi attraverso diarrea o emesi . La reidratazione intravenosa può essere necessaria se la disidratazione è grave. L'ospedalizzazione è indicata per il trattamento delle complicanze gravi del morbillo (ad esempio superinfezioni batteriche, polmonite, disidratazione, croup). Le sovrainfezioni secondarie (per es. otite media o polmonite batterica) devono essere trattate con antibiotici. I pazienti con gravi infezioni complicanti (per es., encefalomielite) dovrebbero essere ospedalizzati.

La febbre può essere gestita con antipiretici standard. Idonee precauzioni per la diffusione aerea vanno adottate nei giorni in cui la malattia è contagiosa.
Il virus del morbillo, in vitro, è suscettibile ad alcuni antivirali. La ribavirina , intravena o orale, è stata utilizzata per trattare adulti immunocompromessi con complicanze severe del morbillo o con la PESS. Questo trattamento dovrebbe essere considerato sperimentale. [99]
Le immunoglobuline possono impedire o modificare la malattia in soggetti sensibili se somministrate entro sei giorni dall'esposizione. Le immunoglobuline possono essere somministrate a soggetti immunocompromessi, infanti da sei mesi a un anno, neonati di età inferiore ai sei mesi che sono nati da madri senza immunità al morbillo, donne in gravidanza.
L'uso della vitamina A durante il trattamento è raccomandato dall' Organizzazione mondiale della sanità per diminuire il rischio di cecità . [100] Una revisione sistematica di studi per il suo utilizzo non ha trovato significative riduzioni della mortalità complessiva, ma ha ridotto la mortalità nei bambini di età inferiore ai due anni. [101] [102] [103]
Non è chiaro se la supplementazione di zinco nei bambini con il morbillo possa influire sul decorso della malattia. [104]
Prognosi
La prognosi per il morbillo è generalmente buona, con infezioni che solo occasionalmente sono fatali. Il tasso di mortalità infantile da infezione del morbillo nei Paesi avanzati è relativamente basso. Tuttavia possono svilupparsi molte complicazioni e sequele. Il morbillo è tuttora una delle cause principali della cecità infantile nei Paesi in via di sviluppo. Globalmente, il morbillo è ancora, al 2017, una delle principali cause di morte nei bambini piccoli, specie in Africa e Asia. I tassi di mortalità sono più elevati nei bambini di età inferiore ai cinque anni. I tassi di mortalità più elevati sono tra i neonati di età compresa tra quattro e dodici mesi e nei bambini immunocompromessi a causa dell'infezione da virus dell'immunodeficienza umana (HIV) o di altre cause. Le complicanze del morbillo sono più probabili nei soggetti di età inferiore a cinque anni o più di venti anni, e la morbilità e la mortalità sono aumentate in persone con disordini di carenza del deficit immunitario, malnutrizione, carenza di vitamina A e inadeguate vaccinazioni.
- L'epidemia italiana di morbillo del 2002 ha causato, su circa 40 000 bambini malati, più di 600 ricoveri ospedalieri, quindici encefaliti e sei decessi [105] [106] .
- L'epidemia in Bulgaria del 2009-2011 ha causato, su 24.364 casi, 19.167 ricoveri ospedalieri registrando 4.704 polmoniti, 3.206 diarrea, 15 encefaliti acute, 21 otiti, 123 polmoniti con diarrea, 5 polmoniti con encefalite e 24 decessi (19 polmoniti, 5 encefaliti). [107]
- L'epidemia in Francia del 2008-2011 ha causato, su oltre 20 000 malati, circa 5 000 ricoveri ospedalieri, 1.023 polmoniti gravi, 27 encefalomieliti e 10 decessi. [108]
- L'epidemia nelle Filippine, nel 2014, ha registrato 57.564 casi e 110 decessi. [109]
Prevenzione
Nel 2000 l' Assemblea Generale delle Nazioni Unite ha adottato l'obiettivo 4 del Millennio per la riduzione della mortalità infantile di due terzi entro il 2015, con la copertura vaccinale contro il morbillo come uno degli indicatori del progresso verso tale obiettivo. Nel 2010 l' Assemblea mondiale della sanità (WHA) ha stabilito tre traguardi per il controllo del morbillo entro il 2015: (1) una maggiore copertura con la prima dose di vaccino per bambini di età di 1 anno ( ≥90% a livello nazionale e ≥80 % in ogni distretto); (2) riduzione dell'incidenza annuale del morbillo annuale a <5 casi per milione di abitanti; (3) la riduzione della mortalità sul morbillo globale del 95% rispetto alla stima del 2000. Nel 2012 il WHA ha approvato il piano d'azione globale contro il morbillo con l'obiettivo di eliminare il morbillo in 4 regioni dell'OMS entro il 2015. Gli Stati membri in tutte 6 le regioni dell'OMS hanno adottato obiettivi di eliminazione del morbillo con piani nazionali di immunizzazione. [36]
Nei paesi sviluppati, con un basso tasso di trasmissione del morbillo, i bambini vengono immunizzati contro il morbillo ad una età di 12 mesi, in genere come parte del vaccino MPR (morbillo, parotite e rosolia ). La vaccinazione non viene somministrata prima di questa età, poiché i bambini più piccoli non rispondono adeguatamente al vaccino a causa di un sistema immunitario immaturo. [63] Ai neonati gli anticorpi anti-morbillo vengono trasferiti dalle madri che sono state vaccinate contro il morbillo o che sono state precedentemente infettate dal virus. [63] Tuttavia, questi anticorpi vengono trasferiti in basse quantità e conferiscono una immunità parziale che dopo 6 mesi dalla nascita gradualmente scompare. [12] [63] Pertanto i bambini sotto un anno di età, i cui anticorpi anti-morbillo materni sono scomparsi, diventano sensibili alla infezione e possono sviluppare episodi lievi e brevi di morbillo che conferiscono poi piena immunità. [12] [63] [100] La presenza di anticorpi materni nel neonato è la causa più comune della inefficacia della vaccinazione primaria. L'età della prima immunizzazione con il vaccino del morbillo deve equilibrare la probabilità di sieroconversione con il rischio di infezione. Questo è il motivo per cui, nei paesi in via di sviluppo , in cui il morbillo è altamente endemico , la prima dose di vaccino contenente il morbillo (MCV) viene somministrata già da nove mesi, spesso seguita da un'altra dose un anno dopo. [12] Nei paesi dove la copertura vaccinale è già sufficientemente alta una seconda dose di vaccino viene solitamente somministrata ad un'età compresa tra i quattro ei cinque anni. È stato dimostrato che sono necessarie due dosi di vaccino contro il morbillo per interrompere la trasmissione indigena e ottenere l' immunità di gregge . Una dose singola nel secondo anno di vita indurrebbe l'immunità in circa il 95% delle persone immunizzate. Ciò significa che sarebbe necessario, per raggiungere il livello di immunità desiderato al 95%, vaccinare il 100% della popolazione suscettibile. Visto che circa il 95% di coloro che non rispondono ad una prima dose sviluppano l'immunità ad una seconda dose, si rende necessario per raggiungere l'immunità di gregge al morbillo una vaccinazione generalizzata con 2 dosi. I tassi di vaccinazione sono stati sufficientemente elevati da rendere il morbillo relativamente raro. Le reazioni avverse alla vaccinazione sono altrettanto rare, con febbre e dolore nel sito di iniezione le più frequenti. Le reazioni avverse potenzialmente letali si verificano in meno di un caso per milione di vaccinazioni (<0,0001%). [110]
Il vaccino risulta meno efficace nei bambini con infezione da HIV rispetto alla popolazione generale [111] , ma il trattamento precoce con farmaci antiretrovirali può aumentare la sua efficacia. [112]
Stato della ricerca
Nel mese di maggio 2015, sulla rivista Science , è stato pubblicato un rapporto in cui i ricercatori hanno scoperto che l'infezione di morbillo può lasciare nella popolazione un maggior rischio di mortalità da altre malattie per 2 o 3 anni. [113] [114]
Un trattamento specifico per il morbillo, tramite il farmaco sperimentale ERDRP-0519, ha mostrato risultati promettenti in studi su animali, ma non è ancora stato testato negli esseri umani. [115] [116] [117]
Note
- ^ morbillo in Vocabolario - Treccani , su www.treccani.it . URL consultato il 3 dicembre 2018 .
- ^ a b c d e f g Caserta, MT (a cura di), Measles , su Merck Manual Professional , Merck Sharp & Dohme Corp., settembre 2013. URL consultato il 23 marzo 2014 .
- ^ Measles (Red Measles, Rubeola) , su Dept of Health, Saskatchewan . URL consultato il 10 febbraio 2015 (archiviato dall' url originale il 10 febbraio 2015) .
- ^ a b c d Morbillo , su www.epicentro.iss.it . URL consultato il 25 aprile 2017 .
- ^ a b Semba RD, Bloem MW., Measles blindness , in Surv Ophthalmol. , vol. 49, n. 2, 2004, pp. 243-55.
- ^ a b Cohen BE, Durstenfeld A, Roehm PC, Viral Causes of Hearing Loss: A Review for Hearing Health Professionals , in Trends in Hearing , 2014.
- ^ a b Measles (Rubeola) Signs and Symptoms , su cdc.gov , 3 novembre 2014. URL consultato il 5 febbraio 2015 .
- ^ a b c d e f g h i j k l Measles Fact sheet N°286 , su who.int , novembre 2014. URL consultato il 4 febbraio 2015 .
- ^ a b Conn's Current Therapy 2015: Expert Consult - Online , Elsevier Health Sciences, 2014, p. 153, ISBN 978-0-323-31956-0 .
- ^ a b c d e f g h i j k William Atkinson, Epidemiology and Prevention of Vaccine-Preventable Diseases , 12ª ed., Public Health Foundation, 2011, pp. 301-323, ISBN 978-0-9832631-3-5 . URL consultato il 25 aprile 2017 .
- ^ John A. Marx, Rosen's emergency medicine : concepts and clinical practice , 7th, Philadelphia, Mosby/Elsevier, 2010, p. 1541, ISBN 978-0-323-05472-0 .
- ^ a b c d e f g Measles, factsheet , su ecdc.europa.eu , European Centre for Disease Prevention and Control (ECDC). URL consultato il 25 aprile 2017 .
- ^ a b SK Kabra e R Lodhra, Antibiotics for preventing complications in children with measles , in Cochrane Database of Systematic Reviews , vol. 8, 14 agosto 2013, pp. CD001477, DOI : 10.1002/14651858.CD001477.pub4 , PMID 23943263 .
- ^ Collaborators GBD 2013 Mortality and Causes of Death,Global, regional, and national age-sex specific all-cause and cause-specific mortality for 240 causes of death, 1990-2013: a systematic analysis for the Global Burden of Disease Study 2013. , in Lancet , vol. 385, 17 dicembre 2014, pp. 117-171, DOI : 10.1016/S0140-6736(14)61682-2 , PMC 4340604 , PMID 25530442 .
- ^ " Maurice R. Hilleman Dies; Created Vaccines ". The Washington Post . April 13, 2005.
- ^ a b Yuki Furuse, Akira Suzuki e Hitoshi Oshitani, Origin of measles virus: divergence from rinderpest virus between the 11th and 12th centuries , in Virology Journal , vol. 7, 4 marzo 2010, p. 52, DOI : 10.1186/1743-422X-7-52 , ISSN 1743-422X , PMC 2838858 , PMID 20202190 . URL consultato il 14 settembre 2014 .
- ^ Cohen SG, Measles and immunomodulation , in The Journal of allergy and clinical immunology , vol. 121, n. 2, febbraio 2008, pp. 543-4, DOI : 10.1016/j.jaci.2007.12.1152 , PMID 18269930 .
- ^ Francis L. Black, Measles endemicity in insular populations: Critical community size and its evolutionary implication , in Journal of Theoretical Biology , vol. 11, n. 2, luglio 1966, pp. 207-211, DOI : 10.1016/0022-5193(66)90161-5 , ISSN 0022-5193 , PMID 5965486 . URL consultato il 15 ottobre 2014 .
- ^ Joseph Patrick Byrne, Encyclopedia of Pestilence, Pandemics, and Plagues: A–M , ABC-CLIO, 2008, p. 413, ISBN 0-313-34102-8 .
- ^ Torrey EF and Yolken RH. 2005. Their bugs are worse than their bite. Washington Post, April 3, p. B01. , su birdflubook.com . URL consultato il 27 febbraio 2016 (archiviato dall' url originale il 28 aprile 2013) .
- ^ Migration and Disease . Digital History.
- ^ Fiji School of Medicine Archiviato il 10 aprile 2015 in Internet Archive .
- ^ a b c d Ludlow M, McQuaid S, Milner D, de Swart RL, Duprex WP, Pathological consequences of systemic measles virus infection , in The Journal of pathology , vol. 235, n. 2, gennaio 2015, pp. 253-65, DOI : 10.1002/path.4457 , PMID 25294240 .
- ^ Live attenuated measles vaccine , in EPI Newsletter / C Expanded Program on Immunization in the Americas , vol. 2, n. 1, 1980, p. 6, PMID 12314356 .
- ^ Rima BK, Earle JA, Yeo RP, Herlihy L, Baczko K, ter Meulen V, Carabaña J, Caballero M, Celma ML, Fernandez-Muñoz R, Temporal and geographical distribution of measles virus genotypes [ collegamento interrotto ] , in The Journal of General Virology , vol. 76, n. 5, 1995, pp. 1173-80, DOI : 10.1099/0022-1317-76-5-1173 , PMID 7730801 .
- ^ Offit PA, Vaccinated: One Man's Quest to Defeat the World's Deadliest Diseases , Washington, DC, Smithsonian, 2007, ISBN 0-06-122796-X .
- ^ " Measles Prevention: Recommendations of the Immunization Practices Advisory Committee (ACIP) ". Centers for Disease Control and Prevention (CDC).
- ^ Measles: Questions and Answers, Immunization Action Coalition .
- ^ WHO vaccine-preventable diseases: monitoring system 2016 global summary: serie storiche, file .xls [ collegamento interrotto ]
- ^ Africa (Regione WHO)=Algeria, Angola, Benin, Botswana, Burkina Faso, Burundi, Camerun, Capo Verde, Repubblica Centrafricana, Ciad, Comore, Congo, Costa d'Avorio, Repubblica Democratica del Congo, Guinea Equatoriale, Eritrea, Ghana, Guinea, Guinea-Bissau, Kenya, Lesotho, Liberia, Madagascar, Malawi, Mali, Mauritania, Maurizius, Mozambico, Namibia, Nigeria, Ruanda, Sao Tome e Principe, Senegal, Seychelles, Sierra Leone, Sud Africa, Sud Sudan, Swaziland, Togo, Uganda, Repubblica di Tanzania, Zambia, Zimbabwe
- ^ Americhe (regione WHO)=Antigua e Barbuda, Argentina, Bahamas, Barbados, Belize, Bolivia, Brasile, Canada, Cile, Colombia, Costa Rica, Cuba, Dominica, Repubblica Dominicana, Ecuador, El Salvador, Grenada, Guatemala, Guyana, Haiti, Honduras, Giamaica, Messico, Nicaragua, Panama, Paraguay, Perù, Saint Kitts e Nevis, Saint Lucia, Saint Vincent e Grenadine, Suriname, Trinidad e Tobago, Stati Uniti d'America, Uruguay, Venezuela
- ^ Medio oriente(regione WHO)=Afghanistan, Bahrein, Djibouti, Egitto, Iran, Iraq, Giordania, Kuwait, Libano, Libia, Marocco, Oman, Pakistan, Qatar, Arabia Saudita, Somalia, Sudan, Siria, Arabia Saudita, Tunisia, Emirati, Yemen
- ^ Europa (regione WHO)=Albania, Andorra, Armenia, Austria, Azerbaigian, Bielorussia, Belgio, Bosnia-Erzegovina, Bulgaria, Croazia, Cipro, Repubblica ceca, Danimarca, Estonia, Finlandia, Francia, Georgia, Germania, Grecia, Ungheria, Islanda, Irlanda, Israele, Kazakistan, Kirghizistan, Lettonia, Lituania, Lussemburgo, Malta, Monaco, Montenegro, Paesi Bassi, Norvegia, Polonia, Portogallo, Repubblica di Moldova, Regno Unito, Romania, Federazione Russa, San Marino, Serbia, Slovacchia, Slovenia, Spagna, Svezia, Svizzera, Tajikistan, Macedonia, Turchia, Turkmenistan, Ucraina, Uzbekistan
- ^ Sud est asiatico (regione WHO)=Bangladesh, Bhutan, Corea del sud, India, Indonesia, Maldive, Myanmar, Nepal, Sri Lanka, Thailandia, Timor-Leste
- ^ Pacifico occidentale (regione WHO)=Brunei Darussalam, Cambogia, Cina, Corea del nord, Laos, Malesia, Isole Marshall, Micronesia, Mongolia, Nauru, Niue, Palau, Papua Nuova Guinea, Filippine, Samoa, Singapore, Isole Salomone, Tonga, Tuvalu, Vanuatu, Vietnam
- ^ a b c d Minal K. Patel, Marta Gacic-Dobo, Peter M. Strebel, Alya Dabbagh, Mick N. Mulders, Jean-Marie Okwo-Bele, Laure Dumolard, Paul A. Rota, Katrina Kretsinger, James L. Goodson, Progress towards regional measles elimination –worldwide, 2000–2015 , in Weekly epidemiological record , vol. 91, n. 45, WORLD HEALTH ORGANIZATION, 11 novembre 2016, pp. 525-536. URL consultato il 25 aprile 2017 .
- ^ MS Bartlett, Measles periodicity and community size , in J. Roy. Stat. Soc. , Ser. A, n. 120, 1957, pp. 48-70.
- ^ Black FL, Measles endemicity in insular populations; critical community size and its evolutionary implications , in Journal of Theoretical Biology , vol. 11, n. 2, 1966, pp. 207-11, DOI : 10.1016/0022-5193(66)90161-5 , PMID 5965486 .
- ^ a b c Measles, factsheet , su who.int , WHO, marzo 2017. URL consultato il 25 aprile 2017 .
- ^ Complications of measles , su cdc.gov , CDC, 3 novembre 2014. URL consultato il 7 novembre 2014 .
- ^ E. Colzani,SA McDonald,P. Carrillo-Santisteve,MC Busana,P. Lopalco,A. Cassini, Impact of measles national vaccination coverage on burden of measles across 29 Member States of the European Union and European Economic Area, 2006–2011 , in Vaccine , Elsevier, 1º aprile 2014, DOI : 10.1016/j.vaccine.2014.01.094 .
- ^ Canada -Measles and Rubella Elimination Working Group (MREWG) - GUIDELINES FOR THE PREVENTION AND CONTROL OF MEASLES OUTBREAKS IN CANADA -2013
- ^ Antonietta Filia, Antonino Bella, Martina del Manso, Cristina Rota – Istituto superiore di sanità, Morbillo: Aspetti epidemiologici , su epicentro.iss.it .
- ^ Epicentro: Copertura vaccinale in Italia
- ^ Bộ Y tế: "VN đã phản ứng rất nhanh đối với dịch sởi" , su tuoitre.vn (archiviato dall' url originale il 31 maggio 2014) .
- ^ Vietnam minister calls for calm in face of 8,500 measles cases, 114 fatalities | Health | Thanh Nien Daily , su thanhniennews.com . URL consultato il 19 aprile 2014 .
- ^ Mark Papania, Elimination of Endemic Measles, Rubella, and Congenital Rubella Syndrome From the Western Hemisphere The US Experience , in JAMA Pediatrics , Feb 2014.
- ^ CDC: Measles data and statistic – 27 aprile 2016
- ^ Measles kills first patient in 12 years , USA Today, 2 luglio 2015. URL consultato il 2 luglio 2015 .
- ^ First Measles Death in US Since 2003 Highlights the Unknown Vulnerables – Phenomena: Germination , su phenomena.nationalgeographic.com . URL consultato il 3 luglio 2015 .
- ^ Robert Koch Institut: Epidemiologisches Bulletin – 2 febbraio 2015, n.5
- ^ Robert Koch Institut: Epidemiologisches Bulletin – 2 dicembre 2013, n.48
- ^ Epicentro: Morbillo in Italia: bollettino settimanale – 19 aprile 2017
- ^ comunicato per i viaggiatori CDC: Measles in Italy, aprile 2017
- ^ Ansa:Usa, Italia entra in 'viaggi a rischio' per il morbillo. Esperti Cdc consigliano cautela ad americani nel Belpaese - 18 aprile 2017
- ^ a b Perry RT, Halsey NA, The Clinical Significance of Measles: A Review , in The Journal of Infectious Diseases , vol. 189, S1, 1º maggio 2004, pp. S4–16, DOI : 10.1086/377712 , PMID 15106083 .
- ^ Sension MG, Quinn TC, Markowitz LE, Linnan MJ, Jones TS, Francis HL, Nzilambi N, Duma MN, Ryder RW, Measles in hospitalized African children with human immunodeficiency virus , in American Journal of Diseases of Children (1960) , vol. 142, n. 12, 1988, pp. 1271-2, DOI : 10.1001/archpedi.1988.02150120025021 , PMID 3195521 .
- ^ a b c d e f Chen SSP, Measles , su emedicine.medscape.com , Medscape, 3 ottobre 2011.
- ^ National Institutes of Health Office of Dietary Supplements, Vitamin A , su ods.od.nih.gov , US Department of Health & Human Services, 2013. URL consultato l'11 marzo 2015 .
- ^ Enders JF, Peebles TC, Propagation in tissue culture of cytopathogenic agents from patients with measles , in Proceedings of the Society for Experimental Biology and Medicine. Society for Experimental Biology and Medicine (New York, NY) , vol. 86, n. 2, 1954, pp. 277-86, DOI : 10.3181/00379727-86-21073 , PMID 13177653 .
- ^ Gowda VK, Sukanya V, Acquired Immunodeficiency Syndrome with Subacute Sclerosing Panencephalitis , in Pediatric Neurology , vol. 47, n. 5, 2012, pp. 379-381, DOI : 10.1016/j.pediatrneurol.2012.06.020 , PMID 23044024 .
- ^ Waggoner JJ, Soda EA, Deresinski S, Rare and emerging viral infections in transplant recipients , in Clinical Infectious Diseases , vol. 57, n. 8, ottobre 2013, pp. 1182-8, DOI : 10.1093/cid/cit456 , PMID 23839998 .
- ^ a b c d e Leuridan E, Sabbe M, Van Damme P, Measles outbreak in Europe: susceptibility of infants too young to be immunized , in Vaccine , vol. 30, n. 41, settembre 2012, pp. 5905-13, DOI : 10.1016/j.vaccine.2012.07.035 , PMID 22841972 .
- ^ Noyce RS, Richardson CD, Nectin 4 is the epithelial cell receptor for measles virus , in Trends in Microbiology , vol. 20, n. 9, settembre 2012, pp. 429-39, DOI : 10.1016/j.tim.2012.05.006 , PMID 22721863 .
- ^ a b Biesbroeck L, Sidbury R, Viral exanthems: an update , in Dermatologic therapy , vol. 26, n. 6, novembre 2013, pp. 433-8, DOI : 10.1111/dth.12107 , PMID 24552405 .
- ^ a b Baxby D,<71::AID-RMV185>3.0.CO;2-S Classic Paper: Henry Koplik. The diagnosis of the invasion of measles from a study of the exanthema as it appears on the buccal membrane , in Reviews in Medical Virology , vol. 7, n. 2, 1997, pp. 71-4, DOI : 10.1002/(SICI)1099-1654(199707)7:2<71::AID-RMV185>3.0.CO;2-S , PMID 10398471 .
- ^ NHS UK: Symptoms of measles. Last reviewed: 26/01/2010 .
- ^ WT Gardiner, Otitis Media in Measles , in The Journal of Laryngology & Otology , vol. 39, n. 11, 2007, pp. 614-617, DOI : 10.1017/S0022215100026712 .
- ^ Fisher DL, Defres S, Solomon T, Measles-induced encephalitis , in QJM , vol. 108, 2014, pp. 177-182, DOI : 10.1093/qjmed/hcu113 , PMID 24865261 . URL consultato il 27 agosto 2014 .
- ^ a b c d Shirley Dang, Six Ways Measles Can Affect the Eyes , 5 marzo 2015.
- ^ Sabella C, Measles: Not just a childhood rash , in Cleveland Clinic Journal of Medicine , vol. 77, n. 3, 2010, pp. 207-213, DOI : 10.3949/ccjm.77a.09123 , PMID 20200172 .
- ^ JB Ellison, Pneumonia in Measles , su 1931 Archives of Disease in Childhood , vol. 6, n. 31, 1931, pp. 37-52, PMC 1975146 .
- ^ H Yano e al.,Isolation of Measles Virus From Middle Ear Fluid of Infants With Acute Otitis Media , in J Infect , vol. 51, n. 4, 2005, pp. 237-240.
- ^ R.Suboti, Histopathological findings in the inner ear caused by measles , in The Journal of Laryngology & Otology , vol. 90, n. 2, 1976, pp. 173-181.
- ^ Renee Buchanan , Daniel J. Bonthius, Measles Virus and Associated Central Nervous System Sequelae , in Seminars in Pediatric Neurology , vol. 19, n. 3, pp. 107-114.
- ^ Warning of rise in meningitis cases from measles outbreak in England and Wales , su meningitis.org .
- ^ Patterson CE, Daley JK, Echols LA, Lane TE, Rall GF, Measles virus infection induces chemokine synthesis by neurons , in J Immunol , vol. 171, 2003, pp. 3102-9.
- ^ a b DL Fisher, S. Defres, T. Solomon; Measles-induced encephalitis, QJM , vol. 108, n. 3, 2015, pp. 177-182, https://academic.oup.com/qjmed/article-lookup/doi/10.1093/qjmed/hcu113 .
- ^ "NINDS Subacute Sclerosing Panencephalitis Information Page"
- ^ a b Subacute Sclerosing Panencephalitis:the Devastating Measles Complication is More Common than We Think
- ^ a b Schönberger K, Ludwig MS, Wildner M, Weissbrich B., Epidemiology of Subacute Sclerosing Panencephalitis (SSPE) in Germany from 2003 to 2009: A Risk Estimation. , in PLoS ONE , 2013.
- ^ Robert Koch Institute Berlin: Bollettino epidemiologico, dicembre 2013
- ^ Bellini WJ, Rota JS, Lowe LE, Katz RS, Dyken PR, Zaki SR, Shieh WJ, Rota PA, Subacute sclerosing panencephalitis: more cases of this fatal disease are prevented by measles immunization than was previously recognized. , in The Journal of Infectious Diseases , vol. 192, n. 10, 2005, pp. 1686-1693, DOI : 10.1086/497169 , PMID 16235165 . URL consultato il 27 aprile 2017 .
- ^ Hardie DR, Albertyn C, Heckmann JM, Smuts HE, Molecular characterisation of virus in the brains of patients with measles inclusion body encephalitis (MIBE) , in Virology Journal. , 2013.
- ^ Mustafa MM, Weitman SD, Winick NJ, Bellini WJ, Timmons CF, Siegel JD, Subacute measles encephalitis in the young immunocompromised host: report of two cases diagnosed by polymerase chain reaction and treated with ribavirin and review of the literature , in Clin Infect Dis. , vol. 10, 1993, pp. 654-60.
- ^ Budka H, Urbanits S, Liberski PP, Eichinger S, Popow-Kraupp T., Subacute measles virus encephalitis: a new and fatal opportunistic infection in a patient with AIDS. , in Neurology. , vol. 10, 1996, pp. 586-587.
- ^ Ari Bitnun, Patrick Shannon, Andrew Durward, Paul A. Rota, William J. Bellini, Caroline Graham, Elaine Wang, Elizabeth L. Ford-Jones, Peter Cox, Laurence Becker, Measles Inclusion-Body Encephalitis Caused by the Vaccine Strain of Measles Virus , in Clin Infect Dis , vol. 29, n. 4, 1999, pp. 855-861.
- ^ WHO: Immunizing the immunocompromised [ collegamento interrotto ]
- ^ M. HALTIA, A. TARKKANEN, A. VAHERI, A.PAETAU, K. KAAKINEN, AND H. ERKKILA, Measles retinopathy during immunosuppression ( PDF ), in British Journal of Oplthalmology , vol. 62, 1978, pp. 356-360.
- ^ a b Measles exposure during pregnancy- guidelines ( PDF ), su hpsc.ie . URL consultato il 30 aprile 2017 (archiviato dall' url originale il 30 ottobre 2017) .
- ^ Chiba ME, Saito M, Suzuki N, Honda Y, Yaegashi N., Measles infection in pregnancy , in J Infect. , 2003.
- ^ a b Total Health, Actual Confirmed Measles Cases in UK , in totalhealth , 5 maggio 2010. URL consultato il 4 maggio 2013 .
- ^ Durrheim DN, Kelly H, Ferson MJ, Featherstone D, Remaining measles challenges in Australia , in The Medical journal of Australia , vol. 187, n. 3, agosto 2007, pp. 181-4, PMID 17680748 .
- ^ Friedman M, Hadari I, Goldstein V, Sarov I, Virus-specific secretory IgA antibodies as a means of rapid diagnosis of measles and mumps infection , in Israel Journal of Medical Sciences , vol. 19, n. 10, 1983, pp. 881-884, PMID 6662670 .
- ^ Differential Diagnosis of Typical Measles ( PDF ), su calhospitalprepare.org .
- ^ Treating measles in children ( PDF ), WHO, 2004.
- ^ Selina SP Chen, Glenn Fennelly, Russell W Steele, Measles Treatment & Management , su Medscape , 2016.
- ^ Hosoya M; Shigeta S; Mori S; Tomoda A; Shiraishi S; Miike T; Suzuki H, High-dose intravenous ribavirin therapy for subacute sclerosing panencephalitis. , in Antimicrob Agents Chemother. , vol. 45, n. 3, 2001, pp. 943-5, ISSN 0066-4804 .
- ^ a b Measles vaccines: WHO position paper. ( PDF ), in Weekly epidemiological record , vol. 84, n. 35, 28 agosto 2009, pp. 349-60, PMID 19714924 .
- ^ Huiming Y, Chaomin W, Meng M, Vitamin A for treating measles in children , in The Cochrane Database of Systematic Reviews , n. 4, 2005, pp. CD001479, DOI : 10.1002/14651858.CD001479.pub3 , PMID 16235283 .
- ^ D'Souza RM, D'Souza R, Vitamin A for treating measles in children , in The Cochrane Database of Systematic Reviews , n. 1, 2002, pp. CD001479, DOI : 10.1002/14651858.CD001479 , PMID 11869601 .
- ^ D'Souza RM, D'Souza R, Vitamin A for preventing secondary infections in children with measles—a systematic review , in Journal of Tropical Pediatrics , vol. 48, n. 2, aprile 2002, pp. 72-7, DOI : 10.1093/tropej/48.2.72 , PMID 12022432 .
- ^ AA Awotiwon, O Oduwole, A Sinha e CI Okwundu, Zinc supplementation for the treatment of measles in children. , in The Cochrane database of systematic reviews , vol. 3, 20 marzo 2015, pp. CD011177, DOI : 10.1002/14651858.CD011177.pub2 , PMID 25794053 .
- ^ Morbillo , in archive.is , 13 aprile 2013. URL consultato il 31 luglio 2017 (archiviato dall' url originale il 13 aprile 2013) .
- ^ Morbillo - VaccinarSì , su VaccinarSì . URL consultato il 31 luglio 2017 .
- ^ The measles outbreak in Bulgaria, 2009–2011: An epidemiological assessment and lessons learnt
- ^ Measles Elimination Efforts and 2008–2011 Outbreak, France
- ^ Philippines measles outbreak 2014: 58,010 cases, 110 deaths
- ^ Galindo BM, Concepción D, Galindo MA, Pérez A, Saiz J, Vaccine-related adverse events in Cuban children, 1999–2008 , in MEDICC Review , vol. 14, n. 1, 2012, pp. 38-43, PMID 22334111 .
- ^ Helfand RF, Witte D, Fowlkes A, Garcia P, Yang C, Fudzulani R, Walls L, Bae S, Strebel P, Broadhead R, Bellini WJ, Cutts F, Evaluation of the immune response to a 2-dose measles vaccination schedule administered at 6 and 9 months of age to HIV-infected and HIV-uninfected children in Malawi , in The Journal of Infectious Diseases , vol. 198, n. 10, 2008, pp. 1457-65, DOI : 10.1086/592756 , PMID 18828743 .
- ^ UNICEF, Global goal to reduce measles deaths in children surpassed , su Joint press release , 2007. URL consultato l'11 marzo 2015 .
- ^ Nicholas Bakalar, Measles May Increase Susceptibility to Other Infections , su The New York Times , The New York Times Company. URL consultato il 7 giugno 2015 .
- ^ Mina, Long-term measles-induced immunomodulation increases overall childhood infectious disease mortality , in Science , vol. 348, n. 6235, 8 maggio 2015, pp. 694-699, DOI : 10.1126/science.aaa3662 . URL consultato il 7 giugno 2015 .
- ^ White LK, Yoon JJ, Lee JK, Sun A, Du Y, Fu H, Snyder JP, Plemper RK,Nonnucleoside Inhibitor of Measles Virus RNA-Dependent RNA Polymerase Complex Activity , in Antimicrobial Agents and Chemotherapy , vol. 51, n. 7, 2007, pp. 2293-303, DOI : 10.1128/AAC.00289-07 , PMC 1913224 , PMID 17470652 .
- ^ Krumm SA, Yan D, Hovingh ES, Evers TJ, Enkirch T, Reddy GP, Sun A, Saindane MT, Arrendale RF, Painter G, Liotta DC, Natchus MG, von Messling V, Plemper RK, An Orally Available, Small-Molecule Polymerase Inhibitor Shows Efficacy Against a Lethal Morbillivirus Infection in a Large Animal Model , in Science Translational Medicine , vol. 6, n. 232, 2014, pp. 232ra52, DOI : 10.1126/scitranslmed.3008517 , PMID 24739760 .
- ^ Will an anti-viral drug put paid to measles? New Scientist 16 April 2014
Voci correlate
Altri progetti
-
 Wikiquote contiene citazioni di o su morbillo
Wikiquote contiene citazioni di o su morbillo -
 Wikizionario contiene il lemma di dizionario « morbillo »
Wikizionario contiene il lemma di dizionario « morbillo » -
 Wikimedia Commons contiene immagini o altri file su morbillo
Wikimedia Commons contiene immagini o altri file su morbillo
Collegamenti esterni
- ( EN ) Morbillo , su Enciclopedia Britannica , Encyclopædia Britannica, Inc.
| Controllo di autorità | Thesaurus BNCF 42991 · LCCN ( EN ) sh85082696 · GND ( DE ) 4120705-1 · BNF ( FR ) cb12260072w (data) · NDL ( EN , JA ) 00562991 |
|---|