Tomografie cu emisie de pozitroni
| Tomografie cu emisie de pozitroni | |
|---|---|
Procedura medicala 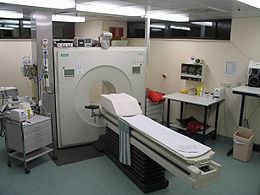 Un echipament tipic PET | |
| Tip | Diagnostic nuclear-medical |
| Anestezie | Nu |
| Clasificare și resurse externe | |
| ICD - 9 | 92.0 |
| Plasă | D049268 |
| MedlinePlus | 003827 |
| Sinonime | |
| ANIMAL DE COMPANIE | |
Tomografie de emisie de pozitroni (PET -ul sau, de la " engleza tomografie cu emisie de pozitroni) este o tehnică de diagnostic medical de medicina nucleara utilizate pentru producerea de bio-imagini (imagini ale corpului).
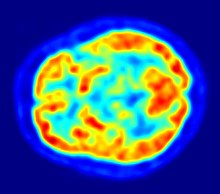
Spre deosebire de tomografia computerizată (CT) și rezonanța magnetică nucleară (RMN), care oferă informații morfologice, PET oferă informații fiziologice care permit obținerea hărților proceselor funcționale din corp .
Această analiză instrumentală este utilizată pentru:
- studiul patologiilor neoplazice ;
- diagnostic diferențial al demențelor și studii de neuroimagistică funcțională;
- boli ale bolilor reumatologice și infecțioase;
- cercetarea studiilor de miocard hibernant și perfuzie cardiacă.
Descriere

Procedura începe cu „ injectarea unui produs radiofarmaceutic format dintr-un trasor de izotop radio cu timp de înjumătățire scurt, legat chimic de o moleculă activă la nivel metabolic (vector), de exemplu, fluorodeoxiglucoză ( 18 F-FDG ). După un timp de așteptare, timp în care molecula activă din punct de vedere metabolic (adesea un zahăr ) atinge o anumită concentrație în țesuturile organice de analizat, subiectul este poziționat în scaner. Izotopul de scurtă durată se descompune, emitând un pozitron . După o cale care poate atinge maximum câțiva milimetri, [1] pozitronul se anihilează cu un electron , [2] producând o pereche de fotoni gamma ambii cu energie de 511 keV emiși în direcții opuse (fotoni „înapoi în spate”) .
Acești fotoni sunt detectați atunci când ajung la un scintilator în dispozitivul de scanare, unde creează un fulger de lumină, detectat prin tuburi fotomultiplicatoare . Punctul crucial al tehnicii este detectarea simultană a perechilor de fotoni: fotonii care nu ajung la detector în perechi, adică într-un interval de timp de câteva nanosecunde, nu sunt luați în considerare. Din măsurarea poziției în care fotonii lovesc detectorul, este posibilă reconstituirea poziției ipotetice a corpului din care au fost emiși, permițând determinarea activității sau a utilizării chimice în părțile corpului investigate.
Cele mai recente modele de tomografe de pe piață pot îmbunătăți rezoluția spațială și contrastul imaginilor utilizând corecția pentru timpul de zbor ( Time of Flight sau TOF în engleză) în timpul reconstrucției lor. Această corecție ia în considerare care dintre cei doi fotoni de coincidență interacționează mai întâi cu detectoarele de tomograf și, prin urmare, este capabil să localizeze punctul de anihilare a pozitronului mai precis.
Cea mai recentă inovație tehnologică privind tomografele este reprezentată de PET digital. Aceste mașini permit achiziționarea de imagini de o calitate mai bună (atât în ceea ce privește rezoluția spațială, cât și contrastul), administrând pacientului mai puțină activitate radiofarmaceutică și reducând timpii de achiziție. Aceste mașini noi utilizează fotodioduri și fotomultiplicatori de siliciu pentru a detecta fotonii gamma produși prin anihilarea pozitronilor în locul combinației clasice de cristale și fotomultiplicatori, permițând o conversie directă a energiei fotonice într-un semnal electric [3] .
Densitatea izotopului din corp este apoi arătată operatorului, sub formă de imagini ale secțiunilor (în general transversale) separate de aproximativ 5 mm. Harta rezultată reprezintă țesuturile în care molecula eșantionului este cea mai concentrată și este citită și interpretată de un specialist în medicina nucleară pentru a determina un diagnostic și un tratament ulterior.
Radionuclizii utilizați în scanarea PET sunt în general izotopi cu un timp de înjumătățire scurt, cum ar fi 11 C (~ 20 min), 13 N (~ 10 min), 15 O (~ 2 min) și în special 18 F (~ 110 min) . Datorită timpului de înjumătățire redus, radioizotopii trebuie să fie produși de un ciclotron poziționat în imediata apropiere a scanerului PET. Acești radionuclizi sunt încorporați în compuși în mod normal asimilați de corpul uman, cum ar fi glucoza, apa sau amoniacul, și apoi injectați în corp pentru a fi analizați pentru a urmări locurile în care sunt distribuiți. Compușii astfel marcați se numesc radiotracere sau radiofarmaceutice.
Evaluarea semicantitativă a absorbției regionale

Evaluarea zonelor hipercaptive pe imagini se face de obicei într-un mod calitativ de către medici experți; cu toate acestea, există cazuri îndoielnice în care o analiză semicantitativă poate fi utilă. Principalul parametru utilizat în acest sens este SUV-ul (Standardized Uptake Value), care poate fi calculat pe fiecare zonă dubioasă folosind următoarea formulă:
Acest raport arată de câte ori zona afectată captează mai mult (sau mai puțin) decât ar captura o zonă cu masă egală. Calculul SUV-ului poate fi apoi corectat în continuare pentru alți parametri, cum ar fi suprafața corpului sau masa slabă. De obicei, cea mai mare valoare a SUV detectată la nivelul leziunilor studiate (SUVmax) este utilizată în evaluări. Alte modele mai precise se bazează pe analiza cineticii absorbției, detectată prin achiziții seriale și măsurători ale grupului circulant.
Multe studii care evaluează răspunsul la terapiile citostatice utilizează măsurători seriale ale SUV-ului în mai multe scanări în timp asupra leziunilor pentru a cuantifica succesul tratamentelor. Acest lucru se datorează faptului că PET are o rezoluție spațială minimă a unui cub cu o latură de 5 mm și, prin urmare, permite o evaluare excelentă (chiar dacă nu garantează dispariția bolii sub această valoare) care vine să facă estimări pe un singur gram de tesut. De regulă, ca criteriu, considerăm reducerea procentuală a valorii între diferitele măsurători, care evident trebuie să fie cât se poate de similară în ceea ce privește activitatea administrată, timpul de achiziție a imaginii din momentul injectării și specificațiile tehnice ale scanării în sine.
În studiul limfomului Hodgkin și al limfoamelor non-Hodgkin (inclusiv limfomul folicular ) care măresc FDG-ul avid, utilizarea criteriilor Deauville pentru evaluarea răspunsului la tratamente este acum frecventă. Aceste criterii se bazează pe compararea SUVmax a leziunilor patologice cu cea detectată la nivelul ficatului și a aortei . Un scor de 4 sau 5 indică lipsa de răspuns la tratamente / progresie [4] .
| Scorul Deauville | Limită SUVmax |
|---|---|
| 1 | Leziune neabsorbantă |
| 2 | Leziunea SUVmax <= SUVmax aortică |
| 3 | SUVmax aortic <leziune SUVmax <= SUVmax hepatic |
| 4 | Leziunea SUVmax> ficatul SUVmax |
| 5 | Leziunea SUVmax> de 2-3 ori SUVmaxul ficatului sau apariția unor noi locuri de boală |
Alte criterii propuse pentru evaluarea răspunsului la terapie sunt PERCIST (Criterii de răspuns în tomografia cu emisie de pozitroni în tumora solidă). În utilizarea acestor criterii, SULpeak (SUV corectat pentru masa slabă) este utilizat ca variabilă, care se măsoară pe cele mai semnificative 5 leziuni ale examenului (maxim 2 pe organ) și cu dimensiuni măsurabile (cel puțin 2 centimetri). Boala este apoi ameliorată folosind criteriile descrise mai jos.
| Evaluarea PERCIST | Descriere |
|---|---|
| Răspuns metabolic complet | Dispariția tuturor leziunilor cu SULpeak> 2,5 |
| Răspunsul metabolic parțial | Reducerea activității metabolice cu cel puțin 30% ( media valorilor tuturor leziunilor măsurabile) și cu cel puțin 0,8 unități de SUL |
| Progresia bolii metabolice | Creșterea activității metabolice de cel puțin 30% (media valorilor tuturor leziunilor măsurabile), creșterea absolută de cel puțin 0,8 unități de SUL, creșterea vizibilă a extensiei bolii, apariția unor leziuni noi |
| Boală metabolică stabilă | Toate condițiile nu sunt incluse în tabelele de mai sus |
În ultimii ani, au fost dezvoltate metode care au ca scop cuantificarea neomogenității leziunilor tumorale; aceste metode se bazează pe analiza texturii și au fost utilizate inițial în radiologie. Adesea, leziunile care prezintă o absorbție radiofarmaceutică mai neomogenă sunt mai agresive datorită prezenței mai mari a necrozei sau a diferitelor clone celulare în interiorul acestora, dovadă fiind corelarea acestor parametri cu datele genetice, moleculare și histologice ( Radiomică și Radiogenomică ).
Principalul defect al parametrilor semicantitativi detectabili în PET este standardizarea slabă. Numeroși factori, care nu sunt întotdeauna controlați, afectează de fapt rezultatele (modelul tomografului, parametrii de achiziție etc.)
Aplicații
PET este utilizat pe scară largă în oncologia clinică [5] (pentru a avea reprezentări ale tumorilor și pentru a căuta metastaze) și în cercetarea cardiologică și neurologică. Metodele alternative de investigație sunt tomografia computerizată cu raze X (CT), imagistica prin rezonanță magnetică (RMN), imagistica prin rezonanță magnetică funcțională (RMF) și tomografia computerizată cu emisie de fotoni unici și ultrasunete.
Cu toate acestea, în timp ce alte metode de scanare, cum ar fi CT și RMN, permit identificarea modificărilor organice și anatomice din corpul uman, scanările PET sunt capabile să detecteze modificări la nivel biologic molecular care adesea preced alterarea anatomică, prin utilizarea markerilor moleculari. care au o rată de absorbție diferită în funcție de țesutul implicat. Cu o scanare PET este posibilă vizualizarea și cuantificarea modificării fluxului sanguin în diferitele structuri anatomice cu o precizie rezonabilă (prin măsurarea concentrației emițătorului de pozitroni injectat).
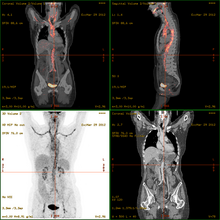
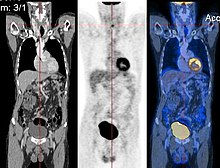
Adesea, și din ce în ce mai frecvent, scanările cu tomografie cu emisie de pozitroni sunt comparate cu scanările cu tomografie computerizată, oferind atât informații anatomice, cât și morfologice și metabolice (în esență, despre modul în care țesutul sau organul este modelat și despre ceea ce fac). Pentru a depăși dificultățile tehnice și logistice care rezultă din mutarea pacientului pentru efectuarea celor două examinări și a inexactităților consecvente, folosim acum exclusiv tomografe PET-CT, în care sistemul de detectare PET și un tomograf CT de ultimă generație sunt asamblate într-un singur portic și controlat de o singură consolă de comandă. Introducerea tomografului PET-CT a permis o mare îmbunătățire a preciziei și interpretabilității imaginilor și o reducere considerabilă a timpilor de examinare.
PET joacă un rol din ce în ce mai mare în verificarea răspunsului la terapie, în special în terapiile anti-cancer. [5]
PET este, de asemenea, utilizat în studii preclinice pe animale, [6] unde sunt permise investigații repetate pe același subiect. Aceste cercetări s-au dovedit deosebit de valoroase în cercetarea cancerului, unde există o creștere a calității statistice a datelor și o reducere substanțială a numărului de animale necesare pentru fiecare studiu individual.
O limitare la difuzia PET este costul ciclotronilor pentru producerea radionuclizilor de înjumătățire scurtă. Puține spitale și universități își pot permite cumpărarea și întreținerea acestor echipamente scumpe și, prin urmare, majoritatea centrelor PET sunt furnizate de furnizori externi. Această constrângere limitează utilizarea PET-ului clinic în principal la utilizarea de trasoare marcate cu 18 F, care având un timp de înjumătățire de 110 minute poate fi transportat la o distanță rezonabilă înainte de a fi utilizat. De asemenea, 68 Ga (care poate fi obținut datorită unui generator) permite obținerea mai ușor de urmărire, în timp ce 82 Rb este uneori utilizat pentru studiul alimentării cu sânge a miocardului.
Utilizarea PET în neurologie
PET-ul cerebral cu FDG permite evaluarea metabolismului glucozei din creier și este utilizat în diagnosticul demențelor și în evaluarea afectării cognitive ușoare (MCI Mild Cognitive Defairment ).
Prin intermediul altor produse radiofarmaceutice este posibilă, de asemenea, realizarea de imagini ale neurotransmisiei (în special a sistemului dopaminergic . Acest subiect este tratat pe larg în intrarea relevantă ) sau vizează căutarea depozitelor și a plăcilor de beta amiloid în boala Alzheimer suspectată.
Urmări specifice sunt, de asemenea, studiate pentru proteina Tau (o substanță adesea asociată cu multe boli neurodegenerative).
Utilizarea PET în cardiologie
Tomografia cu emisie de pozitroni este o metodă utilizată în studiul inimii ( PET cardiac ). Folosind acest tip de imagistică este de fapt posibil să se efectueze atât studii de perfuzie (folosind amoniac marcat cu azot -13, apă marcată cu oxigen -15 sau rubidiu -82), cât și metabolism (folosind fludeoxiglucoză ). Studiile de perfuzie fac posibilă localizarea zonelor inimii în care există o lipsă de perfuzie în urma, de exemplu, a fenomenelor de arterioscleroză (cu o precizie mai mare decât scintigrafia miocardică de perfuzie), în timp ce studiul metabolismului este util pentru cercetarea miocardului vital. Pentru această din urmă indicație, PET este considerat metoda standard de aur .
Utilizarea PET în reumatologie, imunologie și boli infecțioase
PET cu FDG este utilizat pe scară largă în studiul acestor patologii. În special pentru:
- sarcoidoză
- osteomielita scheletului apendicular
- osteomielita vertebrală și spondilodiscita
- căutarea focarelor infecțioase la pacienții cu febră de origine necunoscută sau cu bacteremie cu risc crescut de infecții metastatice
- vasculita marilor vase
- evaluarea chisturilor hepatice sau renale potențial infectate
- infecție suspectată a dispozitivelor intravasculare ( stimulatoare cardiace și catetere)
- infecții asociate cu SIDA sau boala Castleman
- evaluarea leziunilor tuberculoase
Utilizarea PET în oncologie



PET-ul în oncologie are următoarele indicații:
- stadializare și restabilire la sfârșitul terapiei;
- monitorizarea terapiilor antineoplazice;
- diagnostic diferențial între leziunile benigne sau maligne;
- căutarea tumorilor primare oculte (tumori care s-au metastazat deja, dar care au o origine necunoscută);
- căutați cel mai bun loc al unei leziuni din care să efectuați o biopsie ;
- caracterizarea metabolică a leziunilor neoplazice;
- planificarea tratamentelor de radioterapie .
Există multe trasoare care pot fi utilizate în oncologie, dar cel mai frecvent este fludeoxiglucoza 18, adică glucoza care în poziția 2, în loc de hidroxil , are un atom de fluor 18 care emite pozitron. Acest medicament este, de obicei, preluat într-o măsură mai mare de țesuturile neoplazice, deoarece acestea sunt metabolice mai active (celulele neoplazice pot avea un metabolism de până la 200 de ori mai mare decât cele normale), în principal datorită faptului că principala lor cale metabolică pentru susținerea energiei este anaerobă glicoliză .
PET (cu colină) este, de asemenea, utilizat ca alternativă la scintigrafia paratiroidiană pentru detectarea glandelor paratiroide hipertrofice sau adenoamelor paratiroide la pacienții cu hiperparatiroidism .
Riscuri
Scanarea nu este invazivă, dar implică expunerea la radiații ionizante . Doza totală de radiație este semnificativă, de obicei în jur de 5-7 m Sv (milli-sievert). Cu toate acestea, în practica modernă, se utilizează aproape întotdeauna o scanare combinată PET / CT, iar pentru o scanare PET / CT, expunerea la radiații poate fi substanțial în jur de 23-26 mSv (pentru o persoană de 70 kg, doza este mai mare pentru corpurile mai grele ). [7] Comparativ cu nivelul de clasificare pentru lucrătorii în domeniul radiațiilor din Marea Britanie de 6 m Sv , trebuie concluzionat că utilizarea PET necesită o justificare mai mult decât suficientă. Acest lucru poate fi, de asemenea, comparat cu radiația medie anuală de fond de 2,2 mSv în Marea Britanie, 0,02 mSv pentru o radiografie toracică și 6,5-8 mSv pentru o scanare toracică, potrivit revistei Chest și ICRP. [8] Pe de altă parte, conform asociației IFALPA din 1999, s-a declarat că un operator de zbor va primi o doză de radiații de 4-9 mSv pe an. [9]
Notă
- ^ Michael E. Phelps, PET: fizică, instrumentare și scanere , Springer, 2006, pp. 8-10.
- ^ PET Imaging , la medcyclopaedia.com , GE Healthcare.
- ^ https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5612735/
- ^ AA.VV., Fundamentals of Nuclear Medicine , Springer, p. 768-771.
- ^ a b Young H, Baum R, Cremerius U și colab. , Măsurarea răspunsului tumoral clinic și subclinic folosind [18F] -fluorodeoxiglucoză și tomografie cu emisie de pozitroni: revizuire și recomandări EORTC din 1999. , în Jurnalul European al Cancerului , vol. 35, nr. 13, 1999, pp. 1773-1782, DOI : 10.1016 / S0959-8049 (99) 00229-4 , PMID 10673991 .
- ^ Rat Conscious Animal PET Arhivat 5 martie 2012 la Internet Archive .
- ^ Brix G, Lechel U, Glatting G și colab. , Expunerea la radiații a pacienților supuși examenului PET / CT 18F-FDG cu modalitate duală a întregului corp , în J. Nucl. Med. , Vol. 46, nr. 4, aprilie 2005, pp. 608-13, PMID 15809483 .
- ^ de Jong PA, Tiddens HA, Lequin MH, Robinson TE, Brody AS, Estimarea dozei de radiații de la CT în fibroza chistică , în Chest , vol. 133, nr. 5, mai 2008, pp. 1289–91; răspuns autor 1290-1, DOI : 10.1378 / chest.07-2840 , PMID 18460535 .
- ^ Expunerea la radiația echipajului aerian - O imagine de ansamblu Arhivat 12 iunie 2011 la Internet Archive ., Susan Bailey, Nuclear News (o publicație a American Nuclear Society ), ianuarie 2000.
Bibliografie
- Maurizio Dondi și Raffaele Giubbini, Medicina nucleară în practica clinică , 2003, ISBN 88-555-2728-2 .
- Duccio Volterrani, Paola Anna Erba și Giuliano Mariano, Fundamentele medicinei nucleare. Tehnici și aplicații , Springer Verlag , 2010, ISBN 9788847016842 .
- ( EN ) Francesco Signorelli și Domenico Chirchiglia, FDG-PET Imaging in Neurodegenerative Brain Boals, ISBN 978-953-51-1160-3 , 19 iunie 2013
Elemente conexe
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere despre tomografia cu emisie de pozitroni
Wikimedia Commons conține imagini sau alte fișiere despre tomografia cu emisie de pozitroni
linkuri externe
- ( EN ) Tomografie cu emisie de pozitroni , în Encyclopedia Britannica , Encyclopædia Britannica, Inc.
- Liniile directoare ale regiunii Emilia Romagna pentru utilizarea adecvată a PET FDG în oncologie.
- Prezentare la Congresul Național AIMN (Asociația Italiană de Medicină Nucleară) Rimini 2015 privind cuantificarea cu FDG PET a răspunsului la terapii în oncologie
- (RO) PET Textură Analiza opinie
- ( EN ) Liniile directoare ale Asociației Europene de Medicină Nucleară (EAMN) privind utilizarea PET FDG în studiul infecțiilor și inflamațiilor.
- Atlasul imagistic al PET-CT , pe med.harvard.edu .
- Informații despre medicina nucleară , la nucmedinfo.com .
- Introducere în fizica PET , la depts.washington.edu . Adus la 4 mai 2019 (arhivat din original la 24 februarie 2019) .
- GE HealthCare , Philips , Siemens - mari producători de scanere PET
- Informații despre Centrul de cercetare pentru supraviețuirea cancerului Thompson pe PET , la thompsonpet.com . Adus la 21 ianuarie 2006 (arhivat din original la 26 decembrie 2005) .
- Ce este PET-ul? , pe radiologyinfo.org .
| Controllo di autorità | Thesaurus BNCF 54010 · LCCN ( EN ) sh85135956 · GND ( DE ) 4129799-4 |
|---|