Paraquat
| Paraquat | |
|---|---|
| Numele IUPAC | |
| Diclorură de 1-1'-dimetil-4-4'-bipiridiniu | |
| Abrevieri | |
| AH501 PP148 | |
| Denumiri alternative | |
| Diclorură de paraquat Diclorură de metil viologen Metil viologen | |
| Caracteristici generale | |
| Formula moleculară sau brută | CH3 (C 5 H 4 N) 2 CH 3 Cl 2 |
| Masa moleculară ( u ) | 257,16 |
| Aspect | cristale albe care tind spre galben: în soluție devine roșu închis |
| numar CAS | |
| Numărul EINECS | 217-615-7 |
| PubChem | 15938 |
| ZÂMBETE | C[N+]1=CC=C(C=C1)C2=CC=[N+](C=C2)C.[Cl-].[Cl-] |
| Proprietăți fizico-chimice | |
| Densitate (g / cm 3 , în cs ) | 1,25 |
| Solubilitate în apă | 700 g / L (20 ° C) |
| Temperatură de topire | 175-180 ° C (448,15 - 453,15 K) |
| Temperatura de fierbere | 300 ° C (573,15 K) descompunere |
| Presiunea de vapori ( Pa ) la 293,15 K. | <10 −4 |
| Proprietăți toxicologice | |
| LD 50 (mg / kg) | 196 (oral, șoareci) |
| Informații de siguranță | |
| TLV (ppm) | 4,75 x 10 −2 |
| Simboluri de pericol chimic | |
   | |
| Fraze H | 372 - 319 - 315 - 330 - 301 - 311 -345 - 410 |
| Sfaturi P | 261 - 273 - 305 + 351 + 338 - 314 - 501 [1] [2] |
Paraquat , denumirea comercială a diclorurii de N, N '-dimetil-4,4'-bipiridiniu , este un erbicid erbicid cu acțiune desicantă, neselectivă, utilizat la prepararea paturilor de semințe sau la transplant, în rândul între culturi copaci, în terasamente, drenuri, margini de drum etc. De asemenea, este utilizat ca liant în SERS .
Intoxicația cu paraquat poate duce la insuficiență respiratorie acută ( ARDS ).
Studii recente au confirmat că acest produs poate duce, în populația care locuiește în zone adiacente terenului tratat, la o creștere a riscului de apariție a bolii Parkinson măsurabilă între 75% și 80%. Având în vedere pericolul dovedit, Uniunea Europeană și-a interzis comercializarea și utilizarea pe teritoriul UE. Produsul este încă produs în Europa pentru exportul către SUA și alte piețe unde nu există încă nici o interdicție de utilizare a acestuia (Sursa sondajului New York Times).
Utilizare
Acționează rapid asupra părților verzi, în timp ce nu prezintă nicio acțiune asupra părților lemnoase. Poate fi folosit în orice moment al anului, are nevoie doar de lumină și oxigen pentru a-și desfășura acțiunea. Nu se recomandă utilizarea acestuia dacă se așteaptă ploi după câteva ore. Produsul este toxic pentru insectele benefice, animale , pești și animale. Nu prezintă acțiune reziduală, deoarece este absorbit rapid de coloizii solului și rapid inactivat.
Pe piață se găsește atât în preparate unice, cât și într-un amestec cu alte erbicide ( diquat ).
Mecanism de acțiune
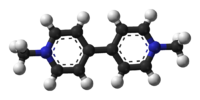
Pesticidul are o structură specială, cu două inele de piridină legate între ele și fiecare are o grupare metil pe azot. Această configurație are o sarcină pozitivă asupra azotului. Paraquat își exprimă acțiunea la nivelul lanțului de transport al electronilor de la PSI (sistemul fotosintetic I) la ciclul Calvin . Sistemul de transport al electronilor se bazează pe diferența de potențial a speciilor chimice prezente. Paraquat se inserează în acest lanț, luând electroni și folosindu-i pentru a transforma oxigenul atmosferic (prezent în concentrații mari datorită ciclului de fotosinteză ) în ion superoxid (O 2 - ) sau peroxid de hidrogen (H 2 OR 2 ). Acești compuși sunt deosebit de periculoși în interiorul celulei, deoarece acționează asupra legăturilor duble ale pigmenților (degradează clorofilele , carotenoizii și alți pigmenți; este cauza „albirii” plantei), dar mai ales asupra acizilor grași ai membrana, care este degradată cu pierderea consecventă de apă și alte substanțe din celulă.
Indicator Redox
În chimia analitică, cea mai frecventă utilizare a paraquatului este ca indicator în reacțiile redox , dată fiind culoarea sa albastră într-un mediu reducător care se transformă în incolor într-un mediu oxidant. Are un coeficient de dispariție molar de 13700 M -1 cm -1 la o lungime de undă de 606 nm [3] .
Notă
- ^ Sigma Aldrich; rev. din 23.12.2011
- ^ Aruncați la o instalație autorizată de eliminare a deșeurilor
- ^ Tadashi Watanabe, Kenichi Honda, Măsurarea coeficientului de extincție al radicalului de cation metil viologen și a eficienței formării acestuia prin fotocataliză semiconductoare , în The Journal of Physical Chemistry , vol. 86, nr. 14, 1982, pp. 2617-2619, DOI : 10.1021 / j100211a014 , ISSN 0022-3654 .
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere pe diclorură de paraquat
Wikimedia Commons conține imagini sau alte fișiere pe diclorură de paraquat
| Controlul autorității | LCCN (EN) sh85097905 · GND (DE) 4275370-3 |
|---|