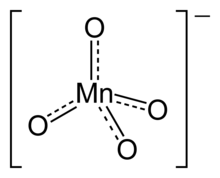
Permanganat
Permanganatul este un oxoanion de mangan cu formula MnO - 4 .
Manganul are o stare de oxidare de +7 și este izoelectronic cu cromat . Compușii săi sunt oxidanți puternici.
Sinteză
Permanganatele pot fi produse prin oxidarea compușilor de mangan cu agenți oxidanți puternici, cum ar fi hipocloritul , dioxidul de plumb , bismutul :
- 2MnCl 2 + 5NaClO + 6NaOH → 2NaMnO 4 + 9NaCl + 3H 2 O
- 2MnSO 4 + 5PbO 2 + 3H 2 SO 4 → 2HMnO 4 + 5PbSO 4 + 2H 2 O
sau, mai puțin eficient, prin dismutarea manganatelor:
- 3Na 2 MnO 4 + 2H 2 O → 2NaMnO 4 + MnO 2 + 4NaOH
Productie industriala
Este sintetizat din minerale care conțin dioxid.
Primele două oxidări se fac prin prăjire: la Mn (V) și Mn (VI). În prima etapă se folosește un amestec de potasiu mineral și caustic , la temperaturi cuprinse între 390 și 420 ° C :
- 4MnO 2 + 12KOH + O 2 → 4K 3 MnO 4 + 3H 2 O
Apoi la temperaturi cuprinse între 180 și 330 ° C și mai lent:
- 4K 3 MnO 4 + 2H 2 O + O 2 → 2K 2 MnO 4 + 4KOH
Ultima oxidare are loc electrochimic .
Reactivitate
Este un oxidant puternic, similar cu percloratul . Poate distruge complet compușii organici .
În soluție acidă , permanganatul este redus la starea de oxidare incoloră +2 a ionului Mn 2+ . E 0 = 1,51 V.
- 16H 3 O + + 2MnO - 4 + 10Cl - → 2Mn 2+ + 5Cl 2 + 24 H 2 O
- 6H + + 2MnO - 4 + 5H 2 C 2 O 4 → 8H 2 O + 2Mn 2+ + 5CO 2
Într-o soluție puternic bazică , permanganatul este redus la starea de oxidare +6, verde, a ionului manganat (MnO 2− 4 ).
- 3OH - + 2MnO - 4 + HSO - 3 → 2MnO 2− 4 + SO 2− 4 + 2 H 2 O
Într-un mediu slab bazic sau neutru cu dioxid de mangan (MnO 2 ), E 0 = 1,23 V.
- 4OH - + 2MnO - 4 + 3 C 2 O 2− 4 → 2MnO 2 + 6CO 2− 3 + 2 H 2 O
În mediul acidului fosforic , se formează Mn (III).
Permanganatele nu sunt stabile termic. De exemplu, permanganatul de potasiu se descompune la 230 ° C:
- 2KMnO 4 → K 2 MnO 4 + MnO 2 + O 2
Prin reducerea cu sulfit dă hipomanganat (MnO 3− 4 ).
Pregătirea soluțiilor
Permanganatul reacționează cu multe impurități care pot fi prezente în apa utilizată pentru prepararea soluției , în special substanțe organice. De asemenea, se descompune în prezența dioxidului solid:
- 4MnO - + 2H 2 O → 4MnO 2 + 3O 2 + 4OH -
și cu Mn 2+ :
- 2MnO - + 3Mn 2+ + 2H 2 O → 5MnO 2 + 4H +
Prin urmare, soluțiile proaspăt preparate trebuie fierte timp de o oră și filtrate pe vată de sticlă sau sept poros.
Compuși
Printre cei mai utilizați compuși:
- Permanganat de potasiu , KMnO 4
- Sodiu permanganat , NaMnO 4
Bibliografie
- NN Greenwood și A. Earnshaw, Chimia elementelor , II, Piccin, ISBN 88-299-1121-6 .
- W. Büchner, R. Schliebs, G. Winter și KH Büchel, Chimie anorganică industrială , Piccin, ISBN 88-299-1348-0 .
Elemente conexe
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere pe permanganat
Wikimedia Commons conține imagini sau alte fișiere pe permanganat
linkuri externe
- ( EN ) Inventarul Național al Poluanților - Fișă informativă despre mangan și compuși , pe npi.gov.au. Adus la 26 iunie 2007 (arhivat din original la 1 martie 2006) .