Fold Rossmann
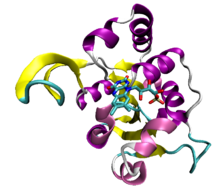
Pliul Rossmann este un domeniu structural proteic al proteinelor care leagă nucleotidele , în special cofactorul NAD . [1] Structura cu două repetări este compusă din șase β-catene paralele, conectate la două perechi de helice α în ordinea topologică β-α-β-α-β. Deoarece fiecare pli Rossmann poate lega doar o singură nucleotidă, legăturile de domeniu pentru dinucleotide, cum ar fi NAD, constau din două pliuri Rossmann pereche care leagă fiecare o jumătate din nucleotida moleculei cofactorului. Pliurile individuale Rossmann pot lega mononucleotidele β, cum ar fi cofactorul FMN .
Motivul poartă numele lui Michael Rossmann , care a subliniat pentru prima dată că acesta este un motiv frecvent recurent în proteinele care se leagă de nucleotide, cum ar fi dehidrogenaza. [2]
În 1989, Israel Hanukoglu de la Institutul Weizmann a descoperit că secvența de consens pentru situsul de legare NADP în unele enzime care utilizează NADP diferă de motivul de legare NADP. [3] Această descoperire a fost utilizată pentru a re-proiecta specificitățile enzimelor. [4]
Notă
- ^ Hanukoglu I., Proteopedia: Rossmann fold: A beta-alfa-beta fold at dinucleotide binding sites , în Biochem Mol Biol Educ , vol. 43, nr. 3, 2015, pp. 206-209, DOI : 10.1002 / bmb.20849 , PMID 25704928 .
- ^ Rao S., Rossmann M., Comparația structurilor super-secundare în proteine , în J Mol Biol , vol. 76, nr. 2, 1973, pp. 241-56, DOI : 10.1016 / 0022-2836 (73) 90388-4 , PMID 4737475 .
- ^ Hanukoglu I., Gutfinger T., secvența ADNc a adrenodoxin reductazei. Identificarea siturilor de legare a NADP în oxidoreductaze. , în Eur J Biochem , vol. 180, n. 2, mar 1989, pp. 479-484, DOI : 10.1111 / j.1432-1033.1989.tb14671.x , PMID 2924777 .
- ^ Scrutton NS, Berry A., Perham RN, Redesign al specificității coenzimei unei dehidrogenaze prin ingineria proteinelor. , în Nature , vol. 343, nr. 6253, ianuarie 1990, pp. 38-43, DOI : 10.1038 / 343038a0 , PMID 2296288 .


