Oxid de azot
| Oxid de azot | |
|---|---|
| Numele IUPAC | |
| monoxid de dinitrogen | |
| Denumiri alternative | |
| oxid de azot oxidarea azotului oxid de azot anhidridă de hiponitroză gaz ilariant NOS | |
| Caracteristici generale | |
| Formula moleculară sau brută | N 2 O |
| Masa moleculară ( u ) | 44.01 |
| Aspect | gaz incolor |
| numar CAS | |
| Numărul EINECS | 233-032-0 |
| PubChem | 948 |
| DrugBank | DB06690 |
| ZÂMBETE | N#[N+][O-] |
| Proprietăți fizico-chimice | |
| Densitate (g / cm 3 , în cs ) | 1,2 (la 185 K) |
| Solubilitate în apă | 1,5 g / L la 293 K. |
| Temperatură de topire | −91 ° C (182 K) |
| Temperatura de fierbere | −88 ° C (185 K) |
| Punct critic | 309,6 K (36,4 ° C) 7.245 MPa |
| Presiunea de vapori ( Pa ) la 293 K. | 5,08 × 10 6 |
| Proprietăți termochimice | |
| Δ f H 0 (kJ mol −1 ) | 81.6 |
| Δ f G 0 (kJ mol −1 ) | 103,7 |
| S 0 m (J K −1 mol −1 ) | 220.0 |
| C 0 p, m (J K −1 mol −1 ) | 38.6 |
| Date farmacologice | |
| Mod de administrare | inhalare |
| Date farmacocinetice | |
| Jumătate de viață | 5 minute |
| Excreţie | respirator |
| Informații de siguranță | |
| Simboluri de pericol chimic | |
  | |
| Pericol | |
| Fraze H | 270 - 280 |
| Sfaturi P | 220 - 244 - 370 + 376 - 403 [1] |
Oxidul de azot (denumit IUPAC monoxid de dinitrogen , cunoscut sub numele de oxid de azot și mai ales ca oxid de azot ) în condiții standard este un gaz incolor, neinflamabil , cu un miros ușor dulce. Are formula chimică N 2 O.
De asemenea, cunoscut sub numele de gaz de râs [2] datorită efectelor sale euforice și disociative , găsește utilizarea medicală ca analgezic și anestezic și este, de asemenea, un poluant important cu gaze cu efect de seră și aer: conform EPA ( Agenția pentru Protecția Mediului ), potențialul său de încălzire climatică este egal cu 310 sau peste o sută de ani, oxidul de azot are de 310 ori mai mult impact decât dioxidul de carbon pe unitate de masă.
În condiții normale, solubilitatea sa în apă este de aproximativ 0.112 g la 100 g. Nu este toxic prin inhalare, dar poate provoca asfixiere dacă este inhalat în cantități excesive. În formă lichefiată poate provoca arsuri la contact, datorită temperaturii scăzute. Structura sa este un hibrid de rezonanță între două structuri care au ambele o sarcină formală pozitivă a atomului central de azot, în timp ce sarcina negativă este pe celălalt atom de azot sau pe atomul de oxigen.
Istorie
Acest gaz a fost descoperit de Joseph Priestley în 1772 . Douăzeci de ani mai târziu, Humphry Davy a experimentat cu el și cu câțiva prieteni, inclusiv cu poeții Samuel Taylor Coleridge și Robert Southey . El a descoperit că oxidul de azot atenuează considerabil senzația de durere , chiar și atunci când utilizatorul este încă semi-conștient. Astfel, a intrat în uz medical ca anestezic, în special în rândul dentiștilor care au avut dificultăți în a folosi munca unui anestezist și care au considerat convenabil ca pacientul lor să rămână suficient de treaz pentru a putea interpreta orice comandă verbală.
William James descrie efectele oxidului de azot asupra sa [3] , afirmând că la scurt timp după inhalare a existat un fior prelungit de la piept la extremități, sensibilitate vizuală crescută, auz și plăcere, pierderea conexiunii cu lucrurile externe, disociere , o percepția imaginilor legate de cuvinte și o imaginație ferventă și imaginativă. După cum povestește în cartea sa The Varieties of Religious Experience: A Study in Human Nature, James a folosit, de asemenea, oxidul de azot ca un fel de vehicul pentru investigația filosofică și pentru a încerca să acceseze intuiția mistică [4] .
Într-un celebru scurtmetraj din Charlie Chaplin din 1914 , intitulat laughing gas sau Charlot, fals dentist , efectul oxidului de azot este descris în mod comic [5] .
Utilizări
Anestezic
Oxidul de azot este considerat unul dintre medicamentele esențiale de pe lista Organizației Mondiale a Sănătății. [6]
A fost utilizat în stomatologie și chirurgie încă din 1844. [7] În acel moment era inspirat direct de un inhalator format dintr-o pungă din țesut. [8] În prezent , în spitale , gazul este administrat printr - o mașină care ajustează automat doza pe vaporizatorul bazat pe respirații pacientului, cu un raport O-oxigen N 2 din 2: 1. Astăzi, având în vedere proprietățile analgezice relativ slabe în comparație cu compușii noi, este utilizat în terapia medicamentoasă în mod complementar. De fapt, poate produce greață și confuzie persistentă dacă expunerea este prea rapidă sau excesivă. Efectul anestezic al oxidului de azot nu este încă pe deplin înțeles, dar se crede că gazul interacționează cu membranele celulelor nervoase din creier modificând comunicarea intercelulară la nivelul sinapselor . [ neclar ]
Gaz ilariant
Utilizarea recreativă a gazului este cunoscută de la sfârșitul secolului al XVIII-lea. În Marea Britanie a fost folosit în partidele societății burgheze, numite petreceri cu râs. Este încă o substanță psihoactivă utilizată în mod obișnuit pentru efecte disociative și euforice. Conform statisticilor, aproximativ 30% dintre britanici și americani au încercat cel puțin o dată în viață [9], iar în Marea Britanie este al doilea drog recreativ cel mai utilizat după canabis. [10] Cele mai frecvente efecte în utilizarea recreativă includ: ușurința corpului, modificări ale percepțiilor tactile, vizuale și auditive, dezorientare, amețeli, scăderea nivelului de anxietate, simțul umorului crescut, detașarea de sine și de mediul înconjurător. [11] [12]
Utilizarea pe scară largă din ultimele două secole în domeniul medical a determinat un profil de toxicitate scăzută și siguranță dovedită, [9] [12], de asemenea, în uz recreativ ocazional. [9] [10] [13] Cu toate acestea, utilizarea și abuzul frecvente, cronice, cu doze mari pot provoca polineuropatie , degenerare a celulelor nervoase și deficiențe grave de vitamina B12. [14] [15] [16] [17] [18] Mai mult, inhalarea gazului suprimă necesitatea aerului, dacă aportul nu este alternat cu inspirații bogate în oxigen poate duce la asfixie, care a cauzat mai multe decese. de-a lungul anilor. [19] [20]
Propulsor pentru aerosoli
Oxidul de azot este un aditiv alimentar și este utilizat ca agent de propulsie [21] în pachetele de spray pentru smântână . Nu este foarte solubil în apă, dar foarte mult în grăsimi, deci se leagă bine de compusul crem (35% din grăsimile emulsionate, restul este apă). Odată cu presurizarea recipientului, când duza este deschisă, gazul tinde să scape, regasificându-se și creând bule mici formate din lipide . Cantitatea de gaz nu este suficientă pentru a anestezia, dar în cantități mari menține un ușor efect euforic.
Crema spray a fost inventată în 1931 de Charlie Goetz și G. Frederick Smith , student la chimie la Universitatea din Illinois și supraveghetorul său. Au folosit inițial dioxid de carbon , care nu era solubil în grăsimi, dar le făcea acide. Utilizarea oxidului de azot a fost propusă de un dentist local, care îl știa ca un anestezic. Din 1948 , crema de pulverizare a fost comercializată în recipiente de unică folosință sub presiune și încărcată cu oxid de azot de către Reddi-Wip a lui Aaron Lapin .
Combustibil pentru rachete
Oxidul de azot poate fi folosit ca combustibil în motoarele cu rachete. Comparativ cu alți agenți oxidanți, are avantajul de a fi netoxic, stabil la temperatura camerei și relativ ușor de depozitat și transportat în zbor.
Este comburentul la alegere în diferite modele de motoare rachete hibride, hibrid deoarece combustibilul este solid, în timp ce comburentul este lichid sau gazos. A fost adesea utilizat în combinație cu o polibutadienă terminată cu hidroxil .
Motoare de combustie internă
În aplicațiile motorului, oxidul de azot este utilizat ca un combustibil , injectat în conducta de admisie a motorului împreună cu combustibilul vehiculului, cu următoarele rezultate:
- temperaturi mai scăzute ale aerului în admisie (care produc o sarcină densă de admisie);
- creșterea oxigenului conținut în sarcina de aspirație (aerul are un procent de oxigen în greutate de 20,9%);
În cursele cu motor , oxidul de azot, mai cunoscut în acest context ca „oxid de azot” sau pur și simplu NOS, este injectat în carburator sau imediat în amonte de acesta, pentru a crește capacitatea de respirație a motorului. Deși nu este în sine inflamabil, descompunerea la temperaturi ridicate asigură mai mult oxigen decât aerul , permițând motorului să ardă un amestec mai bogat de combustibil . Mai mult, fiind stocat sub formă lichidă, evaporarea acestuia în carburator determină scăderea temperaturii: acest lucru face ca amestecul combustibil-combustibil să fie mai dens și să reducă detonarea. De obicei, este introdus în cilindri cilindrici controlați de o electrovalvă care permite gazului să curgă în amonte de carburator prin activarea unui întrerupător special.
Este ilegal să-l folosiți ca supraîncărcător chimic pentru motoarele auto [22] .
Aceeași tehnică a fost folosită în timpul celui de- al doilea război mondial pentru a crește puterea motoarelor aeronavelor, în special de Luftwaffe , al cărei combustibil a fost cel mai slab mediu - în termeni de octan - cel furnizat forțelor aeriene ale aliaților și pentru a compensa lipsa de oxigen la altitudini mari. [ fără sursă ]
Benzina , la fel ca toți combustibilii, are nevoie de un element combustibil pentru a arde: oxigen, alimentat în mod normal de aer . În timp ce adăugarea unui turbo se numește „ supraîncărcare mecanică ”, cea a oxidului de azot se numește „ supraîncărcare chimică ”. Prin adăugarea oxigenului provenit din oxidul de azot în aer (și, prin urmare, creșterea debitului de combustibil), este posibil să se obțină o putere considerabil mai mare decât utilizarea aerului singur. Supraîncărcarea chimică crește performanța unui vehicul de producție în limitele solicitărilor mecanice și termice pe care le poate suporta motorul, în mod normal în ordinea de 40% -45% (exemplu: de la 100 CP ar merge la 140/150 CP). Pentru un vehicul conceput pentru performanțe foarte ridicate, puteți ajunge la o creștere de 150% (de exemplu: de la 100 CP ar ajunge până la 250 CP).
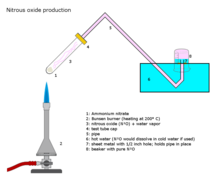
Producție
Cea mai obișnuită modalitate de sinteză a oxidului de dinitrogen constă în încălzirea atentă a azotatului de amoniu , care se descompune în oxid de dinitrogen și vapori de apă [23] .
În aceste condiții, azotatul de amoniu se descompune și prin alte căi, prin urmare gazul obținut va conține alți oxizi de azot. Adăugarea fosfaților permite obținerea unui gaz de puritate puțin mai mare și funcționarea la temperaturi mai scăzute.
Reacția are loc la temperaturi cuprinse între 170 ° C și 240 ° C, temperaturi la care azotatul de amoniu este un exploziv moderat sensibil și un oxidant puternic. Peste 240 ° C, reacția poate accelera și produce o detonație dezastruoasă, de aceea este necesar să avem întotdeauna temperatura reacției sub control. Unele uzine chimice folosesc abur supraîncălzit ca sursă de căldură. [24]
Amestecul de gaze produs prin descompunere este coroziv; este răcit pentru a condensa vaporii de apă și filtrat pentru a elimina oxizii de azot mai mari și orice antrenare de azotat de amoniu. În cele din urmă, este purificat făcându-l balon în trei soluții: bazic, acid și din nou bazic.
Impuritățile monoxidului de azot (NO) sunt chelate prin reacție cu sulfat feros sau oxidate și ulterior absorbite în spălarea bazică. Spălarea acidă intermediară servește la captarea amoniacului care poate fi eliberat prin reacția antrenării azotatului de amoniu cu prima spălare bazică.
Unul dintre primii producători industriali de oxid de azot a fost George Poe din Trenton, New Jersey . [25]
Curiozitate
- În cinematografia recentă, oxidul de azot este menționat în seria Fast and Furious , o faimoasă reproducere a cursei clandestine din SUA, denumindu-l NOS, adică sistemul de oxid de azot, care nu trebuie confundat cu NO 2 sau dioxid de mono-azot, fiind în realitate acesta din urmă este un produs de evacuare al arderii la temperaturi ridicate, așa cum se întâmplă în general în motoarele cu ardere internă.
- În cel de-al cincilea sezon al seriei de televiziune Nip / Tuck , oxidul de azot este folosit de noul partener al lui Sean McNamara , Teddy Rowe, pentru a amplifica intensitatea orgasmului .
- În filmul The Little Shop of Horrors , sadicul și violentul doctor Orin Scrivello ( Steve Martin ) moare din cauza unei supradoze de oxid de azot, din cauza ruperii unei supape în masca pe care a proiectat-o pentru a inhala gazul menționat anterior.
- În primul sezon al emisiunii CHIPS din episodul The Breakdown Man , în timpul unui accident, Ponch intră în contact cu un cilindru cu oxid de azot care scapă, făcându-l euforic și compromitându-și performanțele pe drum.
- În seria de jocuri video Need For Speed , jucătorul poate monta cilindri nitro. Această îmbunătățire se numește N2O.
- În al patrulea episod al celui de-al doilea sezon al Academiei Umbrela , numărul 1 îl folosește cu un alt personaj pentru a depăși un moment de tristețe.
- În cel de-al 80-lea episod al celui de-al doilea sezon al The Dalton , frații Dalton folosesc gazul de pe Melvin Peabody pentru a-l face dependent în timp ce scapă și ulterior câinele Rantanplan provoacă explozia buteliilor de gaz, provocând o euforie în masă în tot penitenciarul. Asistenta medicală specifică apoi numele gazului.
Notă
- ^ foaie informativă cu oxid nitric pe IFA-GESTIS Arhivat 16 octombrie 2019 la Arhiva Internet .
- ^(EN) Thermopedia, „Oxid de azot”
- ^ Efectele subiective ale oxidului de azot. William James. , pe des.emory.edu , Universitatea Emory. Adus la 1 octombrie 2010 .
- ^ Stefano Canali, Halucinogene și intuiție mistică. William James and the Laughing Gas Case - PSYCHOACTIVE , în PSYCHOACTIVE , 14 august 2017. Adus 14 august 2017 .
- ^ Laughing Gas , la imdb.com , Internet Movie Database. Adus la 1 octombrie 2010 .
- ^ Xavier Seuba, O abordare a drepturilor omului la Lista model a medicamentelor esențiale OMS , în Buletinul Organizației Mondiale a Sănătății , vol. 84, nr. 5, 1 mai 2006, pp. 405-411, DOI : 10.2471 / blt.04.019133 . Adus pe 21 noiembrie 2018 .
- ^ Sneader, Walter., Drug discovery: a history , Wiley, 2005, ISBN 0471899798 ,OCLC 57682419 . Adus pe 21 noiembrie 2018 .
- ^ Miller AH (1941). „Dezvoltarea tehnică a anesteziei gazoase”. Jurnalul de anestezie. 2 (4): 398-409. doi: 10.1097 / 00000542-194107000-00004. Arhivat din original la 19 decembrie 2014 ..
- ^ a b c Stephen J Kaar, Jason Ferris și Jon Waldron, Up: Creșterea abuzului de oxid de azot. Un studiu internațional privind utilizarea contemporană a oxidului de azot , în Journal of Psychopharmacology , vol. 30, n. 4, 24 februarie 2016, pp. 395–401, DOI : 10.1177 / 0269881116632375 . Adus pe 21 noiembrie 2018 .
- ^ a b Jan van Amsterdam, Ton Nabben și Wim van den Brink, Utilizarea oxidului de azot recreativ: Prevalență și riscuri , în Regulatory Toxicology and Pharmacology , vol. 73, nr. 3, 2015-12, pp. 790–796, DOI : 10.1016 / j.yrtph.2015.10.017 . Adus pe 21 noiembrie 2018 .
- ^ psychonautwiki.org , https://psychonautwiki.org/wiki/Nitrous_oxide .
- ^ a b Jay, Mike. "Oxid de azot: utilizare recreativă, reglare și reducerea daunelor." Droguri și alcool astăzi 8.3 (2008): 22-25. .
- ^ Abraini JH, David HN, Lemaire M; David; Lemaire (2005). „Proprietăți potențial neuroprotectoare și terapeutice ale oxidului de azot și ale xenonului”. Analele Academiei de Științe din New York. 1053 (1): 289-300. Cod Bib: 2005NYASA1053..289A. doi: 10.1196 / annals.1344.025. PMID 16179534 . .
- ^ Richardson PG., Neuropatie periferică în urma abuzului de oxid de azot. , în Emerg Med Australas. , vol. 22, n. 1, 2007, pp. 88-90, PMID 20152009 .
- ^ Huang MY, Tsai W, Chang WH., Polineuropatia indusă de oxid de azot la un adolescent. , în Emerg Med J. , vol. 26, n. 3, 2009, p. 186, DOI : 10.1093 / bja / aem280 , PMID 17951609 .
- ^ Renard D, Dutray A, Remy A, Castelnovo G, Labauge P., Degenerarea combinată subacută a măduvei spinării cauzată de anestezia oxidului de azot. , în Neurol Sci. , vol. 30, n. 1, 2009, pp. 75-6, PMID 19169627 .
- ^ Krajewski W, Kucharska M, Pilacik B, Fobker M, Stetkiewicz J, Nofer JR, Wronska-Nofer T., Starea metabolică a vitaminei B12 afectată la lucrătorii din domeniul sănătății expuși profesional la oxid de azot. , în Fr J Anaesth. , vol. 99, nr. 6, 2007, pp. 812-8, DOI : 10.1093 / bja / aem280 , PMID 17951609 .
- ^ Jameson M, Roberts S, Anderson NE, Thompson P., deficit de vitamina B (12) indus de oxid de azot. , în J Clin Neurosci. , vol. 6, nr. 2, 1999, pp. 164-6, PMID 18639144 .
- ^ Scott A. Wagner, Michael A. Clark și David L. Wesche, Asphyxial Deaths from the Recreational Use of Nitrous Oxide , în Journal of Forensic Sciences , vol. 37, n. 4, 1 iulie 1992, pp. 13286J, DOI : 10.1520 / jfs13286j . Adus pe 21 noiembrie 2018 .
- ^ justsayn2o.com , http://justsayn2o.com/nitrous.deaths.html .
- ^ Cremă hilară
- ^ Motoare trucate, adrenalină și pariuri nopțile periculoase ale cursei clandestine - Repubblica.it »Cercetare
- ^ AF Holleman, Wiberg, E., Chimie anorganică , San Diego, Academic Press, 2001, ISBN 0-12-352651-5 .
- ^ Uzină de oxid de azot , pe sanghioverseas.com , Organizația Sanghi (arhivată din original la 27 noiembrie 2013) .
- ^ George Poe is Dead , Washington Post, 3 februarie 1914. Adus pe 29 decembrie 2007 .
«Văr de poet celebru și notat ca om de știință. Inventatorul respiratorului. De asemenea, mai întâi pentru a lichefia oxidului de azot. Cadet la Institutul Militar Virginia în timpul Bătăliei de la Newmarket . Menționat pentru Premiul Nobel pentru realizarea științifică în chimie. Prof. George Poe, un văr al poetului Edgar Allan Poe, cunoscut om de știință și inventator, care fusese menționat pentru premiul Nobel pentru realizarea științifică, fost rezident în Washington, a murit ieri în Norfolk, Virginia, de paralizie generală. Prof. Poe a împlinit șaizeci și opt de ani. " .
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere despre oxid de azot
Wikimedia Commons conține imagini sau alte fișiere despre oxid de azot
linkuri externe
- ( EN ) Oxid de dinitrogen , pe Encyclopedia Britannica , Encyclopædia Britannica, Inc.
- https://psychonautwiki.org/wiki/Nitrous_oxide
- https://www.erowid.org/chemicals/nitrous/nitrous.shtml
- http://justsayn2o.com/
| Controllo di autorità | Thesaurus BNCF 42757 · LCCN ( EN ) sh85092097 · GND ( DE ) 4150244-9 · BNF ( FR ) cb12324380n (data) |
|---|