Tensiune de suprafata
În fizică, tensiunea superficială a unui fluid este tensiunea mecanică de coeziune a particulelor de pe suprafața sa externă. Acesta corespunde microscopic densității de suprafață a energiei de legătură pe interfața dintre un corp continuu și un material de altă natură, de exemplu un solid , un lichid sau un gaz : de aceea nu poate fi asimilat dimensional unui efort intern și din acest motiv în sistemul internațional se măsoară în newtoni pe metru (N / m).
Din punct de vedere termodinamic , poate fi definită ca lucrarea necesară creșterii suprafeței continuumului cu o cantitate unitară. [1] Parașorul este o cantitate care exprimă volumul molar de lichide corectat având în vedere efectul tensiunii superficiale.
Definiție mecanică
La nivel microscopic, lichidele sunt compuse din molecule între care se exprimă forțe, în principal de tip electric, care depind puternic de distanța intermoleculară : când aceasta din urmă este mai mică decât o anumită valoare caracteristică ( ) a tipului de substanță, forța dintre două molecule devine respingătoare. În general, însă, moleculele dintr-un lichid se atrag reciproc, așa cum ne oferă situația normală , iar dispunerea geometrică răspunde la o rată ridicată de simetrie: aceasta duce la apariția anularii - în medie - a forțelor care acționează asupra moleculei specifice; în ceea ce privește, în schimb, moleculele de pe suprafața liberă, simetria nu există și sunt afectate de o forță îndreptată spre interiorul lichidului. Acest rezultat indică faptul că creșterea suprafeței libere nu poate avea loc spontan: pentru o creștere de aceea trebuie efectuată o lucrare de suprafață , definit ca . În ultima expresie, indică tensiunea superficială și depinde de tipul de lichid, de gazul de deasupra suprafeței libere, de solidul sau lichidul cu care este în contact substanța de testat și de temperatura .
Unele valori
Având în vedere lichidele în contact cu aerul cu o temperatură de 20 ° C, tensiunea superficială va fi:
| Material | Tensiunea superficială (N / m) |
|---|---|
| Cascadă | 0,073 |
| Mercur | 0,559 |
| Benzen | 0,029 |
| Ulei de masline | 0,0319 |
Stalagmometru
Pentru a măsura experimental valoarea tensiunii superficiale a unui lichid, se folosește un stalagmometru: acest instrument se bazează pe căderea picăturilor dintr-un tub. Picătura care iese din tub este ținută de tensiunea superficială care acționează asupra liniei , de sine este raza găurii; amintindu-mi că este o forță pe unitate de lungime, forța totală se menține și este verticală. Desprinderea picăturii are loc atunci când a atins o dimensiune astfel încât greutatea sa să fie egală cu forța datorată tensiunii superficiale, adică ; această relație permite măsurarea .
Teoria bulei de săpun
Structura bulei de săpun se datorează echilibrului dintre forțele de presiune implicate și, prin urmare, justificarea dimensiunii bulei este o diferență de presiune între mediul intern și exterior; un studiu aprofundat al acestui fenomen a fost efectuat de Laplace .
Imaginați-vă că doriți să aduceți fasciculul unei bule de săpun din la . Munca realizată de presiunile interne și externe pentru a crește volumul de la la trebuie să fie egală cu munca forței de tensiune superficială pentru a aduce suprafața de la la . Urmează deducțiile matematice:
Din relațiile anterioare deducem ecuația Laplace pentru bulele de săpun:
Dacă balonul era plin, termenul limită în calculul muncii tensiunii superficiale ecuația nu ar trebui deci luată în considerare - în acest caz - ar fi:
Umectabilitate
Atunci când este necesar să se țină seama de ceea ce se află în afara lichidului, nu mai este suficient să se ia în considerare forțele de coeziune, deoarece prezența unui alt corp are o influență asupra valorilor tensiunii, în sensul că moleculele pe care le realizează acțiuni (forțe de aderență ) asupra moleculelor stratului superficial al lichidului. De fapt, din motive destul de similare cu cele indicate mai sus, suprafața solidelor are, de asemenea, tensiuni superficiale, dar din cauza lipsei de mobilitate a suprafeței, aceasta nu este nici direct observabilă, nici măsurabilă cu metode directe.
Atunci când lichidul și solidul intră în contact, prin urmare, datorită interacțiunilor dintre diferitele faze , se stabilește o tensiune interfațială, definită ca energia suplimentară pe unitate de suprafață datorită formării unei interfețe (presupunând și prezența unui gaz) solid / lichid și solid / gaz.
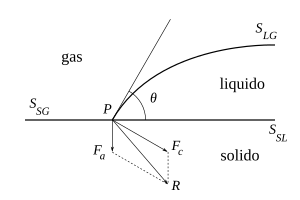
Profilul unei porțiuni de lichid plasat pe o suprafață solidă va forma un unghi cu acesta (vezi figurile) care vor fi mai mari sau mai mici decât unghiul drept, în funcție de care în rezultanta forțelor de coeziune prevalează în modulo, , (normal la tangenta la profilul lichidului în și orientat spre interior), sau rezultatul forțelor de aderență, , (normal față de suprafața solidă orientată spre el).
Spus , Și , respectiv, suprafețele de separare lichid / gaz, solid / lichid și solid / gaz și indicate cu , , energiile lor libere, energia liberă totală este:
Lichidul este dispus astfel încât să minimizeze energia liberă totală a suprafețelor (termenul gravitațional al energiei este neglijabil pentru volume mici decât cea superficială ). O expresie utilă a unghiului de contact este dat de condiția de echilibru, dată de ecuația lui Young :
Numai Și sunt determinabile experimental, cu toate acestea, se găsesc în literatura științifică a relațiilor experimentale pentru calcularea Și , precum legea lui Girifalco și Good (1957-60):
cu
Și Și volume molare de solid și lichid.
Condițiile la graniță Și exprimă respectiv:
- umectabilitate completă cu formarea unui strat de lichid cu grosime moleculară;
- absența totală a umectabilității.
În concluzie, umectabilitatea, favorizată de energiile interfaciale scăzute, energiile de suprafață ridicate și tensiuni superficiale modeste, cu același lichid de umectare ( ) și a tipului de material solid, este puternic influențat de starea de netezime și de prezența impurităților pe suprafața materialului în sine: acest lucru poate fi observat și experimental sub forma unui menisc .
Termodinamica
Acțiunile atractive dintre moleculele unui lichid (forțele de coeziune ) fac ca moleculele stratului de suprafață să fie supuse unei forțe rezultate diferite de zero, care tinde să le facă să se deplaseze spre interior; de aceea tind să scape de suprafața limită a lichidului și, în consecință, aceasta tinde să-și asume extensia minimă posibilă (în absența altor forțe, suprafața minimă este cea sferică).
Moleculele de pe suprafață au o energie potențială mai mare decât cea a moleculelor din interiorul lichidului, astfel încât, dacă doriți să măriți extensia suprafeței libere a unui lichid, este necesar să cheltuiți o energie proporțională cu creșterea suprafeței.
Dacă lichidul suferă o transformare care doar își alterează suprafața , există o variație a energiei interne, , care este practic egal cu variația energiei potențiale a stratului de suprafață și, prin urmare, proporțional cu creșterea a suprafeței. Această variație internă a energiei (pentru prima lege a termodinamicii ) este în parte ( ) furnizat de energia cinetică a moleculelor din mediu și parțial ( ) corespunzătoare unei lucrări mecanice care trebuie asigurată din exterior.
Definește tensiunea superficială (sau suprafața de energie liberă ) a unui lichid cantitatea de lucru necesară pentru a crește extinderea suprafeței sale a unei unități menținând temperatura și presiunea constante ale sistemului , și anume creșterea energiei libere pe unitate de suprafață:
- ,
unde este este energia liberă a lui Gibbs e este suprafața.
Din aceasta este posibil să se deducă prima ecuație Kelvin care dă entalpia de suprafață (sau energia de suprafață)
Influența temperaturii asupra tensiunii superficiale
Există doar relații empirice pentru a determina influența temperaturii asupra valorii asumate de tensiunea superficială.
Eötvös
in care:
- este volumul molar al substanței
- este temperatura critică
- este constantă pentru fiecare substanță.
De exemplu, pentru apă k = 1,03 erg / ° C, V = 18 ml / mol și T C = 374 ° C.
Guggenheim-Katayama
in care este o constantă a fiecărui lichid e este un factor empiric, a cărui valoare este de 11/9 pentru lichidele organice.
Salt de presiune pe o suprafață curbată
În absența vâscozității , saltul de presiune pe o suprafață curbată este dat de ecuația Young-Laplace , care leagă presiunea din interiorul unui lichid de presiunea externă, tensiunea superficială și geometria suprafeței.
- .
Această ecuație este aplicabilă oricărei suprafețe:
- pentru o suprafață plană : presiunea internă și cea externă sunt egale;
- pentru o suprafață sferică
- pentru o suprafață toroidală , unde r și R sunt razele torului.
Pentru o adevărată bulă sferică, termenul datorat tensiunii superficiale este dublu. Acest lucru se datorează prezenței a două suprafețe, una în interior și una în afara bulei.
A doua ecuație Kelvin
A doua ecuație Kelvin poate fi obținută folosind ecuația Clapeyron ; arată cum, datorită tensiunii superficiale, presiunea de vapori a picăturilor mici de lichid în suspensie este mai mare decât presiunea de vapori „standard” a aceluiași lichid dispus într-un strat plat.
unde este:
- este presiunea standard a vaporilor unui lichid dat la o temperatură și presiune date.
- reprezintă volumul molar.
- este raza sferei.
- este constanta gazului .
Notă
Bibliografie
- Donato Spataro, Tratat teoretic și practic de hidromecanică. v.1 , U. Hoepli, Milano, 1915.
- Lev Davidovič Landau , Evgenij Michajlovič Lifšic , Fizica statistică , Editori Riuniti, Roma, 1978.
- ( EN ) Landau LD, Lifshitz EM, Mecanica fluidelor , Pergamon Press, 1959.
- Duilio Citrini , Giorgio Noseda, Hidraulică , Cesano Boscone, Editura Ambrosiana, 1987, p. 468.
Elemente conexe
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere despre tensiunea superficială
Wikimedia Commons conține imagini sau alte fișiere despre tensiunea superficială
linkuri externe
- ( EN ) Tensiunea superficială , în Encyclopedia Britannica , Encyclopædia Britannica, Inc.
- Tensiunea superficială ( PDF ), pe polymertechnology.it .
- Marangoni Stream , pe strangepaths.com .
- Videoclip care prezintă efectele tensiunii superficiale. , pe physics.decapoa.altervista.org . Adus la 19 decembrie 2008 (arhivat din original la 5 martie 2016) .
- Tensiuni superficiale de lichide , pe itchiavari.org .
- ( EN ) Tensiunea interfațială ( PDF ) [ link rupt ] , pe gtdbernoulli.nl .
- ( DE ) Aderare ( PDF ), pe sundoc.bibliothek.uni-halle.de .
| Controlul autorității | Tesauro BNCF 41692 · LCCN (EN) sh85130727 · GND (DE) 4139720-4 · BNF (FR) cb11977813j (dată) · NDL (EN, JA) 00.563.859 |
|---|









































![\ phi = {\ frac {4 {\ sqrt [{3}] {V_ {S} \ cdot V_ {L}}}} {({\ sqrt [{3}] {V_ {S}}} + {\ sqrt [{3}] {V_ {L}}}) ^ {2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9fa6cf165a5108cd3ac2dc75156e543f13ea57c8)



























