Tioli

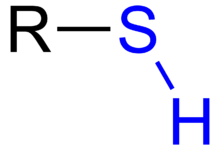
Tiolii ( tioalcoolii sau mercaptanii [1] ) sunt compuși organici similari alcoolilor în care atomul de oxigen a fost înlocuit cu un atom de sulf , având astfel formula generală R-SH. [1] Grupul funcțional –SH este denumit o grupare tiol sau o grupare sulfanil .
O caracteristică comună a aproape tuturor tiolilor este mirosul lor neplăcut intens. Tiolii simpli sunt adăugați la metan , inodor și incolor, ca „ mirositori ”, pentru a dezvălui orice scurgeri.
Etimologia mercaptanului derivă din latină ( mercurius captans ), deoarece s-a observat că compușii care conțin grupări sulfhidril se leagă puternic de elementul mercur. Deși acest nume nu mai este utilizat în mod obișnuit, preferând tiolul mai modern, până în 1993 termenul de mercapto- a fost recomandat de IUPAC ca prefix pentru grupul funcțional (-SH), ulterior a fost înlocuit cu sulfanil-. [1]
Sinteză
Acestea sunt sintetizate prin tratarea halogenurilor de alchil cu ioni de sulfhidrat HS - în exces:
De asemenea, se formează în vinuri prin reacția hidrogenului sulfurat cu alcooli, dând naștere tiolilor cu mirosuri clasice de ceapă și usturoi.
Reactivitate
Oxidarea tiolului este un proces reversibil care duce la formarea disulfurilor RSSR: legătura disulfură este foarte importantă în unele proteine , gândiți-vă, de exemplu, că părul este drept sau ondulat ca o consecință a modificărilor structurale datorate punților disulfurii . Mai mult, punțile disulfură sunt utilizate pentru a sintetiza proteine ciclice mici cărora le conferă rigiditate mai mare și stabilitate metabolică mai mare (unele dintre acestea sunt utilizate în chimia radiofarmaceutică , cum ar fi octreotida ).
La fel ca alcoolii, anionii lor RS - dau reacții de adiție nucleofilă și de substituție nucleofilă , dar tiolații sunt nucleofili mai buni decât alcoolații, deoarece dimensiunea mai mare de sulf față de oxigen permite delocalizarea sarcinii electrice negative pe o suprafață mai largă și se adaptează la atac site.
Datorită unei mai bune distribuții electronice a ionului tiolat, tiolii sunt mai acizi decât alcoolii lor corespunzători. Aceasta explică valoarea pK a în jur de 8-9 în comparație cu cea a alcoolilor (pK aproximativ 17).
Întotdeauna din același motiv, ele sunt mai reactive în reacțiile nucleofile. Un exemplu semnificativ este utilizarea 1,2-etanitiitiolului pentru protecția grupării carbonil a aldehidelor și cetonelor în sinteze organice.
Analize
Ele pot fi identificate prin metode spectrometrice, cum ar fi spectrometria de masă sau cromatografie , sau prin metode de reactivitate chimică care formează compuși care se disting prin caracteristicile chimice și fizice ale compusului produs de reacție, cum ar fi punctul de topire sau culoarea (metode colorimetrice).
Clinica
Tiolii sunt un intermediar care derivă din metabolismul metioninei; catabolismul acestui aminoacid apare în ficat. În caz de insuficiență hepatică (de exemplu datorită cirozei) ficatul este incapabil să catabolizeze chiar și tiolii pentru a pune capăt ciclului catabolic. Acest lucru face ca acest compus să fie eliminat fără alte modificări prin urină și respirație. Având în vedere prezența sulfului, eliminarea acestor compuși determină apariția unui miros caracteristic deosebit de neplăcut. Aceasta este descrisă sub termenul „Foetor hepaticus” și este un semn distinctiv al pacienților cu ciroză.
Metode colorimetrice
6-cloromercur-2-nitrofenolul reacționează la pH acid chiar și cu cantități mici de tioli pentru a da un compus intens colorat [2] .
Notă
- ^ a b c ( EN ) IUPAC Gold Book, "thiols"
- ^ S. Akerfeldt, Acta Chem. Scand. , 13, 1959, p. 627.
Elemente conexe
Alte proiecte
-
 Wikționarul conține dicționarul lema « tiol »
Wikționarul conține dicționarul lema « tiol » -
 Wikimedia Commons conține imagini sau alte fișiere pe mercaptani
Wikimedia Commons conține imagini sau alte fișiere pe mercaptani
linkuri externe
- ( EN ) Tioli , în Encyclopedia Britannica , Encyclopædia Britannica, Inc.
| Controlul autorității | LCCN (EN) sh85134883 · GND (DE) 4185267-9 · NDL (EN, JA) 00.567.614 |
|---|