Neoplasm
| Neoplasm | |
|---|---|
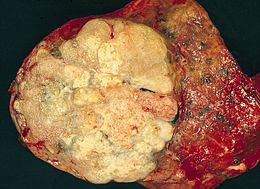
| Adenocarcinomul pulmonar , o formă de neoplasm malign . Rețineți masa periferică mare, lobulată și cu aspect translucid. | |
| Specialitate | anatomie |
| Etiologie | mitoză |
| Clasificare și resurse externe (EN) | |
| ICD-O | 8000/1 și 800 |
| ICD-9 -CM | 140 și239,99 |
| ICD-10 | C00 și D48 |
| Plasă | D009369 |
| Sinonime | |
| Tumora | |
Neoplasmul (din grecescul νέος, neos , „nou”, și πλάσις, plásis , „formațiunea”) sau tumora (din latina tumora , „umflarea”), cunoscută și sub numele de cancer în cazul tumorilor maligne, este, în patologie , „ o masă de țesut care crește în exces și necoordonat în comparație cu țesuturile normale și care persistă în această stare după încetarea stimulilor care au indus procesul ” [1] , după cum clarifică definiția inventată de oncologul Rupert Allan Willis , acceptate la nivel internațional. [2]
Creșterea necontrolată și necoordonată a unui grup de celule , în detrimentul homeostaziei țesuturilor , este determinată de modificări ale propriei moșteniri genetice și stă la baza unei vaste clase de boli, clasificate în funcție de caracteristici diferite, dar în principal în trei moduri :
- în funcție de tipul histologic original al celulelor proliferante: în principal în tumorile epiteliale , mezenchimale , ale celulelor sanguine sau ale țesutului nervos ;
- conform agresivității și evoluției clinice preconizate: în tumorile benigne (necanceroase) și tumorile maligne (canceroase sau canceroase );
- în funcție de stadializarea tumorii, sau clasificarea TNM , pentru tumorile maligne.
În țările dezvoltate , cancerul este principala cauză de deces. Ramura medicinei care se ocupă cu studierea tumorilor din aspectul etiopatogenetic, diagnostic și terapeutic se numește oncologie .
Epidemiologie și note istorice

nu există date
≤ 55
55-80
80-105
105-130
130–155
155-180
180–205
205-230
230-255
255-280
280-305
≥ 305
Termenul de tumoare a fost inventat pe baza aspectului macroscopic al majorității neoplasmelor, care apar frecvent, dar nu întotdeauna, cu o masă semnificativă ( tumoare , "umflare", în latină ) pe locul anatomic de origine.
Termenul de neoplasm , care literalmente înseamnă „nouă formațiune”, este sinonim cu cel anterior, dar ia în considerare, mai degrabă decât aspectul extern al masei, conținutul celular al acesteia, alcătuit din celule „nou formate”.
Neoplasmele reprezintă, după patologiile cardiovasculare, principala cauză de deces în lume (date OMS ). În 2008 , au fost diagnosticate aproximativ 12,7 milioane de tumori maligne și 7,6 milioane de persoane au murit de cancer la nivel mondial. [4] Toate cazurile de cancer sunt cauza a 13% din totalul deceselor anuale, cele mai frecvente fiind: cancerul pulmonar (1,4 milioane de decese), cancerul de stomac (740.000 de decese), cancerul de ficat (700.000 de decese), colorectal (610.000 de decese) și cancer de sân (460.000 de decese). [5] Aceste date fac din tumorile maligne invazive principala cauză de deces în lumea dezvoltată și a doua cauză de deces în țările în curs de dezvoltare . [4] Mai mult de jumătate din cazuri apar în aceste ultime regiuni. [4]
Ratele globale de dezvoltare a cancerului au crescut în principal din cauza îmbătrânirii generale a populației și a modificărilor stilului de viață. [4] Cel mai semnificativ factor de risc pentru apariția cancerului este bătrânețea . [6] Deși se poate întâmpla la orice vârstă, majoritatea persoanelor diagnosticate cu malignitate au peste 65 de ani. [6] Potrivit cercetătorului Robert Weinberg : „Dacă am trăi suficient de mult, mai devreme sau mai târziu am fi condamnați cu toții la cancer”. [7]
Corelația dintre îmbătrânire și cancer este atribuită imunosenescenței [8] , erorilor acumulate în ADN de-a lungul vieții [9] și modificărilor legate de vârstă în sistemul endocrin . [10]
Unele tipuri de cancer cu creștere lentă sunt deosebit de frecvente. Studiile de autopsie efectuate în Europa și Asia au constatat că până la 36% dintre oameni aveau cancer tiroidian nediagnosticat și aparent inofensiv la momentul morții și că 80% dintre bărbați au dezvoltat cancer de prostată până la vârstă.80 de ani. [11] [12] Întrucât aceste tumori nu au cauzat moartea persoanei, identificarea lor ar fi reprezentat supradiagnostic.
Cele mai frecvente trei tipuri de cancer din copilărie sunt leucemia (34%), tumorile cerebrale (23%) și limfoamele (12%). [13] Ratele malignităților infantile au crescut cu 0,6% pe an între 1975 și 2002 în Statele Unite [14] și cu 1,1% pe an între 1978 și 1997 în Europa . [13]
Etiologie
Neoplasmele sunt în primul rând o boală de mediu, cu 90-95% din cazuri atribuibile factorilor de mediu și 5-10% geneticii . [15] Prin factori de mediu, înțelegem orice factor etiologic (adică care specifică agentul cauzal al unei boli) care nu este moștenit genetic, nu doar poluarea . [16] Unii factori comuni de mediu care contribuie la mortalitatea de cancer includ fumat (25-30%), dieta si obezitatea (30-35%), infecții (15-20%), ionizante radiații , stres , lipsa de activitate fizică și de poluanți de mediu . [15]
Este aproape imposibil să se demonstreze ce a cauzat o tumoare la un singur individ, deoarece majoritatea au multiple cauze posibile. De exemplu, dacă un fumător puternic dezvoltă cancer pulmonar, se poate spune că acest comportament a fost cel mai probabil cauza sa, dar nu cu certitudine absolută, deoarece fiecare individ are șanse mici să dezvolte acea tumoare din cauza altor factori. Cel mai probabil, etiologia neoplasmului nu trebuie referită la o mutație a secvenței de nucleotide a ADN-ului nuclear, ci la un control incorect de către histone și nucleozomi asupra replicării celulare.
Produse chimice

Patogeneza neoplasmelor este atribuibilă mutațiilor ADN care afectează creșterea celulară și eventuala dezvoltare a metastazelor . Substanțele care cauzează mutații ADN sunt cunoscute sub numele de mutageni; astfel de substanțe cauzatoare de tumori sunt cunoscute sub numele de agenți cancerigeni. Substanțele particulare au fost legate de tipuri specifice de tumori. Fumatul este asociat cu multe forme de cancer [8] și provoacă 90% din cancerele pulmonare. [17]
Mulți mutageni sunt, de asemenea, agenți cancerigeni, dar unii agenți cancerigeni nu sunt mutageni. Alcoolul este un exemplu de cancerigen chimic care nu este un mutagen. [18] În Europa de Vest , 10% din cazurile de cancer la bărbați și 3% din cazurile de cancer la femei sunt atribuite alcoolului. [19]
Zeci de ani de cercetări au arătat legătura dintre fumat și cancerele de plămâni , laringe , cap, gât, stomac , vezică , rinichi , esofag și pancreas . [20] O țigară conține mai mult de 50 de substanțe recunoscute ca agenți cancerigeni, inclusiv nitrozamine și hidrocarburi policiclice aromatice . [21] Fumatul este responsabil de aproximativ o treime din totalul deceselor provocate de cancer în țările dezvoltate [8] și de aproximativ una din cinci la nivel mondial. [21] Cu toate acestea, numărul fumătorilor din întreaga lume continuă să crească, ducând la ceea ce unele organizații au descris drept epidemia de fumat. [22]
Cancerul legat de profesie se crede că reprezintă între 2% și 20% din toate cazurile. [23] În fiecare an, cel puțin 200.000 de persoane mor de cancer în întreaga lume, posibil dezvoltate ca urmare a propriei lor munci. [24] Majoritatea deceselor provocate de cancer legate de factorii de risc profesional apar în lumea dezvoltată. [24] Se estimează că 20.000 de decese cauzate de cancer și 40.000 de cazuri noi în fiecare an în Statele Unite sunt atribuite condițiilor de muncă. [24] Milioane de lucrători sunt expuși riscului de a dezvolta tipuri de cancer precum cancerul pulmonar și mezoteliomul prin inhalarea fibrelor de azbest și a fumului de țigară sau a leucemiei din cauza expunerii la benzen la locul de muncă. [24]
Nutriție și exerciții fizice
Dieta slabă, inactivitatea fizică și obezitatea sunt corelate cu aproximativ 30-35% din decesele provocate de cancer. [15] [25] Excesul de greutate corporală este asociat cu dezvoltarea multor tipuri de cancer și este un factor prezent în intervalul 14% până la 20% în toate decesele provocate de cancer în Statele Unite. [25] Se crede că inactivitatea fizică contribuie la riscul de a dezvolta cancer, nu numai prin efectele sale asupra greutății corporale, ci și prin efectele sale negative asupra sistemului imunitar și endocrin . [25]
Dietele sărace în legume , fructe și cereale integrale și bogate în carne procesată sau roșie sunt legate de o serie de tipuri de cancer. [25] O dietă bogată în sare este legată de cancerul de stomac, aflatoxina B1 , un aliment adesea contaminat cu carcinom hepatocelular , mestecând nuci de Areca catechu cu cancer de gură. [26] Acest lucru poate explica parțial diferențele de incidență a cancerului în diferite țări, de exemplu, cancerul de stomac este mai frecvent în Japonia datorită dietei lor bogate în săruri , [27] în timp ce cancerul de colon este mai frecvent în Japonia . Frecvent în Statele Unite. Imigranții dezvoltă riscul pe baza noii țări în care se mută, adesea în decursul unei generații , sugerând o legătură substanțială între dietă și cancer. [28]
Infecții
La nivel mondial, aproximativ 18% din decesele provocate de cancer sunt legate de bolile infecțioase . [15] Acest procent variază în diferite regiuni ale lumii, de la maxim 25% în Africa la mai puțin de 10% în întreaga lume dezvoltată. [15] Virușii sunt agenții infecțioși cel mai frecvent responsabili de dezvoltarea tumorilor, dar bacteriile , micobacteriile (vezi tuberculomul ) și paraziții pot fi, de asemenea, cauza.
Un virus care poate provoca cancer se numește oncovirus . Acestea includ papilomavirusul uman (din cauza neoplaziei cervicale ), virusul Epstein-Barr (boala limfoproliferativă și cancerele nazofaringiene), Herpesvirusul uman 8 (cauza sarcomului și limfoamelor Kaposi , revărsarea primară), virusul "hepatita B și C ( carcinom hepatocelular ). Infecția bacteriană poate crește riscul de cancer, așa cum se observă în cazul cancerului de stomac indus de Helicobacter pylori . [29] Infecțiile parazitare puternic asociate cu cancerul sunt cele de la Schistosoma haematobium ( carcinom cu celule scuamoase ale vezicii urinare ) și ale ficatului, Opisthorchis viverrini și Clonorchis sinensis ( colangiocarcinom ). [30]
Moştenire
Cele mai multe tipuri de cancer sunt non-ereditare. Malignitățile ereditare sunt cauzate în principal de un defect genetic. Mai puțin de 0,3% din populație poartă o mutație genetică care afectează riscul de a dezvolta cancer și reprezintă mai puțin de 3-10% din cazurile diagnosticate. [31] Unele dintre aceste afecțiuni sunt reprezentate de unele mutații moștenite în genele BRCA1 și BRCA2 cu un risc crescut de peste 75% de a dezvolta cancer de sân și ovarian , [31] și ereditare care nu sunt asociate cu polipoza colorectală (HNPCC sau sindromul Lynch ), care este prezent la aproximativ 3% dintre persoanele cu cancer colorectal [32], printre altele.
Transmisibilitate
Spre deosebire de alte animale, la om transmiterea unei tumori de la un individ la altul este un eveniment foarte rar, dar nu imposibil. Au fost înregistrate mai multe cazuri, inclusiv un chirurg care a contractat o formă de histiocitom fibros malign după o leziune a brațului în sala de operație [33] și o frecvență semnificativă a sarcomului Kaposi datorită nu transmiterii virale , ci a celulelor canceroase donatoare în urma transplantului [34] ] .
Agenți fizici
Unele substanțe cauzează cancer în primul rând prin acțiunea lor fizică, mai degrabă decât chimică, asupra celulelor. [35]
Un exemplu important este expunerea prelungită la azbest, care este o cauză majoră a mezoteliomului , un tip de cancer pulmonar malign. [35] Alte substanțe care pot fi clasificate în această categorie sunt wollastonitul , attapulgita , vata de sticlă și vata de stâncă . Se crede că acestea au un efect similar azbestului. [35]
Materialele cu particule non-fibroase care cauzează cancer sunt: praf de cobalt , nichel metalic și silice cristalină ( cuarț , cristobalit și tridimit ). [35]
De obicei, agenții cancerigeni fizici trebuie să pătrundă în corp (de exemplu prin inhalarea unor părți mici) și să ia ani de expunere pentru a dezvolta o tumoare. [35]
Un traumatism fizic care poate provoca un neoplasm este un eveniment foarte dificil. [36] Teoria conform căreia oasele rupte pot provoca neoplazie scheletică , de exemplu, nu a fost niciodată dovedită. [36] În mod similar, trauma fizică nu este acceptată ca cauză a cancerului de col uterin, de sân sau de creier . [36]
O cauză acceptată de comunitatea științifică este aplicarea pe termen lung a obiectelor fierbinți asupra corpului. Arsurile repetate pe aceeași parte a corpului, cum ar fi cele produse de încălzitoarele de mână cu cărbune , pot duce la dezvoltarea neoplasmelor cutanate , mai ales dacă sunt prezenți și agenți cancerigeni chimici. [36] Consumul de băuturi calde poate provoca arsuri solare care favorizează cancerul esofagian. [36]
În general, se crede că neoplasma se poate dezvolta în timpul procesului de reparare a traumei, mai degrabă decât aceasta fiind cauza directă. [36] De fapt, leziunile repetate pe aceleași țesuturi pot duce la proliferarea excesivă a celulelor, care poate crește șansele unei mutații canceroase. Nu există dovezi că inflamația poate provoca cancer. [36]
Radiații ionizante
Până la 10% din tumorile maligne sunt legate de expunerea la radiații ionizante . [15] Mai mult, majoritatea cancerelor de piele non-maligne sunt cauzate de radiații neionizante din spectrul ultraviolet .
Sursele majore de radiații ionizante includ imagistica biomedicală și gazul radon . Radiația ionizantă poate cauza cancer in multe parti ale corpului, în toate animalele și la orice vârstă, tumori solide chiar induse de radiații se dezvolta , de obicei , în jurul valorii de 10-15 de ani si poate dura pana la 40 de ani pentru a deveni manifeste clinic. În timp ce leucemii ia 2 10 ani să apară. [37] Copiii și adolescenții sunt de două ori mai predispuși să dezvolte leucemie indusă de radiații decât adulții. Expunerea la radiații înainte de naștere crește efectul de zece ori. [37] Radiațiile ionizante nu sunt un mutagen deosebit de puternic. [37] Expunerea rezidențială la gazul radon, de exemplu, are riscuri de cancer similare cu cele ale fumului pasiv . [37] Se crede că expunerile la doze mici, cum ar fi locuirea în apropierea unei centrale nucleare , au un efect redus sau deloc asupra dezvoltării cancerului. [37] Radiația este o sursă mai puternică de cancer atunci când este combinată cu alți agenți cancerigeni, cum ar fi expunerea la gazul radon împreună cu fumatul. [37]
Spre deosebire de substanțele chimice, radiațiile ionizante lovesc în mod aleatoriu moleculele din interiorul celulelor. Dacă se întâmplă să se găsească un cromozom , acesta se poate rupe, ducând la un număr anormal, dezactivarea uneia sau mai multor gene în partea afectată a cromozomului , eliminarea unor părți ale secvenței ADN, translocații cromozomiale sau poate provoca alte tipuri de anomalii.cromozomiale. [37] Deteriorarea mai mare duce în mod normal la moartea celulelor, dar daunele mai mici pot permite celulei să supraviețuiască, care, atunci când este mutată, poate să prolifereze și să se dezvolte în neoplazie, mai ales dacă genele supresoare au fost deteriorate de radiații. [37] Trei faze independente par a fi implicate în nașterea unui neoplasm datorat radiațiilor ionizante: modificări morfologice ale celulei, dobândirea nemuririi celulare și dezvoltarea adaptărilor care favorizează formarea unei tumori. [37] Deși particula de radiație nu afectează direct ADN - ul , aceasta declanșează un răspuns de la celule care crește indirect probabilitatea mutațiilor. [37]
Utilizarea medicală a radiațiilor ionizante este o sursă în creștere de cancer cauzat de radiații. Radiațiile ionizante pot fi folosite și pentru tratarea tumorilor în sine ( radioterapie ), dar aceasta poate duce, în unele cazuri, la o tumoare secundară. [37] Mai mult, radiațiile ionizante sunt utilizate în unele tehnici de imagistică biomedicală . Un raport estimează că aproximativ 29.000 de tipuri de cancer ar putea fi legate de aproximativ 70 de milioane de scanări CT efectuate în Statele Unite într-un an. [38] Se estimează că 0,4% din cazurile de cancer dezvoltate în Statele Unite în 2007 se datorează scanărilor CT efectuate în trecut și că această cifră poate crește până la 1,5-2%. [39]
Expunerea prelungită la razele ultraviolete de la soare poate duce la dezvoltarea melanomului și a tumorilor maligne ale pielii. [40] Dovezi puternice stabilesc că radiațiile ultraviolete sunt cauza majorității cancerelor de piele non-melanom, care sunt cele mai frecvente forme de cancer la nivel mondial. [40]
Alte radiații neionizante, cum ar fi frecvențele radio utilizate de telefoanele mobile , transmisia de energie electrică și alte surse similare sunt considerate a fi posibile agenți cancerigeni de către Agenția Internațională pentru Cercetarea Cancerului a Organizației Mondiale a Sănătății . [41]
Hormoni

Unii hormoni sunt legați de dezvoltarea cancerului prin promovarea proliferării celulare. [42] Cancerele a căror naștere este cel mai afectată de hormoni sunt cele legate de sex precum cancerul de sân, endometru , prostată, ovarian și testicular , precum și cancerul tiroidian și osos. [42]
Nivelurile hormonale ale unui individ sunt în mare parte determinate genetic, deci acest lucru ar putea explica cel puțin parțial prezența anumitor tipuri de neoplasme care apar adesea în anumite grupuri familiale care nu au anumite gene. [42] De exemplu, fetele femeilor care au avut cancer mamar au niveluri semnificativ mai ridicate de estrogen și progesteron . Aceste niveluri crescute de hormoni pot explica de ce aceste femei au un risc mai mare de cancer de sân. [42] În mod similar, bărbații de origine africană au niveluri semnificativ mai ridicate de testosteron decât bărbații de origine europeană și, prin urmare, au o incidență mai mare a cancerului de prostată. [42] Bărbații de origine asiatică, cu cele mai scăzute niveluri de testosteron , se bucură de cea mai mică incidență. [42]
Cu toate acestea, factorii non-genetici sunt de asemenea relevanți: persoanele obeze au niveluri mai ridicate de anumiți hormoni asociați cu cancerul și, prin urmare, o incidență mai mare a acestor tipuri de cancer. [42] Femeile care iau terapie de substituție hormonală prezintă un risc crescut de a dezvolta cancere asociate cu acești hormoni. [42] Unele tratamente și abordări de prevenire implică reducerea artificială a nivelului acestor hormoni pentru a evita tumorile sensibile la hormoni. [42]
Alte cauze
Cu excepția transmisiilor rare care apar în timpul sarcinii și în unele cazuri marginale de donare de organe , cancerul nu este o boală transmisibilă. Principalul motiv pentru aceasta este respingerea țesuturilor altoite cauzate de histocompatibilitate . [43] La om și alte vertebrate , sistemul imunitar folosește antigene pentru a distinge celulele între „sine” și „non-sine”, deoarece acești antigeni diferă de la persoană la persoană. Când sunt recunoscuți antigeni „non-self”, sistemul imunitar reacționează împotriva celulei. Aceste reacții protejează împotriva greutății celulelor tumorale prin eliminarea celulelor implantate. În Statele Unite , aproximativ 3.500 de femei însărcinate au cancer în fiecare an și s-a observat transmiterea transplacentară a leucemiei acute , limfomului și melanomului de la mamă la făt . [43] Dezvoltarea tumorilor derivate din donatori în timpul unui transplant de organ este extrem de rară. Principalul neoplasm asociat transplantului pare să fie melanomul malign. [44]
Incidența neoplasmelor variază în funcție de specie, deoarece relația dintre numărul de celule prezente în organism se modifică cu cantitatea și calitatea proteinelor implicate în controlul și suprimarea neoplasmelor ( p53 în cazul oamenilor), în 2011 s-a văzut că la om un factor care crește incidența neoplasmelor este înălțimea mai mare, deoarece aceasta implică un număr mai mare de celule, ceea ce face munca proteinei p53 mai dificilă [45] .
La început a fost ipotezată singura corelație între numărul de celule și tumori, această simplă corelație a fost contestată de Richard Peto , deoarece observase că numărul de tumori nu era proporțional cu dimensiunea diferitelor specii de animale și a elaborat paradoxul Peto , care a deplasat atenția asupra originii neoplasmului și a permis să înțeleagă mai bine mecanismul care duce la nașterea acestuia și tocmai să descopere proteinele implicate în controlul neoplasmelor.
Patogenie
Acest articol sau secțiune despre medicamente este considerat a fi verificat . |
Leziuni precanceroase

Unele leziuni, așa-numitele „precanceroase”, sunt adesea identificabile ca un simptom al unui proces tumoral malign care urmează, deoarece posibilitatea unei treceri la stadiul degenerativ este decisiv ridicată. Leziunile apar în general pe piele și mucoase . Acestea au un caracter diferit: variază de la procese inflamatorii cronice la prolificări hiperplazice benigne, de la disontogene la modificări tisulare datorate dezechilibrului hormonal.
Cele mai frecvente cazuri de leziuni precanceroase sunt formate din keratoza senilă , care afectează în principal fața , gâtul , mâinile și antebrațele ; din keratoza arsenicală , care apare în general la subiecții cărora li se administrează medicamente care conțin arsenic ; din radiodermatită cronică ; de la keratoza profesională , care afectează de obicei lucrătorii din gudron și uleiuri minerale ; de la cicatrici de arsură , ulcere , fistule cronice , unele leziuni luetice , lupus erimatos sistemic și lupus vulgaris , xeroderma pigmentosum . Uneori, cazuri de carcinom bazocelular sau carcinom cu celule scuamoase apar atunci când apar astfel de leziuni.
Într-o măsură mai mică, se găsesc leziuni precanceroase ale sistemului digestiv și urinar : leucoplacie și eritroplakie a cavității bucale, sindrom Plummer-Vinson , polipoză familială a colonului , papilom al vezicii urinare . De asemenea, merită menționate leucoplasia vulvară și crauroza , mastopatia fibrocistică a sânului , leucoplasia laringelui .
Progresia tumorii
Pentru ca o celulă să devină canceroasă, trebuie să acumuleze o serie de daune sistemului de control al reproducerii. De fapt, cancerul este o boală genetică a celulelor somatice.
Toate celulele canceroase și precanceroase prezintă modificări, adesea foarte extinse, ale structurii lor cromozomiale ( cariotip ): numărul de cromozomi prezenți în nucleul lor poate fi modificat, iar cromozomii înșiși sunt deteriorați, multipli sau lipsesc ( aneuploidie ): această observație a făcut ca toate începutul secolului al XX-lea de David Paul von Hansemann și Theodor Boveri , a stat la baza teoriei tumorilor ca „boli cromozomiale” acceptate în medicină până la descoperirea structurii ADN-ului la mijlocul secolului trecut și a mecanismului mutații genetice .
Modificarea cromozomială a celulelor canceroase este atât de extinsă încât oferă dovezi că, în fiecare caz de cancer, toate celulele canceroase provin dintr-o singură celulă mamă mutantă (populație de celule clonale ): de fapt, toate au aceeași formă exactă de daune genetice, atât de mult atât de complexă pentru a face extrem de puțin probabilă posibilitatea a două celule mame diferite care au suferit aceeași serie de mutații din întâmplare.
Tulburarea genetică aleatorie care caracterizează celulele canceroase explică variabilitatea extremă a aspectului, efectelor, simptomelor și prognosticului multor forme cunoscute de cancer.
La baza patogenezei tumorii se află mutația anumitor gene:
- proto-oncogene ,
- gene supresoare tumorale,
- genele implicate în repararea ADN-ului .
Questi ultimi sono quelli che garantiscono la stabilità genetica perché se altri geni sono mutati per azione per esempio di agenti cancerogeni , questi riparano il DNA prima che vada incontro alla replicazione, prima cioè che queste mutazioni diventino stabili. Il cancro può colpire persone di ogni età, ma le persone anziane sono colpite con maggiore frequenza, perché i danni genetici tendono ad accumularsi con il tempo.
Le mutazioni necessarie che una data cellula deve accumulare per dare origine a un cancro sono le seguenti, e sono comuni a tutti i tipi di cancro:
- acquisizione dell'autonomia moltiplicativa per sopravvenuta incapacità a sottostare ai meccanismi regolatori della proliferazione cellulare;
- assenza di inibizione dipendente dalla densità (le cellule normali si moltiplicano fino a una definita densità cellulare, raggiunta la quale diventano quiescenti);
- ridotta capacità di adesione con altre cellule o componenti tissutali;
- assenza di matrice extracellulare (spesso digerita da proteasi ) che favorisce l'invasione di tessuti normali adiacenti;
- angiogenesi : formazione di nuovi vasi sanguigni per fornire ossigeno e fattori nutritivi alle cellule tumorali;
- riduzione o perdita della capacità differenziativa;
- acquisizione della capacità di replicazione illimitata per effetto dell'espressione della telomerasi o con sistemi alternativi chiamati "ALT" (Alternative Lengthening of Telomeres);
- riduzione o perdita della possibilità di andare incontro a morte cellulare programmata ( apoptosi ).
- perdita della cosiddetta inibizione da contatto .
Oltre a queste possono verificarsi (e di solito si verificano) anche altre mutazioni, dipendenti dal particolare tipo di cellula originaria e dalla esatta sequenza dei danni genetici.
Il tumore sfrutta dunque, oltre al danno meccanico che esercita la sua massa cellulare, l'azione di molecole di adesione CAM ( caderine , integrine , selectine , immunoglobuline ) e proteasi ( catepsine , collagenasi , ialuronidasi ), prodotte sia autonomamente sia da parte di cellule dell'organismo ospite, e in particolare macrofagi e fibroblasti .
Il grado di aneuploidia , cioè il numero e l'entità dei difetti cromosomici, viene impiegato nelle biopsie come misura del potenziale canceroso di eventuali cellule anomale riscontrate.
Accrescimento
In seguito a mutazioni oncogeniche, le cellule tumorali acquisiscono caratteristiche di crescita autonoma, afinalistica e progressiva, unite alla perdita delle capacità di differenziazione e di possibillità apoptotica .
- L'accrescimento dei tumori benigni viene definito espansivo : l'aumento del volume cellulare totale, e quindi del tumore stesso, porta ad un aumento della tensione locale con possibili fenomeni necrotici dei tessuti circostanti per compressione dei vasi. La crescita è tuttavia lenta, localizzata e contenuta da una capsula fibrosa.
- L'accrescimento dei tumori maligni viene definito infiltrativo : un tumore con caratteristiche di malignità, oltre all'aumento volumetrico cellulare, tende ad infiltrarsi nei tessuti circostanti ed a metastatizzare . Ciò avviene quando un carcinoma in situ , ovvero contenuto entro la membrana basale, acquisisce capacità infiltrativa dovuta ad un aumento della tensione locale, alla motilità e minore coesività delle cellule tumorali ed alla presenza di sostanze che facilitano la lisi e la penetrazione cellulare.
I tumori, nonostante il meccanismo generale di origine sia unico, possono manifestare una gamma molto vasta di evoluzioni e sintomatologie. In tutti però è costante un aumento del numero di cellule cancerose, dovuto alla maggiore velocità di riproduzione cellulare, per cui un maggior numero di cellule tumorali si moltiplica ed un minor numero di esse muore, mentre quelle che sopravvivono continuano a moltiplicarsi. Di solito la crescita di un tumore segue una legge geometrica: è molto lenta all'inizio, ma accelera all'aumentare della massa del tumore.
L'infiltrazione delle cellule neoplastiche non si arresta di fronte alla parete dei vasi linfatici, dei capillari e delle venule che possono essere invase, con la conseguenza che le cellule tumorali raggiungono i linfonodi o il circolo sanguigno dando inizio a quel processo noto con il termine di metastatizzazione . [46] Sembra che anche l'intervento dei macrofagi possa avere un ruolo nel processo di merito. La causa risiederebbe nella proteina S100A10 che si trova sulla superficie di questi leucociti , la quale permette ai macrofagi di legarsi alle cellule malate contribuendo così alla crescita e alla diffusione del tumore. [47] [48]
Un'altra caratteristica dei tumori maligni è la " recidiva ", cioè il rischio di riformazione del tumore nel sito di origine dopo l'asportazione chirurgica. I tumori maligni, infine, se non rimossi per tempo danno luogo alla cachessia , cioè ad un progressivo e rapido decadimento dell'organismo, che va incontro ad una notevole perdita di peso ed a fenomeni di apatia e astenia .
Analogie e differenze con la cellula staminale
La cellula cancerosa, pur essendo diversa dalle cellule staminali , presenta alcune caratteristiche comuni. Entrambe le cellule hanno la capacità di riprodursi mantenendo costante la lunghezza dei telomeri , questo impedisce alla cellula di invecchiare.
Nonostante l'analogia della capacità di mantenere costante la lunghezza dei telomeri , la cellula cancerosa può presentare delle differenze per il sistema di conservare la lunghezza dei telomeri. Circa l'85% dei tumori utilizza per questo scopo l'enzima telomerasi . La maggior parte delle altre cellule cancerose presenta meccanismi alternativi chiamati "ALT" (Alternative Lenghtening of Telomeres). [49] La cellula staminale presenta inoltre la capacità di mantenere costante il numero complessivo di cellule staminali (divisione asimmetrica), a differenza della cellula cancerosa, che si divide in modo simmetrico e aumenta costantemente il numero di cellule.
Al di là delle analogie e differenze tra la cellula cancerosa e la cellula staminale, da alcuni anni è stata proposta la teoria dell'esistenza di particolari cellule cancerose che sarebbero al tempo stesso anche staminali, le cellule staminali tumorali , la cui esistenza è attualmente ancora oggetto di studio. [50] [51] [52] Esse danno origine al teratoma .
Clinica

Classificazione
Esemplari sono la classificazione per organo di insorgenza e la classificazione per estensione della malattia.
In base al comportamento biologico i tumori si classificano in:
- " benigni ": sono costituiti da cellule che mantengono in parte le loro caratteristiche morfologiche e funzionali, pur esibendo autonomia moltiplicativa. Essi sono caratterizzati da un tipo di sviluppo detto espansivo , perché comprime i tessuti vicini senza distruggerli: i tumori benigni che originano dall'epitelio ghiandolare ( adenomi ) sono spesso avviluppati da una capsula di tessuto connettivo fibroso che li delimita nettamente dai tessuti confinanti, coi quali assumono un rapporto di contiguità.
- " maligni " o " cancro ": sono costituiti da cellule che appaiono morfologicamente e funzionalmente diverse dalle corrispondenti normali. L'atipia morfologica, che è tanto maggiore quanto più indifferenziato è il tumore, si manifesta con mancanza di uniformità nella forma e nelle dimensioni delle cellule ( polimorfismo ) e degli organi cellulari, in particolare del nucleo, che è frequentemente ipercromico ed in fase mitotica. I tessuti vicini al tumore maligno vengono invariabilmente infiltrati e distrutti dalle cellule tumorali che si sostituiscono a quelle normali, fenomeno questo caratteristico della malignità e noto col termine "invasività neoplastica".
- " borderline ": in alcuni casi i tumori presentano un comportamento intermedio fra la malignità e la benignità (tumori " borderline ") o risultano inclassificabili (tumori a comportamento biologico incerto). In questi casi, generalmente la frequenza delle metastasi è molto bassa e il decorso è lento. Un esempio è il tumore stromale gastrointestinale .
La pericolosità di un tumore non dipende solo dalla sua natura.
| Caratteristiche | Tumori benigni | Tumori maligni |
|---|---|---|
| Struttura | Il tessuto neoplastico:
| Il tessuto neoplastico:
|
| Crescita | Espansiva: il tumore cresce lentamente, è ben delimitato e spesso contenuto in un feltro di fibre reticolari e collagene ; si espande comprimendo i tessuti circostanti ma non si infiltra in essi. | Infiltrativa: il tumore non ha confini netti, e oltre a crescere di volume si infiltra nei tessuti circostanti, invadendoli. |
| Velocità di crescita | Solitamente lenta. | Solitamente veloce. |
| Recidiva in loco (dopo intervento chirurgico) | Raramente. | Frequente. |
| Metastasi a distanza | No. | Possibili. |
| Danni all'organismo | Il tumore provoca:
| Il tumore provoca: |
Nomenclatura
La nomenclatura dei tumori si fonda generalmente sulla morfologia microscopica con una nomenclatura indicata da organizzazioni internazionali come il WHO , intimamente collegata all'istogenesi (tessuto di derivazione) e al comportamento biologico (benignità o malignità) delle neoplasie; applicato correttamente la nomenclatura, è possibile applicare un sistema di codifica. Un esempio di sistema di codifica delle malattie, tumori compresi, è lo SNOMED .
Stadiazione
L'estensione della maggior parte dei tumori maligni nell'organismo (lo stadio ) viene classificata, in genere, attraverso la Classificazione TNM , proposta e mantenuta aggiornata dalla Union for International Cancer Control.
Diagnosi
La dimensione critica di un tumore è di circa 1 centimetro cubico: raggiunta tale dimensione il tumore diventa rilevabile con visite mediche ed analisi ( marker tumorali presenti nel sangue); [ senza fonte ] spesso però i sintomi iniziali vengono ignorati o sottovalutati.
La natura dei tumori e la loro estensione nell'organismo viene valutata preliminarmente con l'esame clinico, integrato dai dati di laboratorio e dalle tecniche di diagnostica per immagini ( ecografia , esami radiologici tradizionali o computerizzati ( TAC ), imaging a risonanza magnetica , scintigrafia con radioisotopi , PET ).
Al fine di aiutare il medico radiologo nell'analisi della grossa mole di dati fornita dalle tecniche citate, diversi studi si sono focalizzati sulla realizzazione di strumenti per la diagnosi automatizzata/assistita ( CAD ) [54] .
La conferma diagnostica della natura, del grado di malignità ( grading ) e dell'estensione dei tumori ( staging ) spettano ancora all' anatomia patologica ed in particolare all'esame istologico dei tessuti, sempre più spesso integrato da tecniche di smascheramento di antigeni (ad esempio, mediante le colorazioni immunoistochimiche ) o di tecniche di biologia molecolare per lo studio degli acidi nucleici ( genomica ) o delle proteine ( proteomica ).
Trattamento
Vi sono molte opzioni disponibili riguardo al trattamento delle varie neoplasie, sia benigne che maligne, tra cui: la chirurgia , la chemioterapia , la radioterapia e le cure palliative . La decisione del trattamento da utilizzare dipende sostanzialmente dalla posizione e dal tipo e grado di tumore, nonché dalla salute del paziente e dalle sue aspettative.
Trattamento chirurgico
La chirurgia è il principale metodo per trattare la maggior parte dei tumori solidi e isolati e può svolgere un ruolo nella palliazione e nel prolungamento della sopravvivenza. È il trattamento di elezione nel caso di neoplasie benigne. Costituisce, inoltre, una parte fondamentale del processo diagnostico grazie alla messa in vista della massa tumorale e alla possibilità di eseguire una biopsia . Nei casi di neoplasie benigne o di tumori confinati, la chirurgia tenta, in genere, di resecare l'intera massa insieme, in alcuni casi, ai linfonodi locali. Per alcuni tipi di neoplasia, ciò è sufficiente a portare ad un buon risultato. [55]
Chemioterapia
La chemioterapia , in aggiunta alla chirurgia, si è dimostrata utile in un certo numero di neoplasie, tra cui: neoplasie della mammella, al colon-retto, al pancreas, ai testicoli , all'ovaio e al polmone . [55] L'efficacia della chemioterapia è spesso in contrasto con l'alta tossicità subita dagli altri tessuti del corpo.
Radioterapia

La radioterapia è un trattamento che comporta l'utilizzo di radiazioni ionizzanti , nel tentativo di curare o migliorare i sintomi neoplastici. Questo perché le cellule neoplastiche sono molto sensibili alle radiazioni. È utilizzata in circa la metà di tutti i casi e la radiazione può essere sia da fonti interne, come nel caso della brachiterapia sia da fonti esterne, con l'utilizzo di acceleratori lineari . La radioterapia è tipicamente utilizzata in combinata alla chirurgia o alla chemioterapia, ma per alcuni tipi di tumore, come quelli precoci e relativi al capo-collo, può essere utilizzata da sola. È stato dimostrato che è efficace come cura palliativa per diminuire il dolore causato da metastasi ossee, nel 70% dei pazienti. [56]
Trattamenti alternativi
Trattamenti complementari e alternativi, sono un gruppo eterogeneo di assistenza sanitaria, pratiche e prodotti che non fanno parte della medicina convenzionale. [57] Per medicina complementare ci si riferisce ai metodi e alle sostanze utilizzate insieme alla medicina convenzionale, mentre per medicina alternativa si intendono i composti utilizzati al posto della medicina scientificamente riconosciuta. [58]
La maggior parte dei farmaci complementari e alternativi per il trattamento di neoplasie maligne non sono stati rigorosamente studiati o testati. Alcuni trattamenti alternativi valutati dalla comunità medica hanno dimostrato di essere inefficaci, tuttavia, continuano ad essere commercializzati e promossi. [59]
Prognosi
Le neoplasie benigne hanno generalmente una buona prognosi , i tumori maligni hanno una reputazione di malattia mortale.
Nel complesso, circa la metà delle persone in trattamento per il cancro invasivo (esclusi i tumori della pelle in situ e non-melanomi) muoiono a causa sua o per via del trattamento. [4]
La sopravvivenza è peggiore in tutti i paesi in via di sviluppo. [4] Tuttavia, i tassi di sopravvivenza variano notevolmente a seconda della tipologia di tumore, con una gamma che va da una guarigione quasi totale a quasi nessuna speranza di sopravvivenza. Predire la sopravvivenza sia a breve che a lungo termine è difficile e dipende da molti fattori. I più importanti sono il tipo di tumore, l'età del paziente e la sua salute generale. Le persone fragili e con altri problemi di salute hanno tassi di sopravvivenza più bassi. Un centenario è improbabile che sopravviva per più di cinque anni, anche se il trattamento ha successo.
Le persone che riferiscono una migliore qualità della vita, tendono a sopravvivere più a lungo. [60] Le persone con bassa qualità di vita possono incorrere nel disturbo depressivo ed in altre complicanze, dovute al trattamento o alla sua progressione, che danneggia la loro qualità di vita, riducendone la durata.
Prevenzione
Stile di vita
Lo stile di vita ha una significativa influenza sul rischio di contrarre il cancro. Secondo alcuni studi se tutti adottassero uno stile di vita corretto il numero dei tumori si ridurrebbe di un terzo. La dieta, l'inattività fisica, e l' obesità sono collegate approssimativamente al 30-35% delle morti per cancro. [15] [25]
Qualsiasi fumo di tabacco in qualsiasi quantità come l' alcol al di sopra di valori modici aumentano significativamente il rischio di ammalarsi di tumore (oltre che di contrarre malattie cardiovascolari).
Sono a rischio tutti i prodotti animali conservati mediante nitrati o nitriti ( pesce , carne , salumi ).
Dieta
Vi sono delle indicazioni precise sulla dieta da seguire per evitare l'accumularsi di fattori favorenti l'insorgenza dei tumori. [ senza fonte ]
Note
- ^ Cit. in Robbins Basic Pathology , 8ª edizione, Saunders/Elsevier 2007, cap. 6
- ^ ( EN ) Tumor: MedlinePlus Medical Encyclopedia , su medlineplus.gov . URL consultato il 27 novembre 2020 .
- ^ WHO Disease and injury country estimates , su World Health Organization , 2009. URL consultato l'11 novembre 2009 .
- ^ a b c d e f Jemal A, Bray, F, Center, MM, Ferlay, J, Ward, E, Forman, D, Global cancer statistics , in CA: a cancer journal for clinicians , vol. 61, n. 2, febbraio 2011, pp. 69–90, DOI : 10.3322/caac.20107 , PMID 21296855 .
- ^ WHO , Cancer , su who.int , World Health Organization, ottobre 2010. URL consultato il 5 gennaio 2011 .
- ^ a b Coleman, William B. and Rubinas, Tara C., 4 , in Tsongalis, Gregory J. and Coleman, William L. (a cura di), Molecular Pathology: The Molecular Basis of Human Disease , Amsterdam, Elsevier Academic Press, 2009, p. 66, ISBN 0-12-374419-9 .
- ^ Johnson, George, Unearthing Prehistoric Tumors, and Debate , in The New York Times , 28 dicembre 2010.
- ^ Pawelec G, Derhovanessian, E, Larbi, A, Immunosenescence and cancer , in Critical reviews in oncology/hematology , vol. 75, n. 2, agosto 2010, pp. 165–72, DOI : 10.1016/j.critrevonc.2010.06.012 , PMID 20656212 .
- ^ Alberts, B, Johnson A, Lewis J et al. , The Preventable Causes of Cancer , in Molecular biology of the cell , 4th, New York, Garland Science, 2002, ISBN 0-8153-4072-9 .
- ^ Anisimov VN, Sikora, E, Pawelec, G, Relationships between cancer and aging: a multilevel approach , in Biogerontology , vol. 10, n. 4, agosto 2009, pp. 323–38, DOI : 10.1007/s10522-008-9209-8 , PMID 19156531 .
- ^ Fraumeni, Joseph F.; Schottenfeld, David; Marshall, James M., Cancer epidemiology and prevention , Oxford [Oxfordshire], Oxford University Press, 2006, p. 977, ISBN 0-19-514961-0 .
- ^ Bostwick, David G.; Eble, John N., Urological Surgical Pathology , St. Louis, Mosby, 2007, p. 468, ISBN 0-323-01970-6 .
- ^ a b Kaatsch P, Sikora, E, Pawelec, G, Epidemiology of childhood cancer , in Cancer treatment reviews , vol. 36, n. 4, giugno 2010, pp. 277–85, DOI : 10.1016/j.ctrv.2010.02.003 , PMID 20231056 .
- ^ Ward EM, Thun, MJ, Hannan, LM, Jemal, A, Interpreting cancer trends , in Annals of the New York Academy of Sciences , vol. 1076, settembre 2006, pp. 29–53, Bibcode : 2006NYASA1076...29W , DOI : 10.1196/annals.1371.048 , PMID 17119192 .
- ^ a b c d e f g Anand P, Kunnumakkara AB, Kunnumakara AB, Sundaram C, Harikumar KB, Tharakan ST, Lai OS, Sung B, Aggarwal BB,Cancer is a preventable disease that requires major lifestyle changes , in Pharm. Res. , vol. 25, n. 9, settembre 2008, pp. 2097–116, DOI : 10.1007/s11095-008-9661-9 , PMC 2515569 , PMID 18626751 .
- ^ Kravchenko J, Akushevich I, Manton, KG, Cancer mortality and morbidity patterns in the US population: an interdisciplinary approach , Berlin, Springer, 2009, ISBN 0-387-78192-7 .
- ^ Biesalski HK, Bueno de Mesquita B, Chesson A, Chytil F, Grimble R, Hermus RJ, Köhrle J, Lotan R, Norpoth K, Pastorino U, Thurnham D, European Consensus Statement on Lung Cancer: risk factors and prevention. Lung Cancer Panel , in CA Cancer J Clin , vol. 48, n. 3, 1998, pp. 167–76; discussion 164–6, DOI : 10.3322/canjclin.48.3.167 , PMID 9594919 .
- ^ Seitz HK, Pöschl G, Simanowski UA, Alcohol and cancer , in Recent Dev Alcohol , vol. 14, 1998, pp. 67–95, PMID 9751943 .
- ^ Schütze M, Boeing H, Pischon T, Rehm J, Kehoe T, Gmel G, Olsen A, Tjønneland AM, Dahm CC, Overvad K, Clavel-Chapelon F, Boutron-Ruault MC, Trichopoulou A, Benetou V, Zylis D, Kaaks R, Rohrmann S, Palli D, Berrino F, Tumino R, Vineis P, Rodríguez L, Agudo A, Sánchez MJ, Dorronsoro M, Chirlaque MD, Barricarte A, Peeters PH, van Gils CH, Khaw KT, Wareham N, Allen NE, Key TJ, Boffetta P, Slimani N, Jenab M, Romaguera D, Wark PA, Riboli E, Bergmann MM,Alcohol attributable burden of incidence of cancer in eight European countries based on results from prospective cohort study , in BMJ , vol. 342, 2011, pp. d1584, DOI : 10.1136/bmj.d1584 , PMC 3072472 , PMID 21474525 .
- ^ Kuper H, Boffetta P, Adami HO, Tobacco use and cancer causation: association by tumour type , in J. Intern. Med. , vol. 252, n. 3, settembre 2002, pp. 206–24, DOI : 10.1046/j.1365-2796.2002.01022.x , PMID 12270001 .
- ^ a b Kuper H, Adami HO, Boffetta P, Tobacco use, cancer causation and public health impact , in J. Intern. Med. , vol. 251, n. 6, giugno 2002, pp. 455–66, DOI : 10.1046/j.1365-2796.2002.00993.x , PMID 12028500 .
- ^ Proctor RN, The global smoking epidemic: a history and status report , in Clin Lung Cancer , vol. 5, n. 6, maggio 2004, pp. 371–6, DOI : 10.3816/CLC.2004.n.016 , PMID 15217537 .
- ^ Irigaray P, Newby JA, Clapp R, Hardell L, Howard V, Montagnier L, Epstein S, Belpomme D, Lifestyle-related factors and environmental agents causing cancer: an overview , in Biomed. Pharmacother. , vol. 61, n. 10, dicembre 2007, pp. 640–58, DOI : 10.1016/j.biopha.2007.10.006 , PMID 18055160 .
- ^ a b c d WHO calls for prevention of cancer through healthy workplaces , su who.int , World Health Organization, 27 aprile 2007. URL consultato il 13 ottobre 2007 .
- ^ a b c d e Kushi LH, Byers T, Doyle C, Bandera EV, McCullough M, McTiernan A, Gansler T, Andrews KS, Thun MJ, American Cancer Society Guidelines on Nutrition and Physical Activity for cancer prevention: reducing the risk of cancer with healthy food choices and physical activity , in CA Cancer J Clin , vol. 56, n. 5, 2006, pp. 254–81; quiz 313–4, DOI : 10.3322/canjclin.56.5.254 , PMID 17005596 .
- ^ Park S, Bae J, Nam BH, Yoo KY, Aetiology of cancer in Asia ( PDF ), in Asian Pac. J. Cancer Prev. , vol. 9, n. 3, 2008, pp. 371–80, PMID 18990005 (archiviato dall' url originale il 4 settembre 2011) .
- ^ Brenner H, Rothenbacher D, Arndt V, Epidemiology of stomach cancer , in Methods Mol. Biol. , vol. 472, 2009, pp. 467–77, DOI : 10.1007/978-1-60327-492-0_23 , PMID 19107449 .
- ^ Buell P, Dunn JE, Cancer mortality among Japanese Issei and Nisei of California , in Cancer , vol. 18, n. 5, maggio 1965, pp. 656–64, DOI : 10.1002/1097-0142(196505)18:5<656::AID-CNCR2820180515>3.0.CO;2-3 , PMID 14278899 .
- ^ Pagano JS, Blaser M, Buendia MA, Damania B, Khalili K, Raab-Traub N, Roizman B, Infectious agents and cancer: criteria for a causal relation , in Semin. Cancer Biol. , vol. 14, n. 6, dicembre 2004, pp. 453–71, DOI :10.1016/j.semcancer.2004.06.009 , PMID 15489139 .
- ^ Samaras V, Rafailidis PI, Mourtzoukou EG, Peppas G, Falagas ME, Chronic bacterial and parasitic infections and cancer: a review ( PDF ), in J Infect Dev Ctries , vol. 4, n. 5, maggio 2010, pp. 267–81, PMID 20539059 .
- ^ a b Roukos DH, Genome-wide association studies: how predictable is a person's cancer risk? , in Expert Rev Anticancer Ther , vol. 9, n. 4, aprile 2009, pp. 389–92, DOI : 10.1586/era.09.12 , PMID 19374592 .
- ^ Cunningham D, Atkin W, Lenz HJ, Lynch HT, Minsky B, Nordlinger B, Starling N, Colorectal cancer , in Lancet , vol. 375, n. 9719, marzo 2010, pp. 1030–47, DOI : 10.1016/S0140-6736(10)60353-4 , PMID 20304247 .
- ^ ( EN ) Gärtner HV, et al , Genetic analysis of a sarcoma accidentally transplanted from a patient to a surgeon , in N Engl J Med , vol. 335, n. 20, Massachusetts Medical Society, 14 novembre 1996, pp. 1494-1496, DOI : 10.1056/NEJM199611143352004 , PMID 8890100 , PMC 3415354 .
- ^ ( EN ) Barozzi P, et al , Post-transplant Kaposi sarcoma originates from the seeding of donor-derived progenitors , in Nat Med , vol. 9, n. 5, Macmillan Publishers Limited, maggio 2003, pp. 554-561, DOI : 10.1038/nm862 , PMID 12692543 .
- ^ a b c d e Maltoni CFM, Holland JF, Chapter 16: Physical Carcinogens , in Bast RC, Kufe DW, Pollock RE, et al. (a cura di), Holland-Frei Cancer Medicine , 5th, Hamilton, Ontario, BC Decker, 2000, ISBN 1-55009-113-1 . URL consultato il 31 gennaio 2011 .
- ^ a b c d e f g Gaeta, John F, Chapter 17: Trauma and Inflammation , in Bast RC, Kufe DW, Pollock RE, et al. (a cura di), Holland-Frei Cancer Medicine , 5th, Hamilton, Ontario, BC Decker, 2000, ISBN 1-55009-113-1 . URL consultato il 27 gennaio 2011 .
- ^ a b c d e f g h i j k Little JB, Chapter 14: Ionizing Radiation , in Kufe DW, Pollock RE, Weichselbaum RR, Bast RC Jr, Gansler TS, Holland JF, Frei E III (a cura di), Cancer medicine , 6th, Hamilton, Ont, BC Decker, 2000, ISBN 1-55009-113-1 .
- ^ Berrington de González A, Mahesh M, Kim KP, Bhargavan M, Lewis R, Mettler F, Land C, Projected cancer risks from computed tomographic scans performed in the United States in 2007 , in Arch. Intern. Med. , vol. 169, n. 22, dicembre 2009, pp. 2071–7, DOI : 10.1001/archinternmed.2009.440 , PMID 20008689 .
- ^ Brenner DJ, Hall EJ, Computed tomography—an increasing source of radiation exposure , in N. Engl. J. Med. , vol. 357, n. 22, novembre 2007, pp. 2277–84, DOI : 10.1056/NEJMra072149 , PMID 18046031 .
- ^ a b Cleaver JE, Mitchell DL, 15. Ultraviolet Radiation Carcinogenesis , in Bast RC, Kufe DW, Pollock RE, et al. (a cura di), Holland-Frei Cancer Medicine , 5th, Hamilton, Ontario, BC Decker, 2000, ISBN 1-55009-113-1 . URL consultato il 31 gennaio 2011 .
- ^ IARC classifies radiofrequency electromagnetic fields as possibly carcinogenic to humans ( PDF ), su World Health Organization .
- ^ a b c d e f g h i Henderson BE, Bernstein L, Ross RK, Chapter 13: Hormones and the Etiology of Cancer , in Bast RC, Kufe DW, Pollock RE, et al. (a cura di), Holland-Frei Cancer Medicine , 5th, Hamilton, Ontario, BC Decker, 2000, ISBN 1-55009-113-1 . URL consultato il 27 gennaio 2011 .
- ^ a b Tolar J, Neglia JP, Transplacental and other routes of cancer transmission between individuals , in J. Pediatr. Hematol. Oncol. , vol. 25, n. 6, giugno 2003, pp. 430–4, DOI : 10.1097/00043426-200306000-00002 , PMID 12794519 .
- ^ Dingli D, Nowak MA,Cancer biology: infectious tumour cells , in Nature , vol. 443, n. 7107, settembre 2006, pp. 35–6, Bibcode : 2006Natur.443...35D , DOI : 10.1038/443035a , PMC 2711443 , PMID 16957717 .
- ^ Height and cancer incidence in the Million Women Study: prospective cohort, and meta-analysis of prospective studies of height and total cancer risk
- ^ Cellula neoplastica , in Enciclopedia della scienza e della tecnica , Istituto dell'Enciclopedia Italiana, 2007-2008.
- ^ Scoperta la "forbice" che apre alle metastasi Archiviato il 3 novembre 2011 in Internet Archive .
- ^ Proteina S100A10 coinvolta nella diffusione dei tumori Archiviato il 13 gennaio 2012 in Internet Archive .
- ^ Copia archiviata ( PDF ), su dafml.unito.it . URL consultato il 26 giugno 2012 (archiviato dall' url originale il 25 novembre 2012) .
- ^ TNFα enhances cancer stem cell-li... [Biochem Biophys Res Commun. 2012] - PubMed - NCBI
- ^ http://users.unimi.it/minucci/BARB%202011-2012/Cancer+stem+cells.pdf
- ^ Weissman
- ^ Modificata da Robbins Basic Pathology , 8ª edizione, Saunders/Elsevier 2007, cap. 6
- ^ Marrone S., Piantadosi G., Fusco R., Petrillo A., Sansone M., Sansone C.,, Automatic lesion detection in breast DCE-MRI , in Image Analysis and Processing – ICIAP 2013 Lecture Notes in Computer Science , vol. 8157, dicembre 2013, pp. 359-368, DOI : 10.1007/978-3-642-41184-7_37 .
- ^ a b Holland Chp. 40
- ^ Holland Chp. 41
- ^ Cassileth BR, Deng G, Complementary and alternative therapies for cancer , in Oncologist , vol. 9, n. 1, 2004, pp. 80–9, DOI : 10.1634/theoncologist.9-1-80 , PMID 14755017 .
- ^ What Is CAM? National Center for Complementary and Alternative Medicine . retrieved 3 February 2008.
- ^ Vickers A, Alternative cancer cures: 'unproven' or 'disproven'? , in CA Cancer J Clin , vol. 54, n. 2, 2004, pp. 110–8, DOI : 10.3322/canjclin.54.2.110 , PMID 15061600 .
- ^ Montazeri A,Quality of life data as prognostic indicators of survival in cancer patients: an overview of the literature from 1982 to 2008 , in Health Qual Life Outcomes , vol. 7, dicembre 2009, DOI : 10.1186/1477-7525-7-102 , PMC 2805623 , PMID 20030832 .
Voci correlate
- Metastasi
- Neoplasia maligna
- Classificazione TNM
- Chemioterapia dei tumori
- Dolore oncologico
- Malattie croniche non trasmissibili
Altri progetti
-
 Wikizionario contiene il lemma di dizionario « neoplasia »
Wikizionario contiene il lemma di dizionario « neoplasia » -
 Wikimedia Commons contiene immagini o altri file sul neoplasia
Wikimedia Commons contiene immagini o altri file sul neoplasia - Wikibooks - Statistica descrittiva e inferenziale sulle neoplasie
Collegamenti esterni
- AIRC - Associazione Italiana per la Ricerca sul Cancro , su airc.it .
- Sito dell'Istituto Superiore di Sanità. Definizioni e linee guida in ambito oncologico
- ( EN ) Tumore su MedlinePlus
- Sito ufficiale della IARC International Agency for Research on Cancer
- ( EN ) Sito del gruppo di ricerca dell'Università dell'Alberta su DCA e tumori , su depmed.ualberta.ca . URL consultato il 12 ottobre 2008 (archiviato dall' url originale il 23 ottobre 2008) .
- Recupero lesioni croniche nel malato oncologico ( DOC ), su snamid.org . URL consultato il 5 gennaio 2007 (archiviato dall' url originale il 20 febbraio 2009) .
- Consorzio Interuniversitario Nazionale per la Bio-Oncologia , su cinbo.org .
- Diritti economici dei malati di cancro , su aimac.it .
- Tumore , in Sapere.it , De Agostini .
- Tumore , in Treccani.it – Enciclopedie on line , Istituto dell'Enciclopedia Italiana.
- Neoplasia , in Enciclopedia della scienza e della tecnica , Istituto dell'Enciclopedia Italiana, 2007-2008.