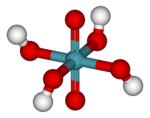
Acid perxenic
| Acid perxenic | |
|---|---|
| Numele IUPAC | |
| acid tetraoxi xenic (VIII) | |
| Caracteristici generale | |
| Formula moleculară sau brută | H 4 XeO 6 |
| Greutatea formulei ( u ) | 231,32 |
| numar CAS | |
| Informații de siguranță | |
| Expresii R. | - |
| Fraze S. | - |
Acidul perxenic este compusul anorganic cu formula H 4 XeO 6 , unde xenonul are un număr de oxidare +8. Acidul perxenic este un acid poliprotic slab care nu a fost niciodată izolat în stare pură. Pe de altă parte, unele dintre sărurile sale, numite perxenate , pot fi obținute. [1] [2]
Sinteza și proprietățile
Soluțiile diluate de acid perxenic se obțin prin acidificarea soluțiilor de perxenate. Acidul pur nu poate fi izolat, deoarece în soluția acidă se descompune formând rapid trioxid de xenon și oxigen gazos: [1] [3]
- 2HXeO 6 3– + 6H + → 2XeO 3 + O 2 + 4H 2 O
H 4 XeO 6 este un acid slab. Au fost măsurate următoarele valori ale constantelor de disociere a acidului : [3]
- H 4 XeO 6 ⇄ H 3 XeO 6 - + H + pK 1 <0
- H 3 XeO 6 - ⇄ H 2 XeO 6 2– + H + pK 2 = 4,29
- H 2 XeO 6 2– ⇄ HXeO 6 3– + H + pK 3 = 10,75
- HXeO 6 3– ⇄ XeO 6 4– + H + pK 4 > 14
H 4 XeO 6 este un oxidant foarte puternic în soluție acidă:
- H 4 XeO 6 + 2H + + 2e - ⇄ XeO 3 + 3H 2 O E ° = +2,42 V
în timp ce în soluție de bază potențialul de reducere scade la +0,99 V. [1]
Perxenați
Perxenatele sunt sărurile acidului perxenic și conțin anionul XeO 6 4– (oxoanionul lui Xe VIII ). Acest anion se formează într-o soluție alcalină prin disproporționarea xenaților sau prin hidroliza XeF 6 : [4]
- 2HXeO 4 - + 2OH - → XeO 6 4– + Xe + O 2 + 2H 2 O
- 2XeF 6 + 16OH - → XeO 6 4– + Xe + O 2 + 12F - + 8H 2 O
Unele perxenate solide au fost izolate. Câteva exemple sunt Na 4 XeO 6 • 6H 2 O, Na 4 XeO 6 • 8H 2 O și Ba 2 XeO 6 • 1,5 H 2 O. Aceste săruri sunt solide incolore, stabile termic până la peste 200 ° C. Studiile de cristalografie cu raze X și spectroscopia Raman au arătat că anionul XeO 6 4– este octaedric. [4] [5] Unghiurile O - Xe - O sunt cuprinse între 87 ° și 93 °, [6], iar distanța de legătură Xe - O este de 187,5 pm . [7]
Anionul XeO 6 4– este, de asemenea, un oxidant puternic în soluție acidă și este redus la xenat: [2] [4]
- 2XeO 6 4– + 6H + → 2HXeO 4 - + O 2 + H 2 O
Prin tratarea Na 4 XeO 6 sau Ba 2 XeO 6 cu acid sulfuric concentrat , se obține XeO 4 . [2]
Notă
Bibliografie
- ( EN ) NN Greenwood și A. Earnshaw, Chimia elementelor , ediția a II-a, Oxford, Butterworth-Heinemann, 1997, ISBN 0-7506-3365-4 .
- WC Hamilton, JA Ibers și DR Mackenzie, Geometry of the Perxenate Ion , în Știință , vol. 141, n. 3580, 1963, pp. 532-534, DOI : 10.1126 / science.141.3580.532 . Adus pe 24 septembrie 2012 .
- ( DE ) AF Holleman și N. Wiberg, Lehrbuch der Anorganischen Chemie , Berlin, Walter de Gruyter, 2007, ISBN 978-3-11-017770-1 .
- ( EN ) CE Housecroft și AG Sharpe, Chimie anorganică , ediția a III-a, Harlow (Anglia), Pearson Education Limited, 2008, ISBN 978-0-13-175553-6 .
- UK Klaening și EH Appelman, Proprietăți protolitice ale acidului perxenic , în Inorg. Chem. , vol. 27, n. 21, 1988, pp. 3760–3762, DOI : 10.1021 / ic00294a018 . Adus pe 24 septembrie 2012 .
- JG Malm, H. Selig, J. Jortner și SA Rice, Chimia xenonului , în Chem. Rev. , vol. 65, nr. 2, 1965, pp. 199-236, DOI : 10.1021 / cr60234a003 . Adus la 22 iunie 2010 .
- JL Peterson, HH Claassen și EH Appelman, Spectre vibraționale și structuri ale ionilor xenat (VI) și perxenat (VIII) în soluție apoasă , în Inorg. Chem. , vol. 9, nr. 3, 1970, pp. 619-621, DOI : 10.1021 / ic50085a037 . Adus pe 24 septembrie 2012 .
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere despre acid perxenic
Wikimedia Commons conține imagini sau alte fișiere despre acid perxenic