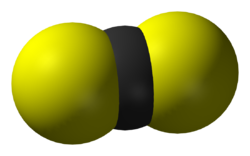
Sulfura de carbon
| Sulfura de carbon | |
|---|---|
| Numele IUPAC | |
| disulfură de carbon | |
| Caracteristici generale | |
| Formula moleculară sau brută | CS 2 |
| Masa moleculară ( u ) | 76,14 g / mol |
| Aspect | lichid incolor |
| numar CAS | |
| Numărul EINECS | 200-843-6 |
| PubChem | 6348 |
| ZÂMBETE | C(=S)=S |
| Proprietăți fizico-chimice | |
| Densitate (g / cm 3 , în cs ) | 1,26 (20 ° C) |
| Solubilitate în apă | 2,1 g / l (20 ° C) |
| Temperatură de topire | −111 ° C (162 K) |
| Temperatura de fierbere | 47 ° C (320 K) |
| Informații de siguranță | |
| Punct de flacără | −30 ° C (243 K) |
| Limite de explozie | 1 - 60% Vol |
| Temperatură de autoaprindere | 100 ° C (373 K) |
| Simboluri de pericol chimic | |
    | |
| Pericol | |
| Fraze H | 225 - 302 - 315 - 319 - 361 - 372 - 412 |
| Sfaturi P | 201 - 210 - 273 - 280 - 308 + 313 - 337 + 313 [1] |
Disulfura de carbon (sau disulfura de carbon ) este o sulfură organică.
La temperatura camerei apare ca un lichid incolor cu un miros caracteristic și neplăcut. Este un compus foarte inflamabil , iritant , toxic datorită interacțiunii sale cu sistemul nervos central și dăunător reproducerii.
Cu toate acestea, este un solvent excelent, cel mai cunoscut pentru elementele pure precum sulful elementar și fosforul elementar.
Prezență în natură și producție
Cantități mici de disulfură de carbon sunt eliberate de erupțiile vulcanice și mlaștini .
CS 2 a fost produs prin reacția directă între carbon (sau cocs ) și sulf la temperaturi ridicate. O reacție la o temperatură mai mică, 600 ° C folosește în schimb gazul natural ca sursă de carbon în prezența silicagelului sau a aluminei ca catalizator [2]
Reacția este analogă arderii metanului . Deși este izoelectronic cu dioxid de carbon , CS 2 este foarte inflamabil:
Reacții
În comparație cu CO 2 , CS 2 este mai reactiv față de nucleofili și mai ușor de redus . Aceste diferențe de reactivitate pot fi atribuite capacității mai mici de donator π a centrelor de sulfură, ceea ce face carbonul mai electrofil. Este utilizat pe scară largă în sinteza compușilor organosulfurați (cum ar fi metam sodiu , un fumigant al solului) și este utilizat în mod obișnuit la producerea țesăturii de viscoză .
Igienă industrială
Expunerea la disulfură de carbon determină sulfocarbonismul , o boală gravă care în trecut și-a asumat o importanță socială importantă datorită amplorii datelor epidemiologice. În Italia a fost una dintre primele boli profesionale recunoscute de INAIL .
Notă
- ^ Foaie de disulfură de carbon pe IFA-GESTIS
- ^ Holleman, AF; Wiberg, E. (2001), Chimie anorganică, San Diego: Academic Press, ISBN 0-12-352651-5
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere despre disulfură de carbon
Wikimedia Commons conține imagini sau alte fișiere despre disulfură de carbon
linkuri externe
- ( EN ) Sulfură de carbon , în Encyclopedia Britannica , Encyclopædia Britannica, Inc.
| Controlul autorității | Tezaur BNCF 38204 · GND (DE) 4131839-0 · NDL (EN, JA) 00.568.536 |
|---|