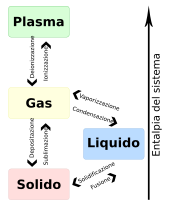
Punct de fuziune
Punctul de topire este definit ca o stare termodinamică , definită de o anumită temperatură (numită temperatură de topire ) și presiune (nu neapărat egală cu presiunea atmosferică ), la care are loc procesul de topire .
În majoritatea cazurilor de interes practic, presiunea este cea atmosferică, practic constantă, și din acest motiv punctul de topire este indicat doar cu temperatura. De exemplu, se spune în mod obișnuit că gheața se topește la 0 ° C, deși în teorie ar fi necesar să se precizeze că acest lucru este adevărat numai la o presiune anume și precisă.
În timpul fuziunii, substanța absoarbe o anumită cantitate de căldură , numită căldură de fuziune , pe care o folosește pentru a rupe legăturile interatomice sau intermoleculare care formează rețeaua cristalină și temperatura încetează să crească până când substanța este complet lichidă: odată ce fuziunea sa încheiat, temperatura începe din nou să crească.
Numai solidele cristaline au un punct de topire foarte precis: solidele amorfe , cum ar fi sticla , nu au un punct de topire bine definit, ci doar un interval de temperatură în care devin progresiv mai moi și mai moi până când se lichefiază. În acest caz vorbim despre un punct de înmuiere .
Mai mult, multe solide cristaline nu au o temperatură de topire precisă, la presiunea atmosferică, deoarece temperatura lor de descompunere este mai mică decât punctul de topire.
Determinarea experimentală a temperaturii de topire
În laboratoarele chimice, măsurarea experimentală a punctului de topire al unei substanțe se realizează prin încălzirea unei probe din acea substanță în condiții controlate și detectarea vizuală sau automată a temperaturii la care se observă topirea.
Proba este, în general, plasată într-un tub capilar , într-o cantitate care o va umple aproximativ 5 mm de jos. Capilarul este încălzit de un fluid (de obicei ulei de silicon sau aer ) a cărui temperatură crește în funcție de un gradient care scade pe măsură ce se apropie de punctul de topire așteptat (dacă este cunoscut). Temperatura de topire poate fi identificată vizual de către un operator sau detectată automat atunci când substanța topită este transparentă; în acest din urmă caz, se presupune că proba este topită în mod convențional, atunci când transmitanța sa depășește pragul de 90%.
Temperaturi de topire
Temperatura de topire a unor substanțe și elemente chimice la o presiune de 1 atm (1 013 hPa )).
Notă
Elemente conexe
linkuri externe
- ( EN ) Punct de topire / Punct de topire (altă versiune) , în Encyclopedia Britannica , Encyclopædia Britannica, Inc.
- Temperaturile latente și căldura de topire a unor substanțe calculate la 1 atm , pe itchiavari.org .
- ( EN ) Punctul de topire absolut al elementelor , pe periodictable.com .