Fierbere
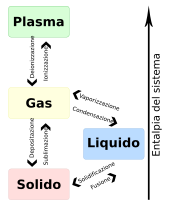
L 'este fenomenul de fierbere vaporizare fizică (adică transformarea unui lichid în gaz ) care implică întreaga masă a unui lichid prin administrarea de căldură . Această tranziție de fază are loc la punctul de fierbere , o temperatură care pentru o presiune dată rămâne constantă pe tot parcursul procesului de fierbere. La această temperatură, vaporizarea are loc numai la suprafața lichidului și se numește evaporare . [1]
Caracteristici


Gazul care se formează în timpul fierberii se îngroașă în grupuri numite „ bule ”, de unde și denumirea fenomenului [2] . Bulele gazoase constituie faza dispersată , în timp ce lichidul din jur se numește fază continuă .
Fierberea are loc numai în stare lichidă și atunci când presiunea vaporilor lichidului este egală cu presiunea atmosferică (sau mai general cu cea a mediului înconjurător).
Deoarece presiunea vaporilor nu este niciodată zero, scăderea suficientă a presiunii poate cauza fierberea la temperaturi chiar apropiate de punctul de îngheț (din acest motiv, în spațiul din afara Pământului nu există corpuri lichide, dacă nu sunt închise în atmosfere care exercită o presiune gravitațională suficientă ).
Invers, prin creșterea presiunii la o temperatură constantă, fierberea se oprește.
Pe măsură ce temperatura crește, având în vedere că crește presiunea vaporilor, rezultă că, sub aceeași presiune, prin încălzirea unui lichid care nu fierbe, acesta este adus la fierbere, în timp ce invers, prin răcirea unui lichid care fierbe, fierberea încetează. Cu toate acestea, continuând să încălziți un lichid care fierbe deja, dacă presiunea este menținută constantă, temperatura nu crește, întrucât toată căldura administrată este absorbită de fenomenul de fierbere ( căldură latentă ).
Punct de fierbere
Temperatura de fierbere la o presiune dată este o caracteristică a unei substanțe sau amestecuri pure , numită „ punctul de fierbere ”, determinată de valorile de temperatură și presiune în care coexistă fazele lichide și gazoase.
Elevatie ebullioscopica
Punctul de fierbere variază în prezența substanțelor dizolvate în lichidul examinat (adică un dizolvat ).
Diferența dintre punctul de fierbere al unei soluții care conține un dizolvat și cel al compusului cu solvent pur se numește elevație ebullioscopică (de obicei indicată cu abrevierea BPE , abrevierea în engleză pentru punctul de fierbere ).
Cota ebullioscopică este direct proporțională cu molalitatea soluției prin intermediul unei caracteristici constante a fiecărui solvent (este o proprietate coligativă ).
Notă
Bibliografie
- Luigi Rolla, chimie și mineralogice. Pentru licee, Ed 29., Dante Alighieri, 1987.
- (EN) Robert Perry , Don W. Green, Perry's Chemical Engineers 'Handbook , ediția a VIII-a, McGraw-Hill, 2007, ISBN 0-07-142294-3 .
Elemente conexe
- Cascadă
- Fierbător
- Bubble (fizică)
- Ebullioscop
- Evaporare
- Punct de fuziune
- Punct triplu
- Regula lui Trouton
- Faza de tranzitie
- Vaporizare
Alte proiecte
-
 Wikționarul conține dicționarul lema « fierbere »
Wikționarul conține dicționarul lema « fierbere » -
 Wikimedia Commons conține imagini sau alte fișiere la fierbere
Wikimedia Commons conține imagini sau alte fișiere la fierbere
linkuri externe
- ( EN ) Fierbere , în Encyclopedia Britannica , Encyclopædia Britannica, Inc.
- ( EN ) Thermopedia, "Fierbere"
- (RO) Punctul de fierbere absolut al elementelor , de pe periodictable.com.
| Controlul autorității | Thesaurus BNCF 20052 · LCCN (EN) sh85040661 · GND (DE) 4054854-5 · BNF (FR) cb12190340j (data) |
|---|