Antimoniu
| Antimoniu | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aspect | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
argintiu , metalic | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Generalitate | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Numele, simbolul, numărul atomic | antimoniu, Sb, 51 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Serie | Semi-metale | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grup , punct , bloc | 15 (VA) , 5 , p | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densitate | 6 697 kg / m³ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Duritate | 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configurare electronică | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termen spectroscopic | 4 S sau 3/2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietăți atomice | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Greutate atomica | 121,760 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Raza atomică (calc.) | 145 (133) pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Raza covalentă | Ora 138 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configurare electronică | [ Kr ] 4 d 10 5 s 2 5p 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| și - după nivelul de energie | 2, 8, 18, 18, 5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Stări de oxidare | ± 3,5 (slab acid ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Structură cristalină | romboedric | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietăți fizice | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Stare a materiei | solid | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punct de fuziune | 903,78 K (630,63 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punct de fierbere | 1 860 K (1 590 ° C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volumul molar | 18,19 × 10 −6 m³ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Entalpia vaporizării | 77,14 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Căldura de fuziune | 19,87 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Presiunea de vapori | 2,49 × 10 −9 Pa a 6 304 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Alte proprietăți | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| numar CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electronegativitate | 2.05 ( scara Pauling ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Căldura specifică | 210 J / (kg K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductibilitate electrică | 2,88 × 10 6 / (m Ω ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductivitate termică | 24,3 W / (m K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energia primei ionizări | 834 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A doua energie de ionizare | 1 594,9 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A treia energie de ionizare | 2 440 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energia celei de-a patra ionizări | 4 260 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A cincea energie de ionizare | 5 400 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energia celei de-a șasea ionizări | 10 400 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Izotopi mai stabili | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| iso: izotop NA: abundență în natură TD: timpul de înjumătățire DM: modul de descompunere DE: energia de descompunere în MeV DP: produs de descompunere | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Antimoniul este elementul chimic cu numărul atomic 51. Simbolul său este Sb , din latina stibium care înseamnă „băț”. Bastoanele realizate cu pulberi de antimoni negru (amestecate cu grăsimi) au fost folosite încă din cele mai vechi timpuri (în Egiptul antic ) pentru machiajul ochilor (kajal, khol), cu funcții rituale și igienice.
Este un semimetal care vine în patru forme alotrope diferite. Forma stabilă are un aspect metalic alb-albăstrui, formele instabile au o culoare galbenă sau neagră. Este utilizat ca agent ignifug și pentru a produce vopsele, emailuri, ceramică și cauciucuri, precum și o gamă largă de aliaje metalice .
Caracteristici
Ca semimetal , antimoniul arată ca un metal , dar nu are comportamente chimice și fizice tipice. În forma sa elementară este un solid alb-argintiu cu reflexe albăstrui care are o conductivitate termică și electrică slabă și care se sublimează la temperaturi relativ scăzute. Reacționează cu acizi oxidanți și halogeni . Antimoniul și aliajele sale se extind la răcire.
Cantitatea de antimoniu din scoarța terestră este estimată a fi între 0,2 și 0,5 ppm [1] . Antimoniul este calcofil , este adesea însoțit de sulf , telur și unele metale grele: plumb , cupru și argint [2] .
Istorie
Antimoniul este un element cunoscut și utilizat în compușii săi din cele mai vechi timpuri, înainte de 3000 î.Hr. [3] Stibnita , sulfură de antimoniu, a fost utilizată atât ca medicament, cât și pentru machiajul ochilor. [3] S-au găsit artefacte care datează din mileniul al IV-lea î.Hr. Pliniu cel bătrân l-a numit stibium în timp ce în jurul anului 800 d.Hr. numele de antimoniu a fost mai folosit și cele două denumiri au fost folosite alternativ atât pentru element cât și pentru sulfura acestuia. Această imprecizie s-a datorat și încercării alchimiștilor de a nu răspândi cunoștințele dobândite, combinând adesea diferite produse pe baza analogiilor lor simbolice. [4] Numai în epoca modernă s-a făcut o distincție.
Înțeles în alchimie
Antimoniul s-a bucurat întotdeauna de o reputație notabilă în alchimie , unde și-a asumat semnificația instinctelor sălbatice și animale care trebuie controlate, [5] simbolizate de lup , [6] și, prin urmare, uneori a fost considerată componenta primordială sau „ materia ”. înainte », a Marii Lucrări , care prin diferite faze ar fi trebuit să culmineze cu producerea pietrei filosofale . [7]
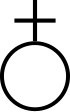
Aceste faze implicau purificarea antimoniului din materie prin eliberarea focului său interior , până când l-a oxidat sau a ucis-o metaforic cu flacăra salamandrei ( nigredo ); în acest mod s-a obținut caput mortuum , adică „capul morții”, un reziduu sulfuros, [8] din care prin sublimare a fost necesar să se separe două tipuri de natură, magmatică și ignorie , asociate respectiv Soarelui și Lunii , și apoi reînscrieți-le în părți egale și sărbătoriți căsătoria chimică . [7] Din unirea lor s-ar naște „copilul”, sau piatra roșie, capabilă să transforme metalele de bază în aur . [7]
Succes și difuzare
În timpul Evului Mediu și al Renașterii, utilizarea antimoniului a cunoscut un succes și o difuzie crescânde, [9] până la punctul că, potrivit istoricului chimiei AF Fourcroy , „niciun corp nu a fost studiat mai mult decât acesta, nimeni nu a fost subiectul unei copii mai mari a scrierilor; s-ar putea crea o întreagă bibliotecă de cărți despre antimoniu. ' [10]
Prima descriere cunoscută a unei proceduri pentru izolarea antimoniului este conținută în cartea De la pirotechnia din 1540 scrisă de metalurgistul italian Vannoccio Biringuccio și publicată postum; această publicație precede cea mai faimoasă carte a lui Georg Agricola , De re metallica din 1556, publicată și ea postum. Descoperirea antimoniului metalic a fost adesea atribuită eronat lui Agricola dintr-un motiv evident: în timp ce cartea De re metallica , scrisă în latină , putea fi citită cu ușurință de către toți cărturarii vremii, cartea De la pirotehnie a fost scrisă în italiană și a întâlnit, prin urmare, o răspândire extrem de minoră.
Ulterior, cartea Triumphwagen des Antimonij a fost publicată la Leipzig în 1604, scrisă în limba germană și apoi tradusă în latină sub denumirea de Currus Triumphalis Antimonii (literal „Carul triumfal al antimoniului”), care conține și descrierea pregătirii antimonului metalic. Deși această carte este mai recentă, călugărul benedictin Basil Valentine , autorul său nominal, a fost foarte des citat în trecut ca descoperitor al antimoniului, deși este acum opinia obișnuită că adevăratul autor al numeroaselor cărți care i-au fost atribuite pur și simplu l-a folosit ca pseudonim numele unui călugăr care nu a existat niciodată; unii cred că provin de la același editor, Johann Thölde . [11]
Pe lângă textul lui Valentino, Paracelsus a contribuit și la faima antimoniului, atribuindu-i virtuți terapeutice, ca și pentru alte metale , inclusiv tratamentul leprei , alopeciei , morfeei , rănilor și ulcerelor . [9] El a inaugurat acea direcție a medicinei numită „ iatrochimie ”, bazată pe utilizarea chimiei în scopuri sănătoase, și destinată să dea naștere unei îndelungate controverse cu farmacologii care au rămas fideli lui Galen cu privire la bunătatea sau altfel a antimoniului. [9]
Printre adepții lui Paracelsus care au susținut validitatea antimoniului, mai mulți alchimiști au derivat numeroși compuși. [12] Oswald Croll, de exemplu, în urma unor corespondențe astrologice precise, a produs un pahar de antimoni care a fost folosit pentru o serie de boli. [12]
Originea numelui
Originea numelui este neclară; poate proveni din cuvintele grecești anti și monos cu sensul de „opus singurătății” deoarece se credea că nu exista în starea sa pură, sau din anthosul grecesc Ammon , care înseamnă „floarea lui Amon ”. [ fără sursă ]
O altă posibilă origine a numelui este „anti- călugăr ”; De fapt, Samuel Johnson , în dicționarul său de chimie, scrie că călugărul german Basil Valentine a încercat antimoniul cu porci care, după un prim efect laxativ puternic, au început imediat să se îngrașe. Basilio a repetat apoi experimentul cu tovarășii săi, care au murit cu toții. De atunci, medicina a numit această substanță antimoină , adică antimonaco [13] . Evident, această versiune trebuie considerată ca o etimologie populară, deoarece termenul antimoniu a existat înainte de 800 d.Hr. și, prin urmare, cu cel puțin 6 secole înainte de exploatările ipotetice ale lui Basil Valentine, care probabil nu a existat niciodată.
Alte utilizări
În 1700, antimoniul a fost interzis de către Facultatea de Medicină din Paris [14] . Interdicția a căzut atunci când recuperarea regelui Ludovic al XIV-lea de febra tifoidă a fost atribuită antimoniului [15] .
Antimoniul a fost utilizat în tratamentul schistosomiazei ; dată fiind afinitatea sa cu sulf , se leagă de atomii de sulf conținuți în anumite enzime utilizate atât de parazit, cât și de gazda umană. Dozele mici sunt capabile să omoare parazitul fără a deteriora organismul pacientului prea mult [16] [14] .
Nume chimic
Simbolul chimic al antimoniului se datorează lui Jöns Jacob Berzelius care a început să-l menționeze în scrierile sale folosind abrevierea numelui latin stibium . Simbolul propus de Berzelius a fost St , ulterior schimbat în Sb [17] . La rândul său, acest nume provine de la numele copt de sulfură de antimoniu, prin greacă.
Aplicații

Antimoniul este din ce în ce mai utilizat în industria semiconductoarelor în producția de diode [18] , senzori cu infraroșu [19] și dispozitive bazate pe efectul Hall .
Aliat cu plumb , își mărește considerabil duritatea și rezistența mecanică, atât de mult încât producția de plumb-antimoniu pentru producerea de baterii auto este principalul consum al acestui element [20] [21] . Alte aplicații includ producțiile de:
- aliaje cu frecare redusă [22] [23]
- aliaje pentru producția de caractere [24] [25]
- gloanțe de urmărire [26]
- învelișuri pentru cabluri [19]
- meciuri [26]
- medicamente emetice [27] [28]
- țevi (aliaje fără plumb, conținând până la 5% antimoniu) [29]
Oxizii și sulfurile de antimoniu, antimonatul de sodiu (V) (NaSbO 3 ) și triclorura de antimoniu (III) (SbCl 3 ) sunt utilizate în producția de compuși ignifugi [30] , emailuri, vopsele, sticlă și ceramică și ca catalizatori de esterificare . Antimoniul este utilizat în industriile semiconductoarelor (dispozitive electronice, diode, tranzistoare, circuite integrate) pentru doparea semiconductoarelor. Cel mai important compus al antimoniului (III) este trioxidul său ( Sb 2 O 3 ), utilizat în principal în producția de ignifugi și ignifugi [31] care sunt la rândul lor folosiți în cele mai diverse sectoare, de la jucării la îmbrăcăminte pentru copii la huse pentru scaune de avion sau auto. Sulfura de antimoniu (III) (Sb 2 S 3 ) este conținută în chibrituri. O aplicație actuală a antimoniului se află în contextul amintirilor de schimbare de fază , ca element principal al unui aliaj de calcogenură numit GST [32] [33] [34] .
Disponibilitate
Deși nu este un element abundent, antimoniul se găsește în peste 100 de minerale diferite. Uneori se găsește în starea sa nativă , dar cea mai frecventă formă este cea a sulfurii, stibnitei (Sb 2 S 3 ).
Antimoniul este comercializat în multe forme fizice: de la pulbere, la cristale, la bucăți, la lingouri.
| Principalii producători de antimoniu în 2019 [35] | ||
|---|---|---|
| Poziţie | țară | Producție (tone) |
| 1 | | 89000 |
| 2 | | 30000 |
| 3 | | 28000 |
| 4 | | 6000 |
| 5 | | 3000 |
| 6 | | 2400 |
| 7 | | 2030 |
| 8 | | 500 |
| 9 | | 310 |
| 10 | | 300 |
| 11 | | 300 |
NOTĂ: Datele pentru Statele Unite nu au fost publicate.
Precauții
| Simboluri de pericol chimic | |
|---|---|
 Atenţie | |
| fraze H | 335 |
| Expresii R. | R 37 |
| sfat P | 262 [36] |
| Fraze S. | S 22-24 / 25 |
Produsele chimice trebuie manipulat cu precauție | |
| Avertizări | |
Antimoniul și mulți dintre compușii săi sunt considerați toxici. Din punct de vedere clinic, otrăvirea cu antimoniu este foarte asemănătoare cu otrăvirea cu arsen . În doze mici provoacă dureri de cap și amețeli, în doze mai mari provoacă crize violente și frecvente de vărsături și duce la moarte în câteva zile. Ca și în cazul arsenului , în prima jumătate a secolului al XIX-lea, crearea testului Marsh , un test de laborator foarte sensibil, a permis analiza sa chimică [37] . În Europa, sunt necesare standarde [38] și soluții pentru reducerea antimoniului în apă pentru a păstra sănătatea umană.
Derivate
Notă
- ^ Gunn, Gus, 1951-, Manual pentru metale critice , ISBN 9781118755211 ,OCLC 861966441 . Accesat la 6 octombrie 2018 .
- ^ Pohl, Walter L., Geologie economică: principii și practică. , Wiley, 2011, ISBN 9781444394863 ,OCLC 927509297 . Accesat la 6 octombrie 2018 .
- ^ a b Paulina Oszajca, The emetic virtue of antimony ( PDF ), în „Fapte și amintiri” , aprilie 2019, pp. 33-44.
- ^ Maria Luigia și Bianca Maria Giusto, Antimoniu, mineral de uz medicinal ( PDF ), în „Fapte și amintiri” , decembrie 2018, p. 210.
- ^ Vezi Antimoniu , pe esopedia.info . Vezi și Simbolismul alchimic al elementelor , pe sentieriniziatici.it .
- ^ Datorită agresivității sale, sulfura de antimoniu ar putea fi numită lupus metallorum , cf. Lupo , pe treccani.it , § 10.
- ^ a b c Patrick Burensteinas, Un alchimist spune (2017), pp. 40-60 , Roma, Studio Tesi Editions, 2019.
- ^ Limbajul alchimiei: alegorii și metafore ermetice , pe duepassinelmistero.com .
- ^ a b c Sergio Tira, introducere la Filostibio, L'Antimonio (1628), pp. 21-22 și 96-97 , Roma, Mediterranee, 1991.
- ^ Antoine-François de Fourcroy , Systeme des connaissances chimiques, et de leurs applications , vol. V, p. 210, § 2 , Paris, Baudoin, 1801 (trad. It. În Filostibio, L'Antimonio , editat de Sergio Tira, introducere, p. 22, op. Cit).
- ^ Povestea manuscriselor ascunse într-o coloană a mănăstirii Erfurt în jurul anului 1450 și descoperite în mod miraculos în jurul anului 1600 poate fi doar o legendă inventată cu succes pentru a da acestor cărți mai multă importanță.
- ^ a b Marcello Fumagalli, Dicționar de alchimie și chimie farmaceutică antică , sub intrarea «antimoniu», pag. 32 , Roma, Mediterranee, 2000.
- ^ John Read, Humor and Humanism in Chemistry , Londra, 1947. citat în Hugh Aldersey-Williams, Favole periodiche , Rizzoli, pp. 478-479, ISBN 978-88-17-04858-3 .
- ^ a b Sneader, Walter., Drug discovery: a history , Wiley, 2005, pp. 57-58, ISBN 0471899798 ,OCLC 57682419 . Accesat la 6 octombrie 2018 .
- ^ Sebastian, Anton., A Dictionary of the History of Medicine. , CRC Press, 1999, ISBN 9781351469999 ,OCLC 1023552019 . Accesat la 6 octombrie 2018 .
- ^ NIIR Board of Consultants & Engineers., Drugs & Pharmaceutical: technology handbook , Asia Pacific Business Press, [data publicării nu a fost identificată], ISBN 8178330547 ,OCLC 880007375 . Accesat la 6 octombrie 2018 .
- ^ Thurlow, KJ, Nomenclatura chimică , Springer, 1998, pp. 35-37, ISBN 9789401149587 ,OCLC 840311024 . Accesat la 6 octombrie 2018 .
- ^ Rashid, Muhammad H., Foundations of Electronics , Apogee, 2002, p. 34, ISBN 8873038530 ,OCLC 849337069 . Accesat la 5 octombrie 2018 .
- ^ A b (EN) Consiliul Național de Cercetare Consiliul Național pentru Materiale, Tendințe în Utilizarea Antimoniului: Raport în NMAB, n. 274, decembrie 1970, p. 87.
- ^ Societatea americană pentru testare și materiale, teste și standarde de coroziune: aplicație și interpretare , în seria manuală ASTM , vol. 20, p. 532.
- ^ Comitetul european pentru dezvoltare. și Lead Development Association., Lead 68: proceduri editate. , [Prima ediție], Pergamon Press, [1969], p. 209, ISBN 9781483137735 ,OCLC 712526558 . Accesat la 5 octombrie 2018 .
- ^ Guruswamy, Sivaraman ,, Engineering Properties and Applications of Lead Alloys , Prima ediție, ISBN 9781482276909 ,OCLC 1027745913 . Accesat la 5 octombrie 2018 .
- ^ Habashi, Fathi. și Wiley InterScience (serviciu online), Alloys: preparare, proprietăți, aplicații , prima ediție, Wiley-VCH, 1998, ISBN 9783527611935 ,OCLC 212131189 . Accesat la 5 octombrie 2018 .
- ^ Kilgour, Frederick G., Evoluția cărții , Oxford University Press, 1998, p. 86, ISBN 1423759915 ,OCLC 65171788 . Accesat la 5 octombrie 2018 .
- ^ Dereu, Brian., Materii prime și finisate: un ghid concis de proprietăți și aplicații , Momentum Press, 2012, ISBN 1606500759 ,OCLC 768374871 . Accesat la 5 octombrie 2018 .
- ^ a b Katz, Harry S. și Milewski, John V., Handbook of fillers for plastics , Van Nostrand Reinhold Co, 1987, p. 283, ISBN 0442260245 ,OCLC 14212758 . Accesat la 5 octombrie 2018 .
- ^ John Quincy, Pharmacopoeia Officinalis [et] Extemporanea: Or, A Complete English Dispensatory, în două părți. Teoretic și practic , ediția a XV-a, T. Longman, 1782.
- ^ The Penny Cyclopaedia of the Society for the Difusion of Useful Knowledge , vol. 2, Londra, 1834, p. 107.
- ^ Merle Henkenius, Utilizarea lipirii fără plumb , în Popular Mechanics , vol. 168, nr. 6, Reviste Hearst, iunie 1991, p. 61.
- ^ Lewin, Menachem. și Pearce, Eli M., Materiale polimerice ignifuge , Springer SUA, 1975, pp. 29-31, ISBN 9781468421484 ,OCLC 840287908 . Accesat la 5 octombrie 2018 .
- ^ Horrocks, A. Richard. și Price, Dennis., Materiale ignifuge , CRC Press, 2001, p. 39, ISBN 1591246148 ,OCLC 53840609 . Accesat la 5 octombrie 2018 .
- ^ Q. Ashton, Heavy Metals - Advances in Research and Application: 2013 Edition , ScholarlyEditions, ISBN 9781481676342 .
- ^ Raoux, Simone. și Wuttig, Matthias., Phase change materials: science and applications , Springer, 2009, p. 228, ISBN 9780387848747 ,OCLC 649692444 . Accesat la 6 octombrie 2018 .
- ^ Li, Hai, 1975-, 2.2 Phase Changhe Memory - Material Research , in Nonvolatile memory design: magnetic, resistive, and phase change , CRC Press, 2012, ISBN 9781439807460 ,OCLC 773316150 . Accesat la 6 octombrie 2018 .
- ^ Statistici privind producția de antimoniu USGS
- ^ foaie de antimoniu pe IFA-GESTIS , pe gestis-en.itrust.de . Adus la 6 iunie 2021 (Arhivat din original la 16 octombrie 2019) .
- ^ Thompson, Robert Bruce., Ghid ilustrat pentru experimentele de chimie la domiciliu: toate laboratoarele, fără prelegere , ed. 1, O'Reilly Media, 2008, p. 399, ISBN 9780596514921 ,OCLC 297574865 . Accesat la 6 octombrie 2018 .
- ^ Reglementările privind tratarea apei , pe acqua-depurazione.it .
Bibliografie
- Francesco Borgese, Elementele tabelului periodic. Descoperire, proprietăți, utilizări. Manual chimic, fizic, geologic , Roma, CISU, 1993, ISBN 88-7975-077-1 .
- R. Barbucci, A. Sabatini și P. Dapporto, Tabel periodic și proprietăți ale elementelor , Florența, Edizioni V. Morelli, 1998 (arhivat din original la 22 octombrie 2010) .
Elemente conexe
- Antimoniu nativ
- Stibism - otrăvire cu antimoniu
- Stibnit
Alte proiecte
-
 Wikicitată conține citate din sau despre antimoniu
Wikicitată conține citate din sau despre antimoniu -
 Wikționarul conține dicționarul lema « antimoniu »
Wikționarul conține dicționarul lema « antimoniu » -
 Wikimedia Commons conține imagini sau alte fișiere despre antimoniu
Wikimedia Commons conține imagini sau alte fișiere despre antimoniu
linkuri externe
- Antimonio , pe Treccani.it - Enciclopedii online , Institutul Enciclopediei Italiene .
- ( EN ) Antimony , în Encyclopedia Britannica , Encyclopædia Britannica, Inc.
- (EN) Antimony pe periodic.lanl.gov, Laboratorul Național Los Alamos .
- (RO) Declarație de sănătate publică pentru antimoniu , pe atsdr.cdc.gov. Adus la 8 martie 2005 (arhivat din original la 15 ianuarie 2009) .
- (EN) Antimony , pe WebElements.com.
- (EN) Antimony , pe EnvironmentalChemistry.com.
- ( EN ) Peter van der Krogt, Elementymology & Elements Multidict: Antimony , la elements.vanderkrogt.net .
- ( RO ) Producția mondială de antimoniu a minelor, pe țări , pe indexmundi.com .
| Controllo di autorità | Thesaurus BNCF 20962 · LCCN ( EN ) sh85005702 · GND ( DE ) 4002299-7 · BNF ( FR ) cb120163060 (data) · NDL ( EN , JA ) 00560276 |
|---|




