Diazotație
Această intrare sau secțiune despre subiectul proceselor chimice nu menționează sursele necesare sau cei prezenți sunt insuficienți . |
În chimie, diazotizarea înseamnă de obicei o reacție organică care implică un substrat aromatic având o grupare amino primară și un reactiv care poate elibera un ion nitrosoniu , cum ar fi acidul azotat sau nitritul de sodiu în prezența acizilor minerali.
Mecanismul de reacție asigură de fapt un intermediar relativ stabil, cunoscut sub numele de sare de diazoniu , care poate reacționa cu alți reactivi sau cu alte substraturi pentru a da naștere la funcționalizări multiple ale aminei originale. De exemplu, ionul diazoniu poate da naștere unui atac electrofil asupra unui inel benzenic sau, mai general, asupra unui inel aromatic. Din acest motiv, diazotizarea are o importanță enormă în funcționalizarea în serii aromatice atât la nivel industrial, cât și la nivel de laborator.
Diazotația este bine cunoscută ca fiind una dintre reacțiile care conduc la sinteza coloranților azoici .
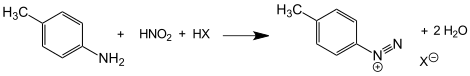
Formarea sării de diazoniu
Reacția produce o sare de diazoniu care poate fi izolată sau poate fi reacționată în continuare. Sărurile de diazoniu se descompun cu ușurință monomolecular, pierzând o moleculă de azot și generând o carbocație . În general, stabilitatea sărurilor de diazoniu este mai mare cu atât este mai mică stabilitatea carbocației. Din acest motiv, sărurile de alchil diazoniu nu sunt foarte stabile și nu sunt foarte utile pentru reacții sintetice, chiar și în laborator. Sărurile arii diazoniu, datorită stabilității slabe a aril- catului, sunt suficient de stabile pentru a fi sintetizate și tratate la temperaturi între 0 și 5 ° C:
Atenție: în stare solidă sunt explozive.
În soluție, descompunerea are loc în 30-60 minute prin încălzire la T> 50-60 ° C. Cu toate acestea, în soluțiile fără agitare, sunt posibile reacții parazitare exoterme care duc la creșteri locale ale temperaturii, cu descompunerea rapidă a întregii mase; descompunerea poate fi explozivă chiar și în faza de soluție. Stabilitatea sărurilor de diazoniu arii crește atunci când substituenții atrăgători de electroni (-NO2, -CN, -COOH, ...) sunt prezente pe nucleul arii care destabilizează cationul arii.
Clorurile de diazoniu pot fi separate de mediul de reacție prin adăugarea de acid tetrafluoboric. Tetrafluoboratul de diazoniu insolubil precipită și poate fi filtrat și uscat cu mare atenție.