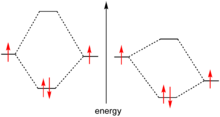
Dublet electronic
Dubletul de electroni este perechea de electroni care ocupă același orbital , dar au rotiri opuse (în conformitate cu principiul de excludere Pauli ).
Electronii unui dublet de electroni pot fi:
- împărțit de doi atomi în legătura covalentă (pură sau polară)
- nepartajat (sau nepereche)
- electronii de bază , dacă aceștia ocupă nivelurile cele mai interioare de energie ale unui atom, adică dacă nu sunt electroni de valență .
Doi atomi pot împărți până la trei perechi de electroni ( triplă legătură ). De fapt, dacă în cel mai exterior nivel de energie al unui atom există 8 electroni, se spune că atomul are un „octet complet” și, conform regulii octetului, atomul în cauză va fi stabil. De exemplu, gazele nobile au un octet complet și, prin urmare, sunt foarte stabile. [1]
Pereche singuratică
O pereche de electroni nepartajați (sau un dublet de electroni neperecheați sau o pereche singură sau o pereche singură ) este indicată printr-un punct (":") sau cu o linie de bare.
Perechile solitare pot crea legături date .
Fiind alcătuite din sarcini negative (electroni), acestea au o acțiune respingătoare față de celelalte grupuri ale moleculei. Din acest motiv, de exemplu, molecula de amoniac (NH 3 ) nu este de tip plan, deoarece atomii de hidrogen sunt respinși de dubletul nepartajat prezent pe atomul de azot . Rezultă că unghiul format de legăturile dintre hidrogen și azot în molecula de amoniac nu este de 120 ° (ceea ce ar fi cel al unei molecule plane formate dintr-un atom central și trei atomi atașați la acesta), ci 107 °.
Notă
- ^ Deși există unii compuși de gaze nobile .
Elemente conexe
- Electron
- Regula octetului
- Structura lui Lewis
- Electron nucleu
- Legătură chimică
- Electrondonator
- Electron nepereche
linkuri externe
- ( EN ) Dublet electronic , pe Encyclopedia Britannica , Encyclopædia Britannica, Inc.