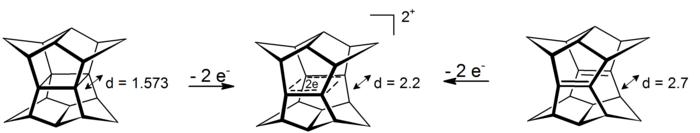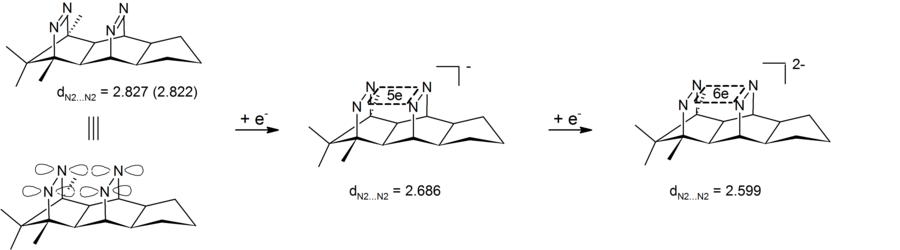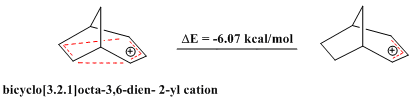Homoaromaticitate
Homoaromaticity în chimia organică este un caz particular al aromaticitate în care conjugarea normală este întreruptă de prezența unuia sau mai multor singur sp3 hibridizate atomi de carbon. Compușii care conțin acest tip de legătură aromatică se numesc compuși homoaromatici . Prezența unui centru sp 3 întrerupe suprapunerea dintre orbitalii p ai atomilor adiacenți în mod tradițional necesari pentru a avea un compus aromatic , totuși compușii homoaromatici posedă o stabilitate termodinamică remarcabilă și multe proprietăți spectroscopice, magnetice și chimice tipice compușilor aromatici, indicând faptul că suprapunerea Orbitalii p reușesc aparent să depășească centrul sp 3 formând în orice caz un ciclu continuu de π electroni. [1]
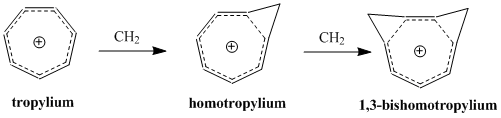
Conceptul de homoaromaticitate a fost introdus de Saul Winstein în 1959 cu studiile sale asupra cationului tris-homociclopropenil. [2] De atunci au existat multe studii asupra acestor specii; sunt cunoscuți atât compușii homoaromatici cationici, cât și cei anionici, în timp ce moleculele neutre par mai puțin frecvente. [3] [4] Cationul "homotropilic" (C 8 H 9 + ) este unul dintre cei mai studiați compuși homoaromatici.
Nomenclatură
Termenul "homoaromaticitate" derivă din asemănarea în structură dintre compușii homoaromatici și compușii aromatici analogi. [2] Nomenclatura IUPAC necesită utilizarea prefixelor bis-, tris- etc. să descrie compuși homoaromatici care conțin doi, trei etc. centre sp 3 separate care perturbă conjugarea sistemului aromatic.
fundal
Conceptul de homoaromaticity rezultă din dezbaterea care a avut loc în 1950 pe structura carbocationilor non-clasice (tetra sau pentacoordinate) , în comparație cu trivalenți clasic carbocationilor . [5] Saul Winstein , un susținător al modelului non-clasic, a fost primul care a descris homoaromaticitatea prin studierea cationului subțire cu 3 biciclete [3.1.0]. 
Într-o serie de experimente de acetoliză, Winstein și colaboratorii au observat că reacția de solvoliză a fost mai rapidă atunci când grupul tosilat părăsit se afla în poziția ecuatorială . Viteza de reacție diferită a fost atribuită asistenței ankimerice invocată de izomerul "cis". Acest rezultat a susținut o structură non-clasică a cationului. [6]
Winstein a observat ulterior că acest model neclasic al cationului subțire cu 3 biciclete [3.1.0] îl face similar cu binecunoscutul cation ciclopropenil aromatic. Ca și în cationul ciclopropenil, sarcina pozitivă este delocalizată la trei atomi de carbon echivalenți care conțin doi electroni π. Această configurație electronică îndeplinește regula lui Hückel pentru aromaticitate, deoarece sunt necesari 4n + 2 π electroni. Winstein remarcat faptul că singura diferență fundamentală între cationul propenil aromatic și cation subțire nonclassical a fost că , în acest din urmă caz, conjugarea a fost întreruptă de trei unități CH2. Numele „tris-homociclopropenil” a fost apoi propus pentru tris-homo corespunzător al cationului ciclopropenil.
Exemple de compuși homoaromatici
După descoperirea primilor compuși homoaromatici, cercetătorii au continuat să sintetizeze noi compuși homoaromatici care posedă o stabilitate similară compușilor aromatici de bază. Există diferite clase de compuși homoaromatici, prevăzuți teoretic și obținuți experimental.
Cationi homo-aromatici
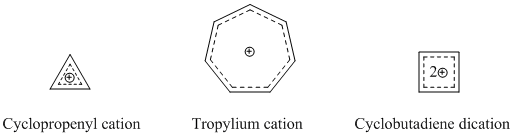
Cationii homo-aromatici sunt cele mai cunoscute și mai stabilite specii homoaromatice. După cum sa menționat deja, cationul de homotropie este unul dintre cei mai cunoscuți și cei mai studiați. Mulți compuși cationici homoaromatici se bazează pe cationi ciclopropenil, tropiliu sau ciclobutadienic, deoarece acești compuși au un puternic caracter aromatic.
O altă specie bine cunoscută este cationul norbornen-7-il, ale cărui proprietăți homoaromatice au fost dovedite atât teoretic, cât și experimental. [7]
Un caz interesant de bis-homoaromaticitate σ este reprezentat de dicările păgânilor . În aceste sisteme cu 4 centre și 2 electroni, delocalizarea este localizată în planul definit de cei patru atomi de carbon din centrul structurii. (Ciclopropanul este un prototip de aromaticitate σ și câștigă aproximativ 11,3 kcal / mol din acest efect. [8] ) Dicările pot fi obținute fie prin oxidarea pagodanului, fie prin oxidarea bis-seco-dodecaedradienei corespunzătoare: [9]
Specie neutră homoaromatică
Există multe clase de compuși homoaromatici neutri, dar se discută mult dacă prezintă sau nu adevărat caracter homoaromatic. Cea mai simplă clasă este cea a mono-homoaromaticelor; una dintre cele mai simple este cicloheptatriena . Există o serie de mono-homoaromatice mai complexe. Un exemplu particular este un derivat C60 care conține o singură punte de metilen. Analizele UV și RMN au arătat că caracterul aromatic al acestei specii nu este distrus prin adăugarea unei legături homoconjugate și, prin urmare, compusul este categoric homoaromatic. [10]
Bis-homoaromatic
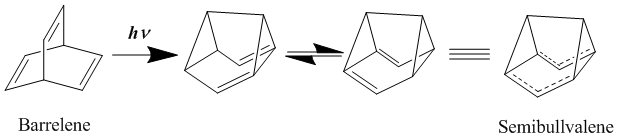
De multă vreme s-a crezut că cele mai bune exemple de homoaromatice neutre sunt compușii bis- homoaromatici , cum ar fi barrelena și semibullvalena. Acesta din urmă a fost sintetizat pentru prima dată în 1966. [11] Semibullvalenul are o structură care ar trebui să se împrumute bine la omoaromaticitate, deși s-a dezbătut mult dacă derivații semibullvaleni au cu adevărat o delocalizare care îi clasifică drept homoaromatică neutră. Stare fundamentală. S-au făcut încercări de a stabiliza în continuare structura de tranziție delocalizată folosind grupuri de donatori sau acceptori de electroni, constatând că bariera de activare a rearanjării poate fi redusă, dar nu eliminată. [12] [13] O adevărată structură de stare de bază delocalizată homoaromatică a fost obținută prin introducerea tensiunii în inele pentru a destabiliza starea de bază a structurilor localizate. [14]
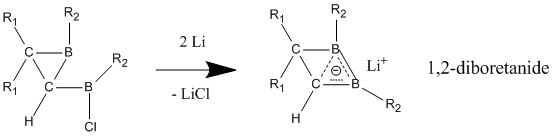
Alți compuși considerați homoaromatici neutri sunt 1,2-diboretanii și derivații înrudiți. La acești compuși care conțin bor, starea delocalizată este mult mai stabilizată decât starea localizată, sugerând omoaromaticitatea compusului. [15] Atașarea grupurilor de donatori de electroni la cei doi atomi de bor favorizează modelul clasic cu legături localizate. Caracterul homoaromatic este mai evident prin atașarea grupurilor de acceptori de electroni la atomii de bor; în acest caz compusul adoptă o structură delocalizată neclasică.
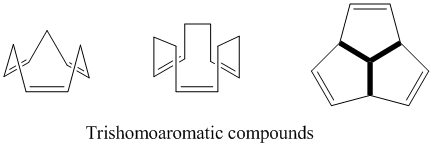
Tris-homoaromatic
După cum indică și numele, acești compuși conțin trei punți de metilen care perturbă conjugarea sistemului aromatic. Ca și în cazul semibullvalenului, se discută mult cât de mult acești compuși sunt homoaromatici. În teorie sunt homoaromatic, dar delocalizarea duce la o stabilizare care nu depășește 5% din cea a benzenului. [16]
Anioni homo-aromatici
Spre deosebire de homoaromatica neutră, homoaromatica anionică este de obicei considerată „adevărată” homoaromatică. Acești compuși anionici sunt preparați în mod tipic din compuși părinți neutri prin reducere cu litiu metalic. Derivații 1,2-diboretanidei au un puternic caracter homoaromatic în legătura lor cu doi electroni pe trei atomi (bor, bor, carbon); legăturile C - B sunt mai scurte decât la speciile neutre clasice corespunzătoare. [17] În aceste 1,2-diboretanide inelul poate fi extins cu substituenți diferiți, menținând în același timp un anumit grad de homoaromaticitate.
Alți anioni homoaromatici sunt dianionii compușilor bis-diazenici, care conțin un ciclu cu patru atomi (cei patru azoti) cu șase electroni. Scurtarea distanței transanulare azot-azot a fost observată experimental, demonstrând că acești bis-diazeni dianionici sunt anioni bis-homoaromatici. O caracteristică particulară a acestor sisteme este că ciclul electronilor delocalizați se află în planul σ definit de cei patru azoti. Aceste specii sunt, prin urmare, primele exemple de σ bis-homoaromaticitate la 4 centri și 6 electroni. [18] [19]
Omoantiaromaticitate
Sunt de asemenea cunoscute cazuri de compuși homoantiaromatici, precum și compuși aromatici și compuși antiaromatici . (Compușii aromatici prezintă o stabilitate excepțională, în timp ce compușii antiaromatici sunt relativ instabili, deoarece au un ciclu cu 4n electroni π delocalizați și, prin urmare, se abat de la regula lui Hückel.) Cationul de bicicletă [3.2.1] octa-3,6- dien-2- yl conține doar 4 π electroni și, prin urmare, este „bis-homoantiaromatic”. Calculele teoretice confirmă faptul că acest cation este mai puțin stabil decât cationul alil corespunzător. [20]
În mod similar, calculele teoretice și analizele RMN au arătat că cationul 2- (4'-fluorofenil) biciclo [3.2.1] octa-3,6-dien-2-il este cation homoantiaromatic în raport cu cationul alil corespunzător. [20]
Notă
- ^ McNaught și Wilkinson
- ^ a b Winstein 1959
- ^ Williams 2001
- ^ Freeman 2005
- ^ Olah 1972
- ^ Winsteinet al. 1959
- ^ Carey și Sundberg 2000
- ^ Exner și von Ragué Schleyer 2001
- ^ Prinzbach și colab. 1995
- ^ Suzuki și colab. 1992
- ^ Zimmerman și Grunewald
- ^ Dewar și Lo 1971
- ^ Hoffmann și Stohrer
- ^ Griffiths și colab. 2011
- ^ Steiner și colab. 1994
- ^ Martin și Mayer
- ^ Steiner și colab. 1996
- ^ Exner și colab. 1998
- ^ Exner și colab. 2000
- ^ a b Volz și Shin
Bibliografie
- ( EN ) FA Carey și RJ Sundberg, Advanced Organic Chemistry: Part A: Structure and Mechanism , New York, Kluwer Academic / Plenum Publishers, 2000, pp. 327-334, ISBN 978-0-387-68346-1 .
- ( EN ) MJS Dewar și DH Lo, stări fundamentale ale moleculelor legate de .sigma. XIV. Aplicarea partiției energetice la metoda MINDO / 2 și un studiu al rearanjării Cope , în J. Am. Chem. Soc. , Vol. 93, nr. 26, 1971, pp. 7201–7207, DOI : 10.1021 / ja00755a014 .
- ( EN ) K. Exner, D. Hunkler, G. Gescheidt și H. Prinzbach, <1910 :: AID-ANIE1910> 3.0.CO; 2-D Do Nonclassical, Cyclically Delocalized 4N / 5e Radical Anions and 4N / 6e Dianions Exist ? - Reducerea cu unul și doi electroni a bis-diazenelor proximale , Synperiplanar , în Angew. Chem. Int. Ed. Engl. , vol. 37, n. 13-14, 1998, pp. 1910–1913, DOI : 10.1002 / (SICI) 1521-3773 (19980803) 37: 13/14 <1910 :: AID-ANIE1910> 3.0.CO; 2-D .
- ( EN ) K. Exner, O. Cullmann, M. Vögtle, H. Prinzbach și alții, Delocalizarea electronică ciclică în plan (σ-Bishomoaromaticity) în anioni radicali 4N / 5e și dianioni 4N / 6e - Generare, structuri, proprietăți, Ion-Pairing și calcule , în J. Am. Chem. Soc. , Vol. 122, nr. 43, 2000, pp. 10650–10660, DOI : 10.1021 / ja0014943 .
- ( EN ) K. Exner și P. von Ragué Schleyer, Theoretical Bond Energies: A Critical Evaluation , în J. Phys. Chem. A , vol. 105, nr. 13, 2001, pp. 3407–3416, DOI : 10.1021 / jp004193o .
- ( EN ) PK Freeman, Neutral Homoaromaticity in Some Heterocyclic Systems , în J. Org. Chem. , vol. 70, nr. 6, 2005, pp. 1998–2001, DOI : 10.1021 / jo040250o .
- ( EN ) PR Griffiths, DE Pivonka și RV Williams, The Experimental Realization of a Neutral Homoaromatic Carbocycle , in Chem. Eur. J. , vol. 17, n. 33, 2011, pp. 9193–9199, DOI : 10.1002 / chim.201100025 .
- ( EN ) R. Hoffmann și WD Stohrer, Cope rearrangement revisited , în J. Am. Chem. Soc. , Vol. 93, nr. 25, 1971, pp. 6941–6948, DOI : 10.1021 / ja00754a042 .
- ( EN ) HD Martin și B. Mayer, Efecte de proximitate în chimia organică? Investigația spectroscopică fotoelectronică a interacțiunilor fără legături și transanulare , în Angew. Chem. Int. Ed. Engl. , vol. 22, n. 4, 1983, pp. 283-314, DOI : 10.1002 / anie . 198302831 .
- AD McNaught și A. Wilkinson, homoaromatic , pe IUPAC. Compendiu de terminologie chimică, ed. A II-a. („Cartea de aur”) , Blackwell Scientific Publications, 2006. Accesat la 5 februarie 2017 .
- (RO) GA Olah, carbocații stabile. CXVIII. Conceptul general și structura carbocațiilor bazate pe diferențierea ionilor de carbeniu trivalenți (clasici) de la penta- legată în trei centre a ionilor de carboniu tetracoordonat (neclasic). Rolul carbocațiilor în reacțiile electrofile , în J. Am. Chem. Soc. , Vol. 94, nr. 3, 1972, pp. 808–820, DOI : 10.1021 / ja00758a020 .
- ( EN ) H. Prinzbach, G. Gescheidt, H.-D. Martin, R. Herges și colab., Delocalizarea ciclică a electronilor în cuști de hidrocarburi: Pagodani, izopagodani, (bisseco / seco-) dodecahedradienes , în Pure Appl. Chem. , vol. 67, nr. 5, 1995, pp. 673–682, DOI : 10.1351 / pac199567050673 .
- ( EN ) D. Steiner, C. Balzereit, HJR Winkler, N. Stamatis și alții, 1,2-Diboretanes și 1,2-Diborolanes non-clasici , în Angew. Chem. Int. Ed. Engl. , vol. 33, nr. 22, 1994, pp. 2303-2306, DOI : 10.1002 / an . 199423031 .
- (RO) D. Steiner, H. Winkler, C. Balzereit, T. Happel și alții, 1,2-Diboretanides: 2π-Electron Homoaromatic Compuși cu bariere ridicate inversiune , în Angew. Chem. Int. Ed. Engl. , vol. 35, nr. 17, 1996, pp. 1990-1992, DOI : 10.1002 / an . 199619901 .
- ( EN ) T. Suzuki, Q. Li, KC Khemani și F. Wudl, Dihidrofulleroid H3C61: sinteză și proprietăți ale fulleroidului părinte , în J. Am. Chem. Soc. , Vol. 114, nr. 18, 1992, pp. 7301–7302, DOI : 10.1021 / ja00044a055 .
- ( EN ) H. Volz și J. Shin, Bicyclo [3.2.1] octa-3,6-dien-2-il Cation: A Bishomoantiaromate , în J. Org. Chem. , vol. 71, nr. 6, 2006, pp. 2220–2226, DOI : 10.1021 / jo0515125 .
- ( EN ) RV Williams, Homoaromaticity , în Chem. Rev. , vol. 101, nr. 5, 2001, pp. 1185-1204, DOI : 10.1021 / cr9903149 .
- ( EN ) S. Winstein, Structuri homo-aromatice , în J. Am. Chem. Soc. , Vol. 81, nr. 24, 1959, pp. 6524–6525, DOI : 10.1021 / ja01533a052 .
- ( EN ) S. Winstein, J. Sonnenberg și L. De Vries, The tris-homocyclopropenyl cation. , în J. Am. Chem. Soc. , Vol. 81, nr. 24, 1959, pp. 6523–6524, DOI : 10.1021 / ja01533a051 .
- ( RO ) HE Zimmerman și GL Grunewald, The Chemistry of Barrelene. III. O fotoizomerizare unică la Semibullvalene , în J. Am. Chem. Soc. , Vol. 88, nr. 1, 1966, pp. 183–184, DOI : 10.1021 / ja00953a045 .