Clorură de beriliu
| Clorură de beriliu | |
|---|---|
| Caracteristici generale | |
| Formula moleculară sau brută | BeCl 2 |
| Masa moleculară ( u ) | 79,9182 g / mol |
| Aspect | cristale albe |
| numar CAS | |
| Numărul EINECS | 232-116-4 |
| PubChem | 24588 |
| ZÂMBETE | [Be+2].[Cl-].[Cl-] |
| Proprietăți fizico-chimice | |
| Solubilitate în apă | 15,1 g / 100 ml (20 ° C) |
| Temperatură de topire | 399 ° C (672,15 K) |
| Temperatura de fierbere | 520 ° C (793,15 K) |
| Informații de siguranță | |
| Simboluri de pericol chimic | |
   | |
| Pericol | |
| Fraze H | 301 - 315 - 317 - 319 - 330 - 335 - 350i - 372 - 411 |
| Sfaturi P | 201 - 260 - 273 - 280 - 284 - 301 + 310 [1] |
Clorură de beriliu este un compus având formula BeCl 2 formată de metal beriliu (Be) și halogen clor (CI); la temperatura camerei apare ca un solid cristalin alb. Se topește și se vaporizează la temperaturi destul de scăzute (405 ° C și respectiv 520 ° C) spre deosebire de halogenurile celorlalte metale alcalino-pământoase. Este solubil în solvenți organici precum alcoolul și eterul. Aceste caracteristici indică caracterul esențial covalent al compusului. Se hidrolizează în apă pentru a forma [Be (H 2 O) 4 ] Cl 2 .
Caracteristici structurale
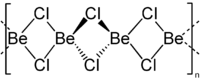
Caracterul covalent (în ciuda diferenței mari de electronegativitate între Be și Cl) se datorează prezenței unui cation cu o încărcare mare (2+) și cu rază mică, aproape de un anion foarte polarizabil (Cl - ) [2] . În formă solidă, clorura de beriliu are o structură polimerică unidimensională formată din celule tetraedrice unite de margini; structura tetraedrică este distorsionată, cu unghiurile Cl-Be-Cl de 109 ° și Be-Cl-Be de 71 ° [3] :
Fiecare Be se leagă cu patru atomi de clor:
- doi se leagă prin electroni nepereche,
- Be apoi prezintă orbitali goi și acceptă perechi de electroni din alți doi atomi de clor.
În faza gazoasă poate apărea atât ca monomer, cât și ca dimer. Forma dimera este prezentă în procente mari numai la temperaturi apropiate de cea de vaporizare, de exemplu 20% la 560 ° C [3] . Monomerii au geometrie liniară cu un unghi de legătură de 180 ° ca dovadă a caracterului covalent parțial al legăturilor: molecula BeCl 2 este adesea utilizată în educația chimică pentru a arăta geometria liniară în teoria VSEPR .
Sinteza compusului
Oxidul de beriliu reacționează cu carbonul și clorul la 600 - 800 ° C [2] :
- BeO (s) + C (s) + Cl 2 (g) → BeCl 2 (g) + CO (g)
BeCl 2 pot fi de asemenea preparate prin tratarea beriliului metalic cu acid clorhidric :
- Fii + 2 HCl → BeCl 2 + H 2
Notă
- ^ Sigma Aldrich; rev. din 30.11.2012
- ^ a b P. Atkins, L. Jones (1998) "Chimie generală", Zanichelli, ISBN 88-08-09184-8
- ^ a b FA Cotton, G. Wilkinson (1980) Chimie anorganică avansată - Un text cuprinzător , J. Wiley și sons ISBN 0-471-02775-8 .
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere despre clorură de beriliu
Wikimedia Commons conține imagini sau alte fișiere despre clorură de beriliu