Teoria VSEPR
Teoria VSEPR (acronim din engleza Valence Shell Electron Pair Repulsion , adică repulsia perechilor de electroni în coaja de valență , pronunțată ocazional „vesper” [1] ) este utilizată ca metodă de evaluare a aranjamentului geometric al atomilor unei molecule în spațiu și se bazează pe faptul că domeniile electronice tind să fie cât mai îndepărtate posibil. Acest lucru este în conformitate cu legea lui Coulomb , conform căreia sarcinile electrice cu semn egal se resping reciproc.
Această teorie se bazează pe ipoteza că distribuția legăturilor în jurul unui atom depinde de numărul total de perechi de electroni care îl înconjoară, atât cele implicate în legături chimice, cât și cele care nu sunt implicate în nicio legătură chimică (numite perechi solitare sau „perechi solitare”) . Aceste perechi de electroni sunt dispuse în spațiu în așa fel încât să reducă la minimum forțele de respingere reciprocă. Forțele de respingere dintre două perechi care nu se leagă sunt mai puternice decât forțele de respingere dintre o pereche care nu se leagă și o pereche de legătură, care la rândul lor sunt mai puternice decât forțele de respingere dintre două perechi de legături.
Principalele puncte ale teoriei
- Perechile de electroni din învelișul de valență al atomului central se resping reciproc;
- Aceste perechi de electroni tind să ocupe cea mai potrivită poziție pentru a minimiza repulsia, maximizând astfel spațiul dintre electroni;
- Coaja de valență este considerată ca o sferă pe a cărei suprafață se află electronii, care va menține distanța maximă între ei;
- O legătură multiplă este considerată a fi o singură pereche de electroni, deci două sau trei perechi de electroni ai unei legături multiple sunt considerate a fi o super pereche de electroni;
- Modelul VSEPR este aplicabil atunci când două sau mai multe structuri de rezonanță pot reprezenta o moleculă.
Sunt considerate trei tipuri de respingere între electronii unei molecule:
- Repulsia dintre perechea singuratică și perechea singuratică (din moment ce „ engleză lone pair-lone pair, lp-lp).
- Repulsia dintre perechea singuratică și perechea de legătură pereche singură (lp-bp).
- Repulsia dintre perechea de electroni care leagă și perechea de legătură (bp-bp).
O moleculă trebuie să minimizeze și să stabilizeze orice fel de respingere electronică; atunci când acest lucru nu este posibil, este de preferat să se ia în considerare o respingere slabă (care determină o ușoară abatere de la configurația ideală).
Repulsia dintre perechea solitară și perechea solitară (lp-lp) este considerată mai puternică, ocupând un volum mai mare de spațiu, decât cea dintre perechea solitară și perechea de electroni care leagă (lp-bp). La rândul său, repulsia dintre perechea de electroni care leagă și perechea de electroni de legătură (bp-bp) este mai slabă și, prin urmare, mai stabilă decât repulsia dintre perechea singuratică și perechea solitară (lp-lp) sau între perechea solitară și legătura perechii de electroni (lp -lp)> (lp-bp)> (bp-bp).
Comparație cu alte teorii și evoluții
Teoria VSEPR este adesea comparată și contrastată cu teoria legăturii de valență (deși nu este considerată o parte a acesteia din urmă), care definește geometria moleculară prin analiza orbitalelor care sunt energetic adecvate pentru a realiza o legătură. Teoria legăturii de valență se referă la formarea legăturilor sigma și pi .
Teoria orbitalilor moleculari, pe de altă parte, este un alt model care ne permite să prezicem dispunerea spațială a atomilor și electronilor care alcătuiesc molecule și ioni poliatomici.
Cu toate acestea, teoria VSEPR a fost adesea criticată pentru că nu are descoperiri cantitative, chiar dacă structurale corecte, pentru moleculele formate din legături covalente.
Mai mult, au fost dezvoltate teorii ale câmpului forței moleculare bazate pe teoria VSEPR. [2]
Metoda AX
Metoda AX de numărare a electronilor este frecvent utilizată pentru aplicarea teoriei VSEPR. Acronimul AX reprezintă atomul central cu litera A și are întotdeauna o valoare implicită de 1. X reprezintă câte legături sigma se formează între atomul central și atomii legați de acesta. Legăturile covalente multiple (duble, triple, etc.) se numără X. În cele din urmă, E reprezintă numărul de perechi solitare de electroni ( pereche singură ) prezente în învelișul de valență al atomului central. Suma lui X și E , definită ca un număr steric , este, de asemenea, asociată cu numărul total de orbitali hibridizați considerați de teoria legăturii de valență .
| Număr steric | Geometrie moleculară cu 0 perechi solitare de electroni | 1 cuplu singuratic | 2 cupluri singuratice | 3 cupluri solitare |
|---|---|---|---|---|
| 2 | Liniar | |||
| 3 |  Trigonal planar |  Unghiular | ||
| 4 | 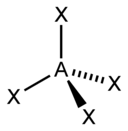 Tetraedric |  Piramida trigonală |  Unghiular | |
| 5 |  Trigonal bipiramidal | 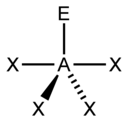 Leagăn ( balansoar ) |  În formă de T (în formă de T ) |  Liniar |
| 6 | 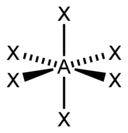 Octahedral |  Piramida pe bază de pătrat |  Pătrat plan | |
| 7 |  Bipyramid pe bază de pentagonală | 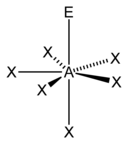 Piramidă cu bază pentagonală | 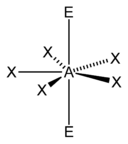 Pentagonal |
| Tipul moleculei | Formă | aranjament de electroni † | Geometrie ‡ | Exemple |
|---|---|---|---|---|
| AXA 1 ȘI n | Diatomică | | | HF , O 2 |
| AXA 2 ȘI 0 | Liniar | | | BeCl 2 , HgCI2 , CO 2 |
| AXA 2 ȘI 1 | Unghiular |  |  | NO 2 - , SO 2 , O 3 |
| AXA 2 ȘI 2 | Unghiular | 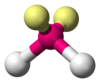 |  | H 2 O , OF 2 |
| AXA 2 ȘI 3 | Liniar |  | | XeF 2 , I 3 - |
| AXA 3 ȘI 0 | Trigonal planar |  |  | BF 3 , CO 3 2− , NO 3 - , SO 3 |
| AXA 3 ȘI 1 | Piramida trigonală |  |  | NH 3 , PCI3 |
| AXA 3 ȘI 2 | În formă de T |  |  | ClF 3 , BrF 3 |
| AX 4 ȘI 0 | Tetraedric | 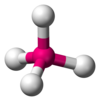 |  | CH 4 , PO 4 3− , SO 4 2− , ClO 4 - |
| AXA 4 ȘI 1 | Leagăn (balansoar) |  | 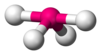 | SF 4 |
| AX 4 ȘI 2 | Pătrat (plat) |  |  | XeF 4 |
| AXA 5 ȘI 0 | Trigonal bipiramidal |  |  | PCl 5 |
| AXA 5 ȘI 1 | Piramida pe bază de pătrat | 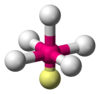 |  | ClF 5 , BrF 5 |
| AXA 5 ȘI 2 | Pentagonal |  |  | XeF 5 - |
| AXA 6 ȘI 0 | Octahedral | 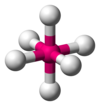 |  | SF 6 |
| AXA 6 ȘI 1 | Piramidă cu bază pentagonală |  |  | XeF 6 |
| AX 7 ȘI 0 | Bipiramidă cu bază pentagonală | 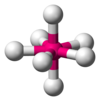 |  | DACĂ 7 |
Exemple
Molecula de dioxid de carbon (CO 2 ) se va aranja în spațiu într-un mod liniar (omițând cele 4 perechi de electroni fără legătură) având oxigenul la capete obținând astfel cea mai mare distanță posibilă între cele două legături duble C = O (și deci cea mai mică respingere dintre ele) cu un unghi de 180 °.
Clorura de beriliu are, de asemenea , o formă liniară.
În metan, cei patru atomi de hidrogen sunt dispuși ca vârfuri ale unui tetraedru obișnuit cu atomul de carbon în centru. Unghiurile de legătură sunt de 109,5 °, deoarece există de fapt patru perechi de electroni de legătură, repulsiile sunt aceleași pentru toate legăturile.
În amoniac, pe de altă parte, există trei perechi de electroni de legătură și o pereche de singuri, repulsia de perechi de legături singulare este mai mare decât cea dintre perechile de legături, tetraedrul nu este deci regulat și unghiul HNH devine 107, 3.
În cele din urmă, în apă există două perechi solitare și două perechi de legături, unghiul HOH este de 104 °.
Notă
- ^ https://neologisms.rice.edu/index.php?a=term&d=1&t=23204
- ^ Caseta VGS. Journal of Molecular Modeling, 1997, 3, 124-141.
Elemente conexe
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere despre teoria VSEPR
Wikimedia Commons conține imagini sau alte fișiere despre teoria VSEPR
linkuri externe
- ( EN ) Teoria VSEPR , pe Encyclopedia Britannica , Encyclopædia Britannica, Inc.
| Controlul autorității | GND ( DE ) 4273775-8 |
|---|
