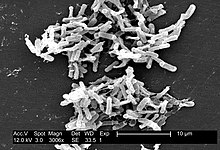
Clostridioides difficile
| Clostridioides difficile | |
|---|---|
| Clostridioides difficile | |
| Clasificare științifică | |
| Domeniu | Prokaryota |
| Regatul | Bacterii |
| Phylum | Firmicute |
| Clasă | Clostridia |
| Ordin | Clostridiales |
| Familie | Clostridiaceae |
| Tip | Clostridioide |
| Specii | C. dificil |
| Nomenclatura binominala | |
| Clostridioides difficile Lawson & Rainey, 2016 | |
Clostridioides difficile , cunoscut odinioară sub numele de Clostridium difficile , [1] este o bacterie formatoare de spori aparținând familiei Clostridiaceae . Este o tijă, Gram + , anaerobă. La fel ca alte specii înrudite, atunci când produce toxine specifice, poate fi patogenă pentru oameni .
Pe larg difuzat în sol, este prezent și în tractul gastro-intestinal al diferitelor animale: câini, pisici, cai, porci, rozătoare. C. difficile face parte din flora saprofită normală a intestinului uman și colonizează între 3% și 15% dintre adulții sănătoși. Poate fi izolat la 80% din fecalele copiilor cu vârsta de până la 1 an, colonizare favorizată de imaturitatea florei bacteriene intestinale.
Specia C. difficile este definită de un pangenom mare și divers cu niveluri extreme de plasticitate evolutivă care a fost modelată pe perioade lungi de timp prin fluxul de gene și recombinare , adesea între linii divergente. Sute de tulpini de C. difficile diferite au fost izolate , nu toate toxigenice. Evoluția continuă a C. difficile ca răspuns la activitățile de mediu și antropice a condus la apariția rapidă și răspândirea la nivel mondial a descendențelor clonale virulente.
Infecția cu Closteridioides difficile este cea mai frecventă cauză a infecțiilor nosocomiale în unele țări și este deașteptat să provoace aproximativ 15.000 de decese pe an în SUA și 3.700 în UE / AEM. [2] [3] [4]
fundal
Hall și O'Toole, în materialul fecal al nou-născuților, în 1935 au identificat bacteria: Bacillus difficile , numită astfel pentru dificultatea întâmpinată în izolare și pentru creșterea extrem de lentă pe mediul de cultură. În 1970 a fost redenumit Clostridium difficile . [5] [6] [7] [8] În timp ce primul caz de colită pseudomembranoasă a fost documentat de Finney în 1893 într-o autopsie a unei femei care a murit din cauza diareei hemoragice post-chirurgicale, care a prezentat pseudomembranele asemănătoare difteriei în colon . [9] [10]
În 1968, s-a observat colită pseudomembranoasă severă, care pune viața în pericol, la hamsteri, utilizați în mod normal pentru studiul C. difficile , tratați cu antibioticul lincomicină . [10]
În 1970 animalele tratate cu antibiotice aveau o cantitate mare de toxină patogenă produsă de C. difficile în materiile fecale, identificând cu toxina cauza principală a manifestărilor clinice ale patologiei colitei pseudomembranoase. [10] În 1980, au fost identificate două toxine distincte (A și B) produse de C. difficile . [11] Toxinele A și B sunt transcrise pe un locus de patogenitate care cuprinde cinci gene : două gene ale toxinei, tcdA (toxina A) și tcdB (toxina B) și trei gene reglatoare, dintre care una (tcdC) codifică un regulator negativ al toxinei transcriere. [12] [13]
Prima secvență genomică completă a unei tulpini de C. difficile a fost publicată pentru prima dată în 2005 de Institutul Sanger din Marea Britanie. Aceasta a fost tulpina 630, o tulpină virulentă și rezistentă la medicamente, izolată în Elveția în 1982.
Specia a fost transferată din genul Clostridium în Clostridioides în 2016, dându-i astfel binomul Clostridioides difficile . [14] [15] [16] Acest nou nume reflectă diferențele taxonomice dintre această specie și membrii genului Clostridium , menținând în același timp abrevierea C. difficile . [17]
Bacteriologie

Găsim spori dificili de Clostridioides în sol, spitale și case pentru bătrâni. Forma activă a bacteriilor se găsește numai în tractul intestinal. La microscop, după colorarea Gram, sunt bacili alungiți cu un capăt ușor umflat. Germenul în sine este gram pozitiv. Cultura sa este optimă într-un mediu de bază de agar la 37 ° C. Când condițiile se îngreunează, bacteriile produc spori care sunt rezistenți la uscare, la temperaturi extreme și la multe substanțe chimice și dezinfectante. [18] [19] .
Sporii sunt metaboliți latenți și foarte rezistenți la procedurile standard de dezinfecție, permițându-le să persiste perioade lungi în mediu. Sporii ingerați de gazdele sensibile se pot reactiva (sau germina) ca răspuns la acizi biliari specifici din intestinul subțire și pot reveni la un stil de viață activ pentru a produce toxine și a provoca boli. Sporii sunt extrem de transmisibili și responsabili de contaminarea mediului. Clostridioides difficile este un germen al florei digestive comensale. De asemenea, detectată în fecalele sugarilor, este adesea asimptomatică datorită incapacității toxinei, în tulpinile toxigene, de a se lega de receptorii enterocitelor încă imature. Unele dintre mutațiile sale emergente sunt multi-rezistente (s-au adaptat la majoritatea antibioticelor) și, în cazul tulburărilor florei digestive cauzate de administrarea de antibiotice, se pot dezvolta semnificativ. Marea variabilitate a diferitelor tulpini îngreunează caracterizarea lor moleculară. Când în 2003 analiza moleculară a condus la identificarea unei tulpini de C. difficile caracterizate ca grupul BI prin analiza de endonuclează de restricție, NAP1 (câmp pulsat nord-american) prin electroforeză cu gel de câmp pulsat și ribotipul 027, „noua” tulpină a fost denumită „ C. difficile BI / NAP1 / 027 ". Diferita terminologie reflectă tehnicile predominante utilizate pentru tipizarea epidemiologică. [20] [21] [22]
Există atât tulpini toxigenice (adică producătoare de toxine), cât și tulpini netoxigenice de C. difficile , dar numai formele toxigene provoacă boli la om.
Bacteriile produc citotoxine polipeptidice cu masă moleculară mare, A și B. Unele tulpini produc doar una dintre toxine, altele produc ambele. Toxina A provoacă o reacție inflamatorie care implică hipersecreție de lichide și necroză hemoragică prin activarea eliberării citokinelor de către neutrofile. Citotoxina B depolimerizează actina, principala proteină a citoscheletului și, astfel, ajută la distrugerea țesuturilor. Acțiunea combinată a toxinelor provoacă necroză a epiteliului superficial și edem (umflarea fluidelor) în zonele afectate ale intestinului. Proliferarea C. difficile este în mod normal contracarată de microflora intestinală normală, despre care se crede că inhibă atașarea bacteriei și a toxinelor sale de pereții intestinali. Modificarea echilibrului microbian intestinal cu antibioterapie și expunerea crescută la bacterii în spital permite C. difficile colonizarea indivizilor sensibili. Mai mult, s-a demonstrat că concentrațiile subinhibitorii de antibiotice promovează producția crescută de toxine de către C. difficile . [23] [24] [25] [26] [27] [28]
Tulpini
C. difficile este taxonomic distinct de multe alte clostridii bine cunoscute, cu o structură de populație diversă cuprinzând sute de tulpini diferite împrăștiate pe cel puțin 6 clade filogenetice. Există atât tulpini toxigenice (adică producătoare de toxine), cât și tulpini netoxigenice de C. difficile , dar numai formele toxigene provoacă boli la om. Patogenitatea depinde de fapt de prezența toxinelor A (TcdA, enterotoxină) și B (TcdB, citotoxină). Au fost identificate peste 400 de tulpini toxigene diferite. [29]
Toate tulpinile toxigene exprimă toxina TcdB, cu sau fără toxina TcdA. De fapt, toxina B are o activitate citotoxică mai puternică decât toxina A. Ambele toxine supraviețuiesc în mediul acid al stomacului și sunt capabile să se lege de suprafața celulelor epiteliale ale mucoasei intestinale unde sunt interiorizate și unde catalizează glicozilarea unor proteine citoplasmatice, cu moartea celulară ulterioară. O a treia toxină a cărei patogenitate nu este clară, toxina binară (CDT), este produsă de unele tulpini de C.difficile . S-a demonstrat că această toxină crește virulența C. difficile prin ribozilarea adenozin difosfat-actină, inducând formarea de proeminențe de microtubuli în celule facilitând adeziunea bacteriei la suprafața celulei. Toxina CDT poate fi, de asemenea, prezentă în tulpini în care toxinele A și B sunt absente, găsite la pacienții asimptomatici. [30]
Există tulpini care produc cantități masive de toxine care au apărut din 2000. În special, C. difficile PCR-ribotipul 027 (BI / NAP1 / 027) a fost asociat cu o creștere a severității cazurilor, recidivelor și mortalității. Tulpina produce ambele toxine în cantități mari datorită unei mutații (ștergere) a genei regulatoare a tdcC și posedă, la fel ca alte specii de Clostridia , toxina binară CDT. Pe lângă 027, au apărut și alte ribotipuri epidemice considerate hipervirulente, unele cu difuzie internațională, cum ar fi 078 și 018.
S-au dezvoltat o varietate de abordări de tipare moleculară pentru a studia C. difficile și CDI-urile, incluzând: tiparea secvenței multilocus (MLST), analiza multilocus număr variabil tandem-repetare ( MLVA), tiparea stratului de suprafață a secvenței genei A polimorfismul lungimii fragmentului , electroforeză cu câmp pulsat (PFGE), analiză de endonuclează de restricție (REA), toxinotipare (pe baza datelor secvenței de toxină A și B) și ribotipare PCR. [31] Când în 2005, analiza moleculară a condus la identificarea unui tip de tulpină de C. difficile caracterizată ca grupa BI prin analiza de endonuclează de restricție, câmpul pulsat nord-american tip NAP1 prin electroforeză cu gel de câmp pulsat și ribotipul 027 prin multiplarea ribotipurilor PCR au fost denumite C. difficile BI / NAP1 / 027. Diferita terminologie reflectă tehnicile predominante utilizate pentru tipizarea epidemiologică, deși ribotiparea PCR este cea mai larg acceptată în Europa, unde Laboratorul de Referință Anaerobe din Cardiff (Marea Britanie) păstrează colectarea tulpinilor și atribuie numerotarea ribotipurilor PCR. În America de Nord, PFGE este metoda preferată de tastare. [32]
În America de Nord, începând din 2016, tulpina NAP1 a fost înlocuită cu tulpini noi în unele zone din Columbia Britanică. Aceste noi tulpini includ NAP2, NAP4, NAP9 și NAP11 și unele tulpini care nu au o denumire NAP. Frecvența acestor noi tulpini a crescut din 2008 până în 2013 într-o regiune studiată, înlocuind bacteriile NAP1 inițial mai comune și mai recunoscute.
În general, majoritatea metodelor de identificare sunt congruente chiar dacă nu există o corespondență unu-la-unu între diferitele tipificări și doar tehnicile MLVA și REA permit o discriminare suficientă între diferite focare. [33] [34]
Principalele baze de date în care sunt înregistrate caracterizările genetice ale diferitelor tulpini de C. difficile sunt: Enterobase [35] Baze de date publice pentru tiparea moleculară și diversitatea genomului microbian (PubMLST). [36]
Unele tulpini, de exemplu RT017 RT078 RT027, pot trăi cu concentrații scăzute de zahăr trehaloză ; aceste tulpini au devenit mai frecvente după introducerea trehalozei ca aditiv alimentar la începutul anilor 2000, crescând astfel aportul de alimente suplimentate cu trehaloză. [37] [38]
Din 2005, morbiditatea și mortalitatea C. difficile au crescut constant la nivel mondial datorită apariției tulpinilor hipervirulente (în special ribotipul 027). Mecanismele propuse în prezent care disting tulpinile hipervirulente de tulpinile anterioare (mai puțin virulente) sunt controversate. Au fost propuse următoarele: rata crescută de sporulare, creșterea producției de toxine, capacitatea de a depăși tulpinile edemice în intestinul gazdei, dar modul în care acest agent patogen a devenit principala cauză a infecțiilor nosocomiale rămâne necunoscut și clasificarea „tulpinii hipervirulente” rămâne arbitrar. [39] [40] Multe tulpini de C. difficile au fost detectate la animale și alimente derivate de la animale, ceea ce a condus la ipoteza că multe transmisii de C. difficile la om sunt legate de dieta cărnii sau a peștilor sau a interspeciei. [41] [42] [43] [44] [45] [46]
Genomul
Pan-genomul C. difficile este compus dintr-un genom central (acele gene prezente în toate izolatele) și un genom accesoriu sau adaptiv (gene absente de la una sau mai multe tulpini sau unice pentru o anumită tulpină).
Un procent mare (11%) al genomului este alcătuit din elemente genetice mobile, în principal sub formă de transpozoni conjugativi.
Analiza a identificat patru clustere distincte susținute statistic cuprinzând o cladă hipervirulentă, o toxină A - B + cladă și două clade cu izolate umane și animale. Diferențele genetice dintre clade au relevat mai multe insule genetice legate de virulență și adaptarea la nișă, inclusiv rezistența la antibiotice, motilitatea, aderența și metabolismul enteric. Doar 19,7% din gene au fost împărtășite de toate tulpinile,
Genomul C. difficile este mare și divers din punct de vedere genetic, prezentând niveluri remarcabile de plasticitate și niveluri foarte scăzute de conservare între tulpini.
C. difficile posedă un genom "deschis" cu niveluri extreme de plasticitate, cu acces frecvent și schimb cu medii gazdă multiple și bazine de gene bacteriene. În consecință, pe măsură ce mai multe tulpini de C. dificile sunt secvențiate din linii divergente și din diferite surse animale și de mediu, este probabil ca această estimare să crească.
Prima secvență genomică completă a unei tulpini de C. difficile a fost publicată pentru prima dată în 2005 de Institutul Sanger din Marea Britanie. A fost tulpina 630, o tulpină virulentă și rezistentă la medicamente, izolată în Elveția în 1982. Oamenii de știință de la Institutul Sanger au secvențiat genomi de aproximativ 30 C. izolate dificile folosind tehnologii de secvențiere de generație următoare de la 454 Life Sciences și Illumina.
Cercetatorii de la Universitatea McGill din Montreal esalonate in genomul tulpinii C.difficile extrem de virulent de la Quebec , în 2005 , folosind tehnologia secventiere ultra-înaltă viteză. Testele au implicat 400.000 de reacții paralele de secvențiere a ADN ale genomului bacteriei, care au fost fragmentate pentru secvențierea. Aceste secvențe au fost asamblate computerizat pentru a forma o secvență genomică completă.
În 2012, oamenii de știință ai Universității Oxford au secvențiat genomurile C. difficile din 486 de cazuri care au avut loc pe parcursul a patru ani în Oxfordshire folosind tehnologii de secvențiere de generația următoare.
În 2006, Sebaihia și colegii au descris primul genom închis complet secvențiat și adnotat al C. difficile (tulpina 630; RT012). [24] Acest C. difficile virulent și extrem de transmisibil și multirezistent a fost inițial izolat în 1982 de la un pacient cu PMC din Zurich, Elveția. Secvențierea și adnotarea tulpinii 630 a dezvăluit un cromozom circular mare de 4.290.252 bp (4.3 Mb), 3.776 secvențe putătoare de codificare a proteinelor (CDS) și un conținut de GC de 29,06%. De asemenea, a fost identificată o plasmidă circulară (pCD630) de 7.881 pb conținând 11 CDS. [24] Cinci ani mai târziu, Monot și colegii [47] au re-adnotat genomul tulpinii 630 folosind o abordare combinată transcriptomică și proteomică pentru a actualiza funcțiile putative ale> 500 de gene putative sau necunoscute anterior. De atunci, multe alte genomi între 4,1 și 4,3 Mbp au fost complet secvențiate și adnotate: CD37 (RT009; izolat în SUA în 1980), M68 (RT017; izolat în Irlanda în 2006), CF5 (RT017; izolat în Belgia în 1995), M120 (RT078; izolat în Marea Britanie în 2007), G46 (RT027; izolat în Marea Britanie în 2006), R20291 (RT027; izolat în Marea Britanie în 2006), 196 (RT027; izolat în Franța în 1985) , 2007855 (RT027; izolat în Statele Unite în 2007) și BI1 (RT027; izolat în Statele Unite în 1988). [48] [49] [50] Genomurile de referință precum cele ale tulpinilor 630 și M120 joacă un rol important în conducta de analiză a datelor NGS. Acestea cuprind o secvență neechivocă și contiguă de nucleotide cunoscute care acoperă întregul cromozom și plasmide (dacă există), oferind astfel o referință de înaltă calitate pentru proiectarea cartografierii genomului.
Pe scurt, studiile MLST asupra diferitelor colecții de tulpini de C. difficile sugerează că există cinci linii sau clade care, în general, pot fi clasificate după cele mai importante ribotipuri PCR; 027, 017, 023, 078 și un grup mare cuprinzând restul ribotipurilor PCR reprezentând o linie interesantă extrem de divergentă.
Epigenom
C. difficile are un epigenom extrem de divers, raportate până acum 17 motive de metilare de înaltă calitate, cele mai multe legate de tipul 6mA. S-a demonstrat că metilarea într-unul dintre aceste motive, CAAAA A foarte conservată, afectează sporularea, un pas cheie în transmiterea bolii C. difficile , precum și lungimea celulei, formarea biofilmului și colonizarea gazdei. [51]
Bacteriofagii
O altă componentă importantă a mobilomului C. difficile sunt bacteriofagii (fagii). Fagii au evoluat cu C. difficile pe perioade foarte lungi de timp, iar infecția cu fagi este o parte intrinsecă a istoriei naturale și a biologiei C. difficile . Achiziționarea fagilor și pierderea lor din genomul C. difficile sunt evenimente genetice semnificative care au avut un impact asupra evoluției gazdei. [52]
Cel puțin opt bacteriofagi , în principal temperate, adică lizogeni, au fost izolați din C. difficile , cu dimensiuni ale genomului variind de la aproximativ 30 până la aproximativ 60 kb. Ambele tulpini de origine ecologică C. difficile care cele de origine clinică sunt purtătoare ale unui set diversificat și predominant de profag .
Relevanță clinică
Doar tulpinile producătoare de toxine de Clostridioides difficile au relevanță clinică.
Evoluția rapidă a rezistenței la antibiotice în C. difficile [53] și efectele rezultate asupra prevenirii și tratamentului infecțiilor cu C. difficile sunt un motiv de îngrijorare pentru sănătatea publică. [54]
Factorii de virulență ai C. difficile sunt: enterotoxina , sporii și hialuronidaza . Acest bacil se găsește în mod normal în microbiota umană , astfel încât, dacă se utilizează antibiotice pentru o lungă perioadă de timp, ele pot distruge, de asemenea, acele bacterii care mențin confinatul C. difficile care poate prelua și provoca crampe abdominale și diverse boli (colită pseudomembranoasă). Aceste boli au o evoluție benignă și autolimitată, cu excepția cazului în care există complicații care pot compromite peretele intestinal cu un posibil pasaj în circulația bacilului, cu consecință sepsis și deci moartea individului.
Izolarea se poate face prin co-cultură în medii selective pentru C. difficile . Enterotoxina poate fi testată cu metoda ELISA , în timp ce citotoxina cu detectarea toxicității în culturile celulare.
Notă
- ^ Paul A. Lawson, Diane M. Citron și Kerin L. Tyrrell, Reclasificarea Clostridium difficile ca Clostridioides difficile (Hall și O'Toole 1935) Prévot 1938 , în Anaerobe , vol. 40, 2016-08, pp. 95–99, DOI : 10.1016 / j.anaerobe.2016.06.008 . Adus la 22 ianuarie 2021 .
- ^ Evelyn Balsells, Ting Shi și Callum Leese, Sarcina globală a infecțiilor cu Clostridium difficile: o revizuire sistematică și meta-analiză , în Journal of Global Health , vol. 9, nr. 1, DOI : 10.7189 / jogh.09.010407 . Adus la 23 ianuarie 2021 .
- ^ (EN) CDC Aproape jumătate de milion de americani suferă de infecții cu C. difficile în Centrele pentru Controlul și Prevenirea Bolilor, 31 decembrie 2018. Accesat la 23 ianuarie 2021.
- ^ (EN) Infecții cu Clostridium difficile - Fapte și supraveghere , ale Centrului European de Prevenire și Control al Bolilor. Adus la 23 ianuarie 2021 .
- ^ Hall, Ivan C. și O'Toole. Elizabeth, Flora intestinală la nou-născuți, cu o descriere a unui nou anaerob patogen, Bacillus difficile , în American Journal of Diseases of Children , vol. 49, nr. 2, 1935, pp. 390-402.
- ^ X. Chen, K. Katchar; JD. Aurar; N. Nanthakumar; A. Cheknis; DN. Gerding; CP. Kelly, Un model de șoarece al bolii asociate cu Clostridium difficile. , în Gastroenterologie , vol. 135, nr. 6, decembrie 2008, pp. 1984-92, DOI : 10.1053 / j.gastro.2008.09.002 , PMID 18848941 .
- ^ CP. Kelly, JT. LaMont, Clostridium difficile - mai dificil ca niciodată. , în N Engl J Med , vol. 359, nr. 18, octombrie 2008, pp. 1932-40, DOI : 10.1056 / NEJMra0707500 , PMID 18971494 .
- ^ MEA. Hu, K. Katchar; L. Kyne; S. Maroo; S. Tummala; V. Dreisbach; H. Xu; DIN. Leffler; CP. Kelly, Derivarea prospectivă și validarea unei reguli de predicție clinică pentru infecția recurentă cu Clostridium difficile. , în Gastroenterologie , vol. 136, nr. 4, aprilie 2009, pp. 1206-14, DOI : 10.1053 / j.gastro.2008.12.038 , PMID 19162027 .
- ^ JT. Lamont, Theodore E. Woodward Award. Cum funcționează enterotoxinele bacteriene: informații din studiile in vivo. , în Trans Am Clin Climatol Assoc , vol. 113, 2002, pp. 167-80; discuție 180-1, PMID 12053708 .
- ^ a b c Stephen H. Gillespie și Peter M. Hawkey, Principiile și practica bacteriologiei clinice , John Wiley și Sons, 1 iulie 2006, pp. 557–, ISBN 978-0-470-03532-0 .
- ^ I. Brook, Izolarea toxinei care produce Clostridium difficile de la doi copii cu diaree asociată cu oxacilină și dicloxacilină. , în Pediatrie , vol. 65, nr. 6, iunie 1980, pp. 1154-6, PMID 7375240 .
- ^ T. Chopra, GJ. Alangaden; P. Chandrasekar, infecția cu Clostridium difficile la pacienții cu cancer și pacienții cu transplant de celule stem hematopoietice. , în Expert Rev Anti Infect Ther , voi. 8, nr. 10, octombrie 2010, pp. 1113-9, DOI : 10.1586 / eri.10.95 , PMID 20954878 .
- ^ Patrizia Spigaglia și Paola Mastrantonio,Molecular Analysis of the Pathogenicity Locus and Polymorphism in the Putative Negative Regulator of Toxin Production (TcdC) among Clostridium difficile Clinical Isolates , în Journal of Clinical Microbiology , vol. 40, nr. 9, 2002-9, pp. 3470–3475, DOI :10.1128 / JCM.40.9.3470-3475.2002 . Adus la 22 ianuarie 2021 .
- ^ Aharon Oren și George M. Garrity,Listă de noi nume și de noi combinații anterior eficiente, dar nu valabile, publicate în International Journal of Systematic and Evolutionary Microbiology , vol. 67, nr. 9, 2017, pp. 3140-3143, DOI : 10.1099 / ijsem.0.002278 , PMC 5817221 , PMID 28891789 .
- ^ Paul A. Lawson, Diane M. Citron, Kerin L. Tyrrell și Sydney M. Finegold, Reclasificarea Clostridium difficile ca Clostridioides difficile (Hall și O'Toole 1935) Prévot 1938 , în Anaerobe , vol. 40, august 2016, pp. 95–99, DOI : 10.1016 / j.anaerobe.2016.06.008 , ISSN 1095-8274 , PMID 27370902 .
- ^ (EN) Duolong Zhu, Joseph A. Sorg și Xingmin Sun,Clostridioides difficult Biology: Sporulation, Germination, and TerapiesCorresponding for C. difficile Infection , in Frontiers in Cellular Microbiology and Infection, vol. 8, 2018, pp. 29, DOI : 10.3389 / fcimb.2018.00029 , ISSN 2235-2988 , PMC 5809512 , PMID 29473021 .
- ^ Paul A. Lawson, Diane M. Citron, Kerin L. Tyrrell și Sydney M. Finegold, Reclasificarea Clostridium difficile ca Clostridioides difficile (Hall și O'Toole 1935) Prévot 1938 , în Anaerobe , vol. 40, august 2016, pp. 95–99, DOI : 10.1016 / j.anaerobe.2016.06.008 , ISSN 1075-9964 , PMID 27370902 .
- ^ Dale N. Gerding, Carlene A. Muto și Robert C. Owens, Măsuri de control și prevenire a infecției cu Clostridium difficile , în Clinical Infectious Diseases: An Publication Official of the Infectious Diseases Society of America , 46 Suppl 1, 15 ianuarie 2008, pp. S43–49, DOI : 10.1086 / 521861 . Adus la 22 ianuarie 2021 .
- ^ William A. Rutala, Maria F. Gergen și David J. Weber, Eficacitatea diferitelor metode de curățare și dezinfecție împotriva sporilor de Clostridium difficile: importanța îndepărtării fizice versus inactivarea sporicidă , în Controlul infecțiilor și Epidemiologia spitalului , vol. 33, nr. 12, 2012-12, pp. 1255–1258, DOI : 10.1086 / 668434 . Adus la 22 ianuarie 2021 .
- ^ Spigaglia, P., Barbanti, F., Mastrantonio, P., European Study Group on Clostridium difficile (ESGCD), Ackermann, G., Balmelli, C., ... & Drudy, D. (2011). Rezistența multidrog în izolatele clinice europene Clostridium difficile . Jurnalul de chimioterapie antimicrobiană, 66 (10), 2227-2234.
- ^ Kuijper, EJ, van den Berg, RJ, Debast, S., Visser, CE, Veenendaal, D., Troelstra, A., ... & Notermans, DW (2006). Clostridium difficile ribotipul 027, toxinotipul III, Olanda . Boli infecțioase emergente, 12 (5), 827.
- ^ John G. Bartlett, Narrative Review: The New Epidemic of Clostridium difficile - Associated Disease Disease , în Annals of Internal Medicine , vol. 145, nr. 10, 21 noiembrie 2006, pp. 758–764, DOI : 10.7326 / 0003-4819-145-10-200611210-00008 . Adus pe 21 ianuarie 2021 .
- ^ Daniel R. Knight, Briony Elliott și Barbara J. Chang, Diversity and Evolution in the Genome of Clostridium difficile , în Clinical Microbiology Reviews , vol. 28, n. 3, 2015-7, pp. 721–741, DOI : 10.1128 / CMR.00127-14 . Adus pe 21 ianuarie 2021 .
- ^ a b c Mohammed Sebaihia, Brendan W. Wren și Peter Mullany, agentul patogen uman multirezistent Clostridium difficile are un genom mozaic extrem de mobil , în Nature Genetics , vol. 38, nr. 7, 2006-07, pp. 779–786, DOI : 10.1038 / ng1830 . Adus pe 21 ianuarie 2021 .
- ^ Donald C. Vinh,Tulpini și toxine ale Clostridium , în CMAJ: Canadian Medical Association Journal , vol. 172, nr. 3, 1 februarie 2005, pp. 312-313, DOI : 10.1503 / cmaj.1041642 . Adus pe 21 ianuarie 2021 .
- ^ L. Clifford McDonald, George E. Killgore și Angela Thompson, An Epidemic, Toxin Gene - Variant Strain of Clostridium difficile , în New England Journal of Medicine , vol. 353, nr. 23, 8 decembrie 2005, pp. 2433–2441, DOI : 10.1056 / NEJMoa051590 . Adus pe 21 ianuarie 2021 .
- ^ (EN) Rawish Fatima și Muhammad Aziz, The Strain of hypervirulent Clostridium difficile: NAP1 / B1 / 027 - A Brief Overview , în Cureus, vol. 11, n. 1, 29 ianuarie 2019, DOI : 10.7759 / cureus.3977 . Adus pe 21 ianuarie 2021 .
- ^ Gayatri Vedantam, Andrew Clark și Michele Chu, infecția cu Clostridium difficile , în Gut Microbes , vol. 3, nr. 2, 1 martie 2012, pp. 121–134, DOI : 10.4161 / gmic.19399 . Adus pe 21 ianuarie 2021 .
- ^ (EN) Kate E. Dingle, David Griffiths și Xavier Didelot, Clinical Clostridium difficile: clonality and patogenicity locus Diversity in PLOS ONE, vol. 6, nr. 5, 19 mai 2011, pp. e19993, DOI : 10.1371 / journal.pone.0019993 . Adus la 23 ianuarie 2021 .
- ^ (EN) C. Eckert, A. Emirian și A. Le Monnier, Prevalența și patogenitatea tulpinilor binare toxice Clostridium difficile pozitive care nu produc toxine A și B , în New New Microbes and Infections, vol. 3, 2015-01, pp. 12-17, DOI : 10.1016 / j.nmni.2014.10.003 . Adus la 23 ianuarie 2021 .
- ^ Centrul European pentru Prevenirea și Controlul Bolilor. Proceduri de laborator pentru diagnosticarea și tiparea infecției umane cu Clostridium difficile. , Oficiul Publicațiilor, 2018, DOI : 10.2900 / 04291 . Adus la 23 ianuarie 2021 .
- ^ Specia în continuă evoluție a Clostridium difficile , pe Medscape . Adus la 23 ianuarie 2021 .
- ^ George Killgore, Angela Thompson și Stuart Johnson, Comparația a șapte tehnici de tipare a tulpinilor internaționale de epidemie de Clostridium difficile: analiza endonucleazei de restricție, electroforeza în gel cu câmp pulsat, ribotarea PCR, tiparea secvenței multiloc, analiza repetitivă a numărului variabil multiloc, polimorfism de lungime a fragmentului amplificat și proteinarea stratului de suprafață A de tipare a secvenței genelor , în Journal of Clinical Microbiology , vol. 46, nr. 2, 2008-02, pp. 431-437, DOI : 10.1128 / JCM.01484-07 . Adus la 24 ianuarie 2021 .
- ^ Fred C. Tenover, Thomas Åkerlund e Dale N. Gerding, Comparison of Strain Typing Results for Clostridium difficile Isolates from North America▿ , in Journal of Clinical Microbiology , vol. 49, n. 5, 2011-5, pp. 1831–1837, DOI : 10.1128/JCM.02446-10 . URL consultato il 24 gennaio 2021 .
- ^ EnteroBase , su enterobase.warwick.ac.uk . URL consultato il 24 gennaio 2021 .
- ^ ( EN ) Clostridioides difficile , su PubMLST . URL consultato il 24 gennaio 2021 .
- ^ J. Collins, C. Robinson e H. Danhof, Dietary trehalose enhances virulence of epidemic Clostridium difficile , in Nature , vol. 553, n. 7688, 18 gennaio 2018, pp. 291–294, DOI : 10.1038/nature25178 . URL consultato il 24 gennaio 2021 .
- ^ ( EN ) David W. Eyre, Xavier Didelot e Anthony M. Buckley, Clostridium difficile trehalose metabolism variants are common and not associated with adverse patient outcomes when variably present in the same lineage , in EBioMedicine , vol. 43, 1º maggio 2019, pp. 347–355, DOI : 10.1016/j.ebiom.2019.04.038 . URL consultato il 24 gennaio 2021 .
- ^ ( EN ) Michelle Merrigan, Anilrudh Venugopal e Michael Mallozzi, Human Hypervirulent Clostridium difficile Strains Exhibit Increased Sporulation as Well as Robust Toxin Production , in Journal of Bacteriology , vol. 192, n. 19, 1º ottobre 2010, pp. 4904–4911, DOI : 10.1128/JB.00445-10 . URL consultato il 24 gennaio 2021 .
- ^ Laith Yakob, Thomas V. Riley e David L. Paterson, Mechanisms of hypervirulent Clostridium difficile ribotype 027 displacement of endemic strains: an epidemiological model , in Scientific Reports , vol. 5, 28 luglio 2015, DOI : 10.1038/srep12666 . URL consultato il 24 gennaio 2021 .
- ^ ( EN ) Alexander Rodriguez-Palacios, Kevin Q Mo e Bhavan U. Shah, Global and Historical Distribution of Clostridioides difficile in the Human Diet (1981-2019): Systematic Review and Meta-Analysis of 21886 Samples Reveal Sources of Heterogeneity, High-Risk Foods, and Unexpected Higher Prevalence Towards the Tropic , Infectious Diseases (except HIV/AIDS), 22 novembre 2019, DOI : 10.1101/19012450 . URL consultato il 24 gennaio 2021 .
- ^ Dallas G. Hoover e Alexander Rodriguez-Palacios, Transmission of Clostridium difficile in foods , in Infectious Disease Clinics of North America , vol. 27, n. 3, 2013-09, pp. 675–685, DOI : 10.1016/j.idc.2013.05.004 . URL consultato il 23 gennaio 2021 .
- ^ ( EN ) K. Keel, JS Brazier e KW Post, Prevalence of PCR Ribotypes among Clostridium difficile Isolates from Pigs, Calves, and Other Species , in Journal of Clinical Microbiology , vol. 45, n. 6, 1º giugno 2007, pp. 1963–1964, DOI : 10.1128/JCM.00224-07 . URL consultato il 24 gennaio 2021 .
- ^ Alexander WW Brown e Robert B. Wilson, Clostridium difficile colitis and zoonotic origins-a narrative review , in Gastroenterology Report , vol. 6, n. 3, 2018-08, pp. 157–166, DOI : 10.1093/gastro/goy016 . URL consultato il 23 gennaio 2021 .
- ^ Alan M. Mc Govern, Niki F. Foster e Lynette A. Pereira, Human Clostridium difficile infection caused by a livestock-associated PCR ribotype 237 strain in Western Australia , in JMM case reports , vol. 3, n. 4, 2016-08, pp. e005062, DOI : 10.1099/jmmcr.0.005062 . URL consultato il 23 gennaio 2021 .
- ^ ( EN ) Luis G Arroyo, Stephen A Kruth e Barbara M Willey, PCR ribotyping of Clostridium difficile isolates originating from human and animal sources , in Journal of Medical Microbiology , vol. 54, n. 2, 1º febbraio 2005, DOI : 10.1099/jmm.0.45805-0#tab2 . URL consultato il 23 gennaio 2021 .
- ^ Marc Monot, Caroline Boursaux-Eude e Marie Thibonnier, Reannotation of the genome sequence of Clostridium difficile strain 630 , in Journal of Medical Microbiology , vol. 60, Pt 8, 2011-08, pp. 1193–1199, DOI : 10.1099/jmm.0.030452-0 . URL consultato il 24 gennaio 2021 .
- ^ Tom Gaulton, Raju Misra e Graham Rose, Complete Genome Sequence of the Hypervirulent Bacterium Clostridium difficile Strain G46, Ribotype 027 , in Genome Announcements , vol. 3, n. 2, 26 marzo 2015, DOI : 10.1128/genomeA.00073-15 . URL consultato il 24 gennaio 2021 .
- ^ Michael SM Brouwer, Elaine Allan e Peter Mullany, Draft genome sequence of the nontoxigenic Clostridium difficile strain CD37 , in Journal of Bacteriology , vol. 194, n. 8, 2012-04, pp. 2125–2126, DOI : 10.1128/JB.00122-12 . URL consultato il 24 gennaio 2021 .
- ^ Miao He, Mohammed Sebaihia e Trevor D. Lawley, Evolutionary dynamics of Clostridium difficile over short and long time scales , in Proceedings of the National Academy of Sciences of the United States of America , vol. 107, n. 16, 20 aprile 2010, pp. 7527–7532, DOI : 10.1073/pnas.0914322107 . URL consultato il 24 gennaio 2021 .
- ^ Pedro H. Oliveira, John W. Ribis e Elizabeth M. Garrett, Epigenomic characterization of Clostridioides difficile finds a conserved DNA methyltransferase that mediates sporulation and pathogenesis , in Nature microbiology , vol. 5, n. 1, 2020-1, pp. 166–180, DOI : 10.1038/s41564-019-0613-4 . URL consultato il 22 gennaio 2021 .
- ^ Katherine R. Hargreaves e Martha RJ Clokie, Clostridium difficile phages: still difficult? , in Frontiers in Microbiology , vol. 5, 28 aprile 2014, DOI : 10.3389/fmicb.2014.00184 . URL consultato il 22 gennaio 2021 .
- ^ Saeed S. Banawas, Clostridium difficile Infections: A Global Overview of Drug Sensitivity and Resistance Mechanisms , in BioMed Research International , vol. 2018, 21 febbraio 2018, DOI : 10.1155/2018/8414257 . URL consultato il 24 gennaio 2021 .
- ^ Patrizia Spigaglia, Paola Mastrantonio e Fabrizio Barbanti, Antibiotic Resistances of Clostridium difficile , in Advances in Experimental Medicine and Biology , vol. 1050, 2018, pp. 137–159, DOI : 10.1007/978-3-319-72799-8_9 . URL consultato il 24 gennaio 2021 .
Bibliografia
- Giampiero Carosi, Carosi - Pauluzzi e Sergio Pauluzzi, Malattie infettive , PICCIN, 2007, pp. 233–, ISBN 978-88-299-1844-7 .
- ( EN ) Tracy Dale Wilkins, Clostridium difficile , Springer, 2000, ISBN 978-3-540-67291-3 .
- ( EN ) Patrice Boquet e Emmanuel Lemichez, Bacterial virulence factors and Rho GTPases , Springer, 2005, pp. 117–, ISBN 978-3-540-23865-2 .
- ( EN ) Ferruccio Mandler, Catalogo ragionato dei presidi diagnostici per la microbiologia clinica , PICCIN, 1999, pp. 62–, ISBN 978-88-299-1442-5 .
- ( EN ) Stephen H. Gillespie e Peter M. Hawkey, Principles and Practice of Clinical Bacteriology , John Wiley and Sons, 1º luglio 2006, pp. 557–, ISBN 978-0-470-03532-0 .
- ( EN ) James G. Fox, The Mouse in Biomedical Research: Diseases , Academic Press, 2007, pp. 357–, ISBN 978-0-12-369456-0 .
- ( EN ) ICDDR, B, Diarrhoeal Diseases Research , ICDDR, B, settembre 1992, pp. 156–.
- ( EN ) Allison Tannis, Probiotic Rescue: How You Can Use Probiotics to Fight Cholesterol, Cancer Superbugs, Digestive Complaints and More , John Wiley and Sons, 3 aprile 2008, pp. 182–, ISBN 978-0-470-15475-5 .
Riviste
- CH. Choi, SA. Jung; BI. Lee; KM. Lee; JS. Kim; DS. Han, [Diagnostic guideline of ulcerative colitis]. , in Korean J Gastroenterol , vol. 53, n. 3, marzo 2009, pp. 145-60, PMID 19835217 .
- E. van Nood, P. Speelman; EJ. Kuijper; JJ. Keller, Struggling with recurrent Clostridium difficile infections: is donor faeces the solution? , in Euro Surveill , vol. 14, n. 34, 2009, PMID 19712646 .
- E. Palencia-Herrejón, B. Sánchez; I. Escobar; ML. Gómez-Lus, [Proton pump inhibitors and infection risk]. , in Rev Esp Quimioter , vol. 24, n. 1, marzo 2011, pp. 4-12, PMID 21412664 .
- AC. de Oliveira, QS. Damasceno, [Surfaces of the hospital environment as possible deposits of resistant bacteria: a review]. , in Rev Esc Enferm USP , vol. 44, n. 4, dicembre 2010, pp. 1118-23, PMID 21337799 .
- J. Freeman, MP. Bauer; SD. Baines; J. Corver; WN. Fawley; B. Goorhuis; EJ. Kuijper; MH. Wilcox, The changing epidemiology of Clostridium difficile infections. , in Clin Microbiol Rev , vol. 23, n. 3, luglio 2010, pp. 529-49, DOI : 10.1128/CMR.00082-09 , PMID 20610822 .
- D. Shah, MD. Dang; R. Hasbun; HL. Koo; ZD. Jiang; HL. DuPont; KW. Garey, Clostridium difficile infection: update on emerging antibiotic treatment options and antibiotic resistance. , in Expert Rev Anti Infect Ther , vol. 8, n. 5, maggio 2010, pp. 555-64, DOI : 10.1586/eri.10.28 , PMID 20455684 .
- C. Vaishnavi, Clinical spectrum pathogenesis of Clostridium difficile associated diseases. , in Indian J Med Res , vol. 131, aprile 2010, pp. 487-99, PMID 20424299 .
- H. Taslim, Clostridium difficile infection in the elderly. , in Acta Med Indones , vol. 41, n. 3, luglio 2009, pp. 148-51, PMID 19752488 .
- M. Bixquert Jiménez, Treatment of irritable bowel syndrome with probiotics. An etiopathogenic approach at last? , in Rev Esp Enferm Dig , vol. 101, n. 8, agosto 2009, pp. 553-64, PMID 19785495 .
- C. Eckert, F. Barbut, [Clostridium-difficile-associated infections]. , in Med Sci (Paris) , vol. 26, n. 2, febbraio 2010, pp. 153-8, DOI : 10.1051/medsci/2010262153 , PMID 20188046 .
Veterinaria
- Wilfried R. Kraft e Ulrich M. Dürr, Trattato di medicina e chirurgia del gatto , Elsevier srl, 2001, pp. 199–, ISBN 978-88-214-2525-7 .
- ( EN ) Norman Edward Robinson e Kim A. Sprayberry, Current therapy in equine medicine , Elsevier Health Sciences, 2009, pp. 158–, ISBN 978-1-4160-5475-7 .
Voci correlate
- Infezione da Clostridioides difficile
- Terreno selettivo per Clostridioides difficile
- Infezioni correlate all'assistenza
Altri progetti
-
 Wikimedia Commons contiene immagini o altri file su Clostridium difficile
Wikimedia Commons contiene immagini o altri file su Clostridium difficile -
 Wikispecies contiene informazioni su Clostridium difficile
Wikispecies contiene informazioni su Clostridium difficile
Collegamenti esterni
| Controllo di autorità | BNE ( ES ) XX535557 (data) |
|---|