Hidrură de aluminiu
| Hidrură de aluminiu | |
|---|---|
| Numele IUPAC | |
| Trihidrură de aluminiu | |
| Denumiri alternative | |
| Hidrură de aluminiu, alan | |
| Caracteristici generale | |
| Formula moleculară sau brută | AlH 3 |
| Masa moleculară ( u ) | 29,99 |
| Aspect | Solid cristalin alb, nevolatil, foarte polimerizat. |
| numar CAS | |
| Numărul EINECS | 232-053-2 |
| PubChem | 14488 |
| ZÂMBETE | [AlH3] |
| Proprietăți fizico-chimice | |
| Densitate (g / cm 3 , în cs ) | 1.486 |
| Solubilitate în apă | Reactiv |
| Temperatură de topire | 150 ° C |
| Informații de siguranță | |
| Simboluri de pericol chimic | |
| | |
Hidrură de aluminiu este un compus chimic având formula AIH3. Este un solid instabil peste 150 ° C. Are proprietăți reducătoare și reacționează violent cu apa și alte substanțe protice care eliberează hidrogen . Nu are utilizări practice semnificative și nu este disponibil comercial.
fundal
AlH 3 a fost sintetizat pentru prima dată în 1942 de Egon Wiberg (1901-1976). [1]
Structura
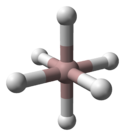
Hidrura de aluminiu este un solid polimeric. Multe polimorfi sunt posibile, numite α-, β-, γ-, δ-, ε- și θ-AIH3. Forma α-AlH 3 este cea mai stabilă și structura sa a fost determinată de difracția cu raze X și difracția neutronică . Fiecare atom de aluminiu este înconjurat de șase atomi de hidrogen care pun în legătură cu alți șase atomi de aluminiu. Distanțele Al - H sunt echivalente (172 pm ), iar unghiul Al - H - Al este de 141 °. [2]
celula primitivă a α-AlH 3 | Coordonarea Al | Coordonarea lui H |
Sinteză
Cea mai convenabilă sinteză se realizează prin reacția în soluție eterică de litiu tetrahidroaluminat LiAlH 4 și triclorură de aluminiu AlCl 3 în condiții strict controlate. În funcție de condițiile utilizate, este posibil să se determine ce polimorf să se obțină: [3]
- 3LiAlH 4 + AlCl 3 + n Et 3 O → 4 [AlH 3 (Et 3 O) n ] + 3LiCl
Reactivitate
Hidrura de aluminiu este instabilă la peste 150 ° C; are proprietăți reducătoare și reacționează violent cu apa și alte substanțe protice care eliberează H 2 . [4]
Aplicații
Hidrura de aluminiu nu are utilizări practice semnificative și nu este disponibilă comercial. A fost investigat ca un posibil aditiv pentru combustibilii solizi pentru rachete. [5] Mai mult, fiind o substanță care conține hidrogen în propriul rețea cristalină, a fost studiată ca un material de potențial interes în dezvoltarea vehiculelor alimentate cu hidrogen . [6] Niciuna dintre aceste aplicații nu a avut succes până în prezent (2013).
Notă
Bibliografie
- FM Brower, NE Matzek, PF Reigler, HW Rinn, CB Roberts, DL Schmidt, JA Snover, K. Terada, Prepararea și proprietățile hidrurii de aluminiu , în J. Am. Chem. Soc. , Vol. 98, nr. 9, 1976, pp. 2450–2453, DOI : 10.1021 / ja00425a011 . Adus pe 29 noiembrie 2013 .
- J. Graetz, J. Reilly, G. Sandrock, J. Johnson, WM Zhou, J. Wegrzyn, Hidrură de aluminiu, AlH 3 , ca compus de stocare a hidrogenului , în Raportul tehnic BNL - 77336-2006 , 2006, DOI : 10.2172 / 899889 . Adus pe 29 noiembrie 2013 .
- ( EN ) NN Greenwood și A. Earnshaw, Chimia elementelor , ediția a II-a, Oxford, Butterworth-Heinemann, 1997, ISBN 0-7506-3365-4 .
- O. Stecher și E. Wiberg, Über einen nichtflüchtigen, polymeren Aluminiumwasserstoff (AlH 3 ) x und einige flüchtige Verbindungen des monomeren AlH 3 , în Ber. deutsch. chim. Iisus , vol. 75, nr. 12, 1942, pp. 2003-2012, DOI : 10.1002 / cber.19420751280 . Adus pe 29 noiembrie 2013 .
- (EN) EA Sullivan, hidruri, în Kirk-Othmer Encyclopedia of Chemical Technology, ediția a IV-a, John Wiley & Sons, 1998.
- JW Turley și HW Rinn, structură cristalină din hidrură de aluminiu , în Inorg. Chem. , vol. 8, nr. 1, 1969, pp. 18-22, DOI : 10.1021 / ic50071a005 . Adus pe 29 noiembrie 2013 .
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere pe hidrură de aluminiu
Wikimedia Commons conține imagini sau alte fișiere pe hidrură de aluminiu
linkuri externe
- Hidrură de aluminiu , pe webelements.com .
- Depozitarea hidrogenului , pe bnl.gov . Adus la 22 mai 2008 (arhivat din original la 23 august 2006) .
| Controlul autorității | GND ( DE ) 4142120-6 |
|---|