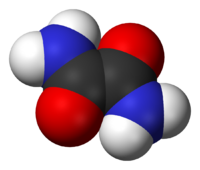
Oxamida
| Oxamida | |
|---|---|
| Denumiri alternative | |
| etanodiamida | |
| Caracteristici generale | |
| Formula moleculară sau brută | C 2 H 4 N 2 O 2 |
| Masa moleculară ( u ) | 88.0654 |
| Aspect | pudră albă |
| numar CAS | |
| Numărul EINECS | 207-442-5 |
| PubChem | 10113 |
| ZÂMBETE | C(=O)(C(=O)N)N |
| Proprietăți fizico-chimice | |
| Densitate (g / cm 3 , în cs ) | 1.667 [1] |
| Solubilitate în apă | 0,3 g / L la 20 ° C [2] |
| Temperatură de topire | ≈350 ° C (623 K) dec. [2] |
| Proprietăți termochimice | |
| Δ f H 0 (kJ mol −1 ) | -504,4 [1] |
| Informații de siguranță | |
| Simboluri de pericol chimic | |
 | |
| Atenţie | |
| Fraze H | 302 - 315 - 319 [3] |
| Sfaturi P | 305 + 351 + 338 [3] |
Oxamida este compusul organic cu formula (CONH 2 ) 2 . În condiții normale, este un solid cristalin alb. Este solubil în etanol , ușor solubil în apă și insolubil în eter etilic . Oxamidă este di amida a acidului oxalic .
fundal
Oxamida a fost sintetizată pentru prima dată în 1830 de Jean Baptiste Dumas . [4] În 1859 Justus von Liebig l-a preparat din cianogen și apă, folosind acetaldehidă ca catalizator. [5] În 1913, biochimistul german Walter Löb a obținut-o prin tratarea vaporilor de formamidă cu descărcare electrică. [6]
Sinteză
Oxamida este sintetizată industrial prin oxidarea catalitică a cianurii de hidrogen . Reacția este practic cantitativă și fără tratamente speciale se obține 99% oxamidă pură. [2]
Utilizări
Oxamida este utilizată în principal ca îngrășământ cu azot cu eliberare lentă, cu avantajul că, datorită solubilității sale slabe, nu este spălat din sol de ploaie, așa cum se întâmplă cu alte îngrășăminte cu azot, cum ar fi ureea și sulfatul de amoniu . [7] Este, de asemenea, utilizat ca materie primă pentru sinteza altor compuși organici. [2]
Informații privind toxicitatea / siguranța
Oxamida poate provoca iritarea ochilor și a pielii și este dăunătoare dacă este ingerată. Nu există date care să indice proprietăți cancerigene. [3]
Notă
Bibliografie
- ( DE ) J. Dumas, Ueber das Oxamid, eine gewissen Thierstoffen verwandte Substanz , în Ann. Fizic. , vol. 95, nr. 8, 1830, pp. 474–487, DOI : 10.1002 / andp.18300950803 .
- DR Lide (Editor), CRC Handbook of Chemistry and Physics, Internet Version 2005 , at hbcponline.com , CRC Press, Boca Raton, 2005. Accesat la 9 decembrie 2017 .
- ( DE ) W. Löb, Über das Verhalten des Formamids unter der Wirkung der stillen Entladung Ein Beitrag zur Frage der Stickstoff-Assimilation , în Ber. Dtsch. Chem. Iisus , vol. 46, nr. 1, 1913, pp. 684-697, DOI : 10.1002 / cber.19130460193 .
- ( EN ) W. Riemenschneider, Oxalic acid , în Ullmann's Encyclopedia of Industrial Chemistry , Wiley-VCH, 2002, DOI : 10.1002 / 14356007.a18_247 .
- ( EN ) H. Sawada și T. Murakami, acid oxalic , în Kirk-Othmer Encyclopedia of Chemical Technology , ediția a IV-a, John Wiley & Sons, 1998.
- Sigma-Aldrich, Fișa cu date de siguranță Oxamide , de pe sigmaaldrich.com , 2013. Accesat la 8 decembrie 2017 .
- J. von Liebig, Ueber die Bildung des Oxamids aus Cyan , în Justus Liebigs Ann. Chem. , vol. 113, nr. 2, 1860, pp. 246–247, DOI : 10.1002 / jlac.18601130213 . Adus pe 3 aprilie 2014 .
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere pe Oxamide
Wikimedia Commons conține imagini sau alte fișiere pe Oxamide
| Controlul autorității | GND ( DE ) 4413479-4 |
|---|