Peroxidisulfat
Salt la navigare Salt la căutare
| Ion peroxidisulfat | |||
|---|---|---|---|
| Numele IUPAC | |||
| mu-peroxid-bis (trioxidosulfat) (2-) [1] | |||
| Caracteristici generale | |||
| Formula moleculară sau brută | S 2 O 2− 8 | ||
| Masa moleculară ( u ) | 192.112 gm mol -1 | ||
| numar CAS | |||
| ZÂMBETE | [O-]S(=O)(=O)OOS(=O)(=O)[O-] | ||
| Informații de siguranță | |||
| Simboluri de pericol chimic | |||
  | |||
| Atenţie | |||
| Fraze H | --- | ||
| Sfaturi P | --- | ||
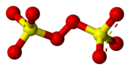
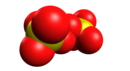
Ionul peroxidisulfat , numit și persulfat , este un anion aparținând clasei peroxisulfatului , cu formula S 2 O 2− 8 . Are doi atomi de sulf cu o stare de oxidare de +6.
Sărurile care conțin acest ion se numesc peroxidisulfați și se formează atunci când acidul său conjugat , acidul peroxidisulfuric , reacționează cu o bază.
Aplicații
Se utilizează ionul peroxidisulfat:
- combinat cu metale alcaline, în extracția ligninei
- combinat cu amoniu , potasiu sau sodiu , ca inițiator de polimerizare a plasticului
- în decolorarea uleiurilor
- dezinfectant de apă
- ca îngrășământ și agent pentru îmbunătățirea calității solului
- ca agent oxidant puternic, în reacții chimice ( Eº = 2,0 V )
Reacțiile de oxidare la care participă persulfatul sunt lente, dar sunt catalizate de Ag + . Se utilizează pentru prepararea permanganatului începând cu Mn 2+ :
- 2Mn 2+ + 5S 2 O 2− 8 + 8H 2 O → 2MnO - 4 + 10SO 2− 4 + 16H +
Un anion de peroxid de sulf similar cu peroxidisulfatul, dar mult mai instabil, este peroximonosulfatul .
Notă
- ^ Nomenclatura chimiei anorganice: Recomandările IUPAC 2005 (Cartea roșie) , Cambridge, The Royal Society of Chemistry , 2005, p. 315, ISBN 978-0-85404-438-2 .
Bibliografie
- Ivano Bertini și Fabrizio Mani, Chimie anorganică , CEDAM, ISBN 88-13-16199-9 .
Elemente conexe
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere pe Peroxidisulfat
Wikimedia Commons conține imagini sau alte fișiere pe Peroxidisulfat