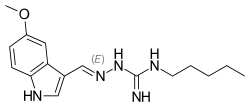Tegaserod
| Tegaserod | |
|---|---|
| Numele IUPAC | |
| (2 E ) -2 - [(5-Metoxi-1 H -indol-3-il) metilen] - N- pentilhidrazincarboximidamidă | |
| Caracteristici generale | |
| Formula moleculară sau brută | C 16 H 23 N 5 O |
| Masa moleculară ( u ) | 301,39 g / mol |
| numar CAS | |
| Numărul EINECS | 630-469-2 |
| Codul ATC | A06 |
| PubChem | 5362436 CID 5362436 |
| DrugBank | DB01079 |
| ZÂMBETE | CCCCCNC(=N)NN=CC1=CNC2=C1C=C(OC)C=C2 |
| Date farmacologice | |
| Mod de administrare | Oral |
| Date farmacocinetice | |
| Biodisponibilitate | 10% |
| Legarea proteinelor | 98% |
| Jumătate de viață | 11 ± 5 ore |
| Excreţie | Fecale (67%) și renale (33%) |
| Informații de siguranță | |
Tegaserod este un agonist al receptorului 5-HT4, utilizat pentru tratamentul sindromului intestinului iritabil și a constipației . Medicamentul este fabricat și vândut de compania farmaceutică Novartis sub denumirea comercială de Zelnorm și Zelmac . Aprobat de Administrația SUA pentru Alimente și Medicamente (FDA) în 2002, ulterior a fost retras de pe piață în 2007 din cauza îngrijorărilor FDA cu privire la posibilele efecte cardiovasculare adverse. Înainte de aceasta, tegaserodul era singurul medicament aprobat de FDA pentru a ajuta la ameliorarea disconfortului abdominal, a balonării și a constipației asociate sindromului intestinului iritabil. [1] [2] Utilizarea acestuia a fost aprobată și pentru tratamentul constipației idiopatice cronice. În prezent, tegaserod poate fi utilizat numai în situații de urgență și numai cu permisiunea FDA.
Farmacodinamica
Tegaserod funcționează prin legarea cu afinitate ridicată la receptorii 5-HT4 localizați pe neuroni în tractul gastro-intestinal. [3] Activarea acestor receptori implică o stimulare a peristaltismului și a capacității secretoare a intestinului, inhibând în același timp senzațiile viscerale. Zelnorm este, de asemenea, un antagonist al receptorului 5-HT2B. [4] Molecula cauzează probabil o creștere a activității motorii bazale a intestinului și normalizează motilitatea afectată în tot tractul gastro-intestinal, reducând astfel și senzația de durere abdominală .
Farmacocinetica
După administrarea orală, tegaserodul este absorbit într-o măsură limitată din tractul gastro-intestinal . Concentrația plasmatică maximă (C max ) este atinsă în decurs de 1 oră (T max ). Biodisponibilitatea este de doar aproximativ 10% (la persoanele cu repaus alimentar) și luarea acestuia cu alimente reduce și mai mult biodisponibilitatea acesteia (cu aproximativ 40-65%), întârziind, de asemenea, T max. În fluidele și țesuturile biologice . Legarea proteinelor plasmatice este de aproximativ 98%. Timpul de înjumătățire este de aproximativ 11 ore, cu o variabilitate individuală între 6 și 16 ore. Nu se știe dacă tegaserodul poate traversa bariera placentară. Studiile experimentale au arătat că molecula poate fi dozată în laptele șobolanilor, dar nu este clar dacă acest lucru se întâmplă și cu laptele uman. După o primă hidroliză a acidului gastric, tegaserodul este oxidat și glucuronidat până la principalul metabolit inactiv, glucuronatul acidului 5-metoxindol-3-carboxilic. Compusul este eliminat în principal prin fecale (aproximativ 67%) ca medicament nemodificat și în urină (restul de 33%) ca metabolit . [5] [6]
Utilizări clinice
Tegaserod este indicat în tratamentul sindromului intestinului iritabil (IBS), în special la femeile unde constipația predomină printre simptome. [7] [8] Este, de asemenea, utilizat în tratamentul constipației idiopatice cronice (adică de cauză necunoscută) la vârstnici, adică peste 65 de ani. [9] [10]
Efecte secundare și nedorite
În timpul tratamentului cu medicamentul sunt raportate evenimentele adverse care au apărut mai frecvent: cefalee , migrenă , vertij , dureri de spate (dureri de spate), dureri la nivelul membrelor inferioare și în special la nivelul picioarelor, dureri articulare, miopatie. De asemenea, au fost raportate tulburări gastro-intestinale, cum ar fi greață , vărsături , dureri abdominale, tensiune și plenitudine abdominală , flatulență , diaree . Pot apărea și alte simptome, cum ar fi oboseala , faringita , congestia sânilor, dismenoreea , mâncărimea și erupțiile cutanate.
Cel mai grav efect advers al terapiei cu tegaserod a fost recunoscut în contextul post-introducere pe piață și reprezintă un risc crescut de infarct miocardic sau accident vascular cerebral .
La 30 martie 2007, Food and Drug Administration a solicitat companiei Novartis să prevadă retragerea de pe piață a tegaserodului. Autoritatea americană a medicamentelor în urma datelor colectate în faza de farmacovigilență după punerea pe piață a susținut că a existat o corelație între prescrierea medicamentului și riscul crescut de atac de cord sau accident vascular cerebral. Analiza datelor colectate la peste 18.000 de pacienți a arătat că evenimente cardiovasculare adverse grave (incluzând angina pectorală, infarct miocardic și accident vascular cerebral) au apărut la 13 din 11.614 pacienți tratați cu tegaserod (o rată de 0,11%) comparativ cu 1 din 7.031 pacienți tratați cu placebo (o rată de 0,01%).
Novartis a răspuns la autoritatea de reglementare susținând că toți pacienții afectați aveau boli cardiovasculare preexistente sau factori de risc pentru această afecțiune și că, de asemenea, nu exista o relație de cauzalitate între utilizarea tegaserodului și evenimentele cardiovasculare. În aceeași zi cu anunțul FDA, Novartis Pharmaceuticals Canada a anunțat că suspendă comercializarea și vânzările medicamentului în Canada ca răspuns la o cerere din partea Health Canada. Unele companii farmaceutice din India, cum ar fi Cipla și Torrent Pharmaceuticals Ltd., par să păstreze în continuare tegaserodul ca medicament generic pe listele lor și că unii vânzători online îl pot vinde, în ciuda faptului că medicamentul a fost interzis în India în 2011.
Contraindicații
Tegaserod este contraindicat în caz de hipersensibilitate cunoscută la substanța activă sau la oricare dintre excipienții conținuți în formularea farmacologică. Medicamentul este, de asemenea, contraindicat la subiecții cu insuficiență renală severă, insuficiență hepatică moderată sau severă și la cei care au un istoric clinic de obstrucție intestinală, boli simptomatice ale vezicii biliare , disfuncție a sfincterului Oddi sau aderențe abdominale.
Notă
- ^ LJ. Scott, CM. Perry, Tegaserod. , în Droguri , vol. 58, nr. 3, septembrie 1999, pp. 491-6; discuția 497-8, PMID 10493276 .
- ^ FIE. Lacy, S. Yu, Tegaserod: un nou agonist 5-HT4. , în J Clin Gastroenterol , vol. 34, nr. 1, ianuarie 2002, pp. 27-33, PMID 11743242 .
- ^ NJ. Talley, modulatori neuroenterici serotoninergici. , In Lancet, vol. 358, nr. 9298, decembrie 2001, pp. 2061-8, DOI : 10.1016 / S0140-6736 (01) 07103-3 , PMID 11755632 .
- ^ DT. Beattie, JA. Smith; D. marchiz; RG. Vickery; SR. Armstrong; T. Pulido-Rios; JL. McCullough; C. Sandlund; C. Richardson; N. Niciodată; PP. Humphrey, agonistul receptorului 5-HT4, tegaserod, este un antagonist puternic al receptorului 5-HT2B in vitro și in vivo. , în Br J Pharmacol , voi. 143, nr. 5, noiembrie 2004, pp. 549-60, DOI : 10.1038 / sj.bjp.0705929 , PMID 15466450 .
- ^ M. Camilleri, Articolul de recenzie: tegaserod. , în Aliment Pharmacol Ther , vol. 15, nr. 3, mar 2001, pp. 277-89, PMID 11207504 .
- ^ S. Appel-Dingemanse, Farmacocinetica clinică a tegaserodului, un agonist parțial al receptorului serotoninei 5-HT (4) cu activitate promotilă. In Clin Pharmacokinet, vol. 41, nr. 13, 2002, pp. 1021-42, PMID 12403641 .
- ^ M. Camilleri, Managementul sindromului intestinului iritabil. , în Gastroenterologie , vol. 120, n. 3, februarie 2001, pp. 652-68, PMID 11179242 .
- ^ M. Camilleri, Medicamente noi pentru sindromul intestinului iritabil: motilitate și senzație. , în J Pediatr Gastroenterol Nutr , 32 Suppl 1, 2001, pp. S35-7, PMID 11321419 .
- ^ RF. Baun, HB. Levy, Tegaserod pentru tratarea constipației cronice la pacienții vârstnici. In Ann Pharmacother, voi. 41, nr. 2, februarie 2007, pp. 309-13, DOI : 10.1345 / aph.1H220 , PMID 17227825 .
- ^ G. Spinzi, A. Amato; G. Imperiali; N. Lenoci; G. Mandelli; S. Paggi; F. Radaelli; N. Teren; V. Terruzzi, Constipație la vârstnici: strategii de management. , în Îmbătrânirea drogurilor , vol. 26, n. 6, 2009, pp. 469-74, DOI : 10.2165 / 00002512-200926060-00003 , PMID 19591521 .
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere pe tegaserod
Wikimedia Commons conține imagini sau alte fișiere pe tegaserod