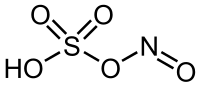
Acid nitrosilsulfuric
Salt la navigare Salt la căutare
| Acid nitrosilsulfuric | |
|---|---|
| Denumiri alternative | |
| nitrosil hidrogen sulfat | |
| Caracteristici generale | |
| Formula moleculară sau brută | NOHSO 4 sau HNO 4 S |
| Masa moleculară ( u ) | 127.08 |
| Aspect | cristale galbene |
| numar CAS | |
| Numărul EINECS | 231-964-2 |
| PubChem | 82157 |
| ZÂMBETE | N(=O)OS(=O)(=O)O |
| Proprietăți fizico-chimice | |
| Temperatură de topire | 70 ° C (343 K) |
| Temperatura de fierbere | se descompune |
| Informații de siguranță | |
| Simboluri de pericol chimic | |
  | |
| Pericol | |
| Fraze H | 272 - 301 - 311 - 314 - 330 |
| Sfaturi P | 220 - 260 - 280 - 284 - 301 + 310 - 305 + 351 + 338 [1] |
Acidul nitrosilsulfuric este un derivat al acidului sulfuric în care un atom de hidrogen este înlocuit cu nitrosil .
Poate fi preparat prin reacția acidului azotat cu acidul sulfuric:
- HNO 2 + H 2 SO 4 → NOHSO 4 + H 2 O
compusul se formează în timpul preparării sărurilor de diazoniu . [2] [3]
De asemenea, se formează în procesul camerelor de plumb pentru a recupera catalizatorul care este dioxidul de azot :
- NO + NO 2 + 2H 2 SO 4 ⇄ 2NOHSO 4 + H 2 O
echilibrul este reglat în principal de concentrația de acid sulfuric: dacă este prezent în exces, reacția este deplasată spre dreapta, diluția readuce sistemul înapoi la reactivi. Deoarece reacția este exotermă, produsele sunt favorizate de temperaturi scăzute.
Amestecul de acid sulfuric și nitrosilsulfuric se numește „azotat”.
Notă
- ^ Sigma Aldrich; rev. din 24.12.2012, referindu-se la soluția apoasă la 40%
- ^ HH Hodgson, AP Mahadevan, ER Ward, 1,4-Dinitronaphthalene Organic Syntheses, 1955 , 3, 341
- ^ RB Sandin, TL Cairns, 1,2,3-Triiode-5-nitrobenzene Organic Syntheses, 1943 , 2, 604; 1939 , 19, 81
Bibliografie
- L. Berti, M. Calatozzolo, R. Di Bartolo, The sulfur and chlor-soda industry . Editura G. D'Anna ISBN 88-8104-166-9
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere despre acidul nitrosilsulfuric
Wikimedia Commons conține imagini sau alte fișiere despre acidul nitrosilsulfuric