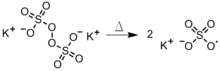Polimerizarea radicalilor liberi
Polimerizarea radicalilor liberi este o metodă de polimerizare în lanț prin care se formează un polimer prin adăugarea ulterioară a unui radical liber . Există mai multe metode prin care se pot forma radicalii liberi, pornind în general de la moleculele inițiatorului. Aceste specii radicale (numite radicali primari ) sunt apoi capabili să reacționeze cu unități monomerice , generând centrele active pe care se vor dezvolta lanțurile (numite radicali secundari ). [1]
Cu acest tip de reacție chimică, se pot obține diverse macromolecule și materiale compozite . Natura relativ nespecifică a interacțiunilor chimice ale radicalilor înseamnă că acest proces este utilizat pe scară largă. În 2001, o treime din polimerii produși în Statele Unite au fost fabricate urmând această metodologie. [2]
Faza de inițiere
Este prima etapă de polimerizare. În această fază se creează un centru activ care va funcționa ca un punct de plecare pentru creșterea lanțului macromolecular. Nu toți monomerii funcționează bine cu orice inițiator. Faza de inițiere radicală este optimă cu dublele legături carbon-carbon ale monomerilor vinilici și cu gruparea carbonil (dublă legătură carbon-oxigen) prezentă în aldehide și cetone. Această etapă a reacției poate fi împărțită în două reacții distincte: inițial radicalii sunt creați de o moleculă inițiator ( radicali primari ), ulterior aceștia atacă unitățile de monomeri din împrejurimi.
Există diferite tipuri de inițiatori și modalități de inițiere a polimerizării radicale.
Tipuri de inițiator și faza de inițiere
- Descompunerea termică
- Inițiatorul este încălzit până când apare ruptura homolitică a legăturii covalente, din care provin doi radicali (Figura 1). Această metodă funcționează bine cu peroxizi organici și compuși azoici. [3]
 Figura 1 : Descompunerea termică a peroxidului de cumil
Figura 1 : Descompunerea termică a peroxidului de cumil - Fotoliză
- Radiația rupe legătura omolitic, generând doi radicali, ca în figura 2. Această metodă este în general utilizată cu ioduri metalice, alchil-metale și compuși azoici. [3]Inițierea fotolitică poate avea loc, de asemenea, printr-o extracție bimoleculară de hidrogen atunci când radicalul se află în starea sa cea mai scăzută de triplet. [4] : Fotoliza impune inițiatorului să îndeplinească următoarele cerințe: [4]
 Figura 2 : Fotoliza azobisisobutironitrilului (AIBN)
Figura 2 : Fotoliza azobisisobutironitrilului (AIBN)- Absorbibilitate ridicată în intervalul 300-400 nm.
- Eficiență bună în generarea de radicali capabili să atace legături duble C = C.
- Solubilitate adecvată în sistemul polimer-monomer.
- Nu conferă culori gălbui sau mirosuri neplăcute materialului finit.
- Fotoiniciatorul și orice produse secundare rezultate trebuie să fie netoxice.
- Reacții redox
- Reducerea peroxidului de hidrogen sau a peroxidului de hidrogen alchil prin fier este destul de frecventă. [3] Alți agenți reducători utilizați sunt Cr 2+ , V 2+ , Ti 3+ , Co 2+ și Cu + . [2]
- Persulfati
- Disocierea persulfatului în faza apoasă (Figura 3) este o metodă utilă în polimerizarea în emulsie , în care radicalul se difuzează printr-o picătură hidrofobă de monomer. [3]
- Radiații ionizante
- Radiațiile α , β , γ și x determină expulzarea unui electron din molecula inițiatorului, urmată de disociere și captarea electronilor pentru a produce un radical (Figura 4). [3]
- Prin electrochimie
- Electroliza unei soluții care conține atât monomeri cât și electroliți este o altă alternativă.O moleculă de monomer primește un electron la catod și se transformă într-un anion radical, în timp ce un monomer la anod pierde un electron și devine un radical cationic (figura 5). Ionii radicali pot iniția acum polimerizarea radicală și / sau ionică. De obicei, această metodă este aleasă atunci când doriți să acoperiți suprafața unui metal cu pelicule polimerice (filme). [5]
Notă
- ^ Glosar de termeni de bază în știința polimerilor (Recomandările IUPAC 1996) ( PDF ), în Chimie pură și aplicată , vol. 68, nr. 12, 1996, pp. 2287–2311, DOI : 10.1351 / pac199668122287 .
- ^ a b George Odian, Principiile polimerizării , 4th, New York, Wiley-Interscience, 2004, ISBN 978-0-471-27400-1 .
- ^ a b c d e JMG Cowie și Arrighi, Valeria, Polymers: Chemistry and Physics of Modern Materials , 3rd, Scotland, CRC Press, 2008, ISBN 0-8493-9813-4 .
- ^ a b HJ Hageman, Photoinitiators for Free Radical Polymerization , in Progress in Organic Coatings , vol. 13, n. 2, 1985, pp. 123-150, DOI : 10.1016 / 0033-0655 (85) 80021-2 .
- ^ Malcolm P. Stevens,Polymer Chemistry: An Introduction , New York, Oxford University Press, 1999, ISBN 0-19-512444-8 .
Bibliografie
- AIM, Fundamentals of science of polymers , Pisa, Pacini Editore, februarie 2003, capitolul 15 „Polimerizare radicală”.