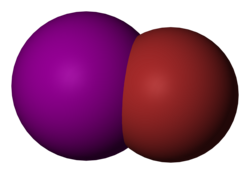
Bromură de iod (I)
| Bromură de iod (I) | |
|---|---|
| Numele IUPAC | |
| bromură de iod (I), monobromură de iod | |
| Denumiri alternative | |
| bromură de iod | |
| Caracteristici generale | |
| Formula moleculară sau brută | BrI |
| Greutatea formulei ( u ) | 206,81 |
| Aspect | cristale negre |
| numar CAS | |
| Numărul EINECS | 232-159-9 |
| PubChem | 82238 |
| ZÂMBETE | BrI |
| Proprietăți fizico-chimice | |
| Densitate (g / cm 3 , în cs ) | 4.3 [1] |
| Solubilitate în apă | se descompune [2] |
| Temperatură de topire | 40 ° C (313 K) [1] |
| Temperatura de fierbere | 116 ° C (389 K) dec [1] |
| Proprietăți termochimice | |
| Δ f H 0 (kJ mol −1 ) | -10,5 [3] |
| Informații de siguranță | |
| Simboluri de pericol chimic | |
  | |
| Pericol | |
| Fraze H | 314 - 335 [2] |
| Sfaturi P | 280 - 301 + 330 + 331 - 303 + 361 + 353 - 304 + 340 - 305 + 351 + 338 - 310 [2] |
Bromura de iod (I) sau monobromura de iod este compusul anorganic interhalogen cu formula IBr. În această bromură iodul se află în starea de oxidare +1. Este o specie destul de stabilă și poate fi obținută la temperatura camerei sub formă de cristale negre. [3] [4] Poate fi utilizat în reacțiile de halogenare a substanțelor organice. Iodul și bromul pot forma, de asemenea, bromură de iod (III), IBr 3 . [5]
Sinteză
Compusul a fost descris pentru prima dată în 1826 de Antoine Jérôme Balard , farmacist și chimist din Montpellier , descoperitor al bromului. [6] Compusul este obținut prin sinteză directă din iod și brom; compusul brut este apoi purificat prin cristalizare fracționată: [3]
Structură și proprietăți
IBr cristalizează în sistemul ortorombic , grup spațial Ccm2 1 , cu constante de rețea a = 490 pm , b = 699 pm și c = 893 pm , patru unități de formulă pe unitate de celulă . [7]
IBr este cel mai puțin volatil dintre interhalogenii diatomici; rezultatele distanței internucleare I - Br 252 pm . În stare topită compusul prezintă o conductivitate echitabilă, datorită unei reacții de disociere care poate fi reprezentată ca [3]
IBr este compus din acid Lewis și, prin urmare, este potrivit pentru formarea aductilor de transfer de sarcină cu donatori, de exemplu calcogeni. [8]
Notă
- ^ a b c Lide 2005
- ^ a b c GESTIS 2019
- ^ a b c d Greenwood și Earnshaw 1997
- ^ Holleman și Wiberg 2007
- ^ Jackisch 1998
- ^ Ballard 1826 , p. 372 .
- ^ Swink și Carpenter 1968
- ^ (EN) Carla M. Aragoni, Massimiliano Arca și Francis Demartin, calcule DFT, studii structurale și spectroscopice asupra produselor formate între IBr și N, N'-dimetilbenzoimidazol-2 (3H) -tionă și -2 (3H) -selonă , în Dalton Transactions , n. 13, 16 iunie 2005, pp. 2252-2258, DOI : 10.1039 / B503883A . Adus la 22 martie 2021 .
Bibliografie
- ( FR ) M. Balard, Sur une substance particulière contaue dans l'eau de la mer , în Ann. Chim. Fizic. , vol. 32, 1826, pp. 337-383.
- GESTIS, bromură de iod , pe gestis-en.itrust.de , 2019. Adus 22 februarie 2019 . Pagina de bromură de iod din baza de date GESTIS.
- ( EN ) NN Greenwood și A. Earnshaw, Chimia elementelor , ediția a II-a, Oxford, Butterworth-Heinemann, 1997, ISBN 0-7506-3365-4 .
- ( DE ) AF Holleman și N. Wiberg, Lehrbuch der Anorganischen Chemie , Berlin, Walter de Gruyter, 2007, ISBN 978-3-11-017770-1 .
- ( EN ) PF Jackisch, Bromine Compounds , în Kirk-Othmer Encyclopedia of Chemical Technology , ediția a IV-a, John Wiley & Sons, 1998.
- DR Lide (Editor), CRC Handbook of Chemistry and Physics, Internet Version 2005 , at hbcponline.com , CRC Press, Boca Raton, 2005. Accesat la 9 decembrie 2017 .
- ( EN ) LN Swink și GB Carpenter, Structura cristalină a monobromurii de iod, IBr , în Acta Cryst. , B24, 1968, pp. 429-433, DOI : 10.1107 / S0567740868002505 .
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere pe monobromură de iod
Wikimedia Commons conține imagini sau alte fișiere pe monobromură de iod