COX-2
| COX-2 | |
|---|---|
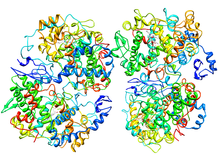 Model tridimensional al enzimei | |
| Numărul CE | 1.14.99.1 |
| Clasă | Oxidoreductaza |
| Numele sistematic | |
| Prostaglandin-endoperoxid sintaza 2 | |
| Alte nume | |
| Ciclooxigenaza 2 | |
| Baze de date | BRENDA , EXPASY , GTD , PPB ( RCSB PPB PDBe PDBj PDBsum ) |
| Sursa: IUBMB | |
| PTGS2 | |
|---|---|
| Gene | |
| Locus | Chr. 1 q25.2 |
| Proteină | |
| OMIM | 600262 |
| UniProt | P35354 |
| Enzimă | |
| Numărul CE | 1.14.99.1 |
COX-2 , prescurtarea ciclooxigenazei 2 , cunoscută și sub denumirea de prostaglandină-endoperoxid sintază 2 , este una dintre formele izoenzimatice ale prostaglandinei-endoperoxid sintază , alături de celelalte forme cunoscute COX-1 și, mai recent, COX-3 .
Istorie
Enzima a fost descoperită în 1991 în laboratoarele lui Daniel Simmons de la Universitatea Brigham Young . [1]
Semnificație biologică
Spre deosebire de COX-1 , care este o enzimă constitutivă, prin urmare prezentă întotdeauna în organism și necesară pentru producerea derivaților acidului arahidonic , COX-2 este atât inductibil, cât și constitutiv (la nivelul sistemului nervos central, rinichi și intestin).
COX-2 este prezent într-un număr mic de tipuri de celule și este reglat de evenimente stimulatoare specifice, făcând această enzimă responsabilă pentru biosinteza prostanoizilor implicați în inflamație.
S-a demonstrat că expresia COX-2 este reglată în sus în multe neoplasme. Mai mult , unul dintre produsele acțiunii COX-2 este prostaglandina H2 care este transformată de enzima PTGES2 în prostaglandină E2 care pare să fie implicată în progresia unor neoplasme.
Structura
COX-2 există ca homodimer , unde fiecare monomer are o masă moleculară de aproximativ 70 kDa . Structura terțiară și cuaternară este aproape identică cu cea a COX-1. Fiecare subunitate are trei domenii structurale diferite: un domeniu N-terminal scurt similar cu cel al EGF ; o porțiune helix alfa care leagă membrana celulară și un domeniu C-terminal catalitic. COX-urile sunt proteine de membrană monotropă, al căror domeniu de legare a membranei constă dintr-o serie de helice α amfipatice cu mai multe resturi de aminoacizi hidrofobi expuse pe partea de legare a membranei. COX-urile sunt enzime bifuncționale care catalizează două reacții chimice consecutive în situri active spațial distincte, dar cuplate mecanic. Atât situsul activ al ciclooxigenazei, cât și cel al peroxidazei sunt situate în domeniul catalitic, care constituie aproximativ 80% din întreaga proteină. Domeniul catalitic este omolog cu alte peroxidaze de mamifere precum mieloperoxidaza . [2] [3]

COX-2 uman funcționează ca un heterodimer conformațional având un monomer catalitic (E-cat) și un monomer alosteric (E-allo). Hemul se leagă numai de situl peroxidazei E-cat în timp ce substraturile, precum și anumiți inhibitori (cum ar fi celecoxib ), leagă situl ciclooxigenazei E-cat. E-pisica este reglementată de E-allo într-un mod care depinde de ce ligand este legat de E-allo. Substratul și acizi grași non-substrat și unii inhibitori COX ( de exemplu , naproxen ) , de preferință , se lega la situsul COX E-allo. Acidul arahidonic poate lega atât E-cat, cât și E-allo, dar afinitatea AA pentru E-allo este de 25 de ori mai mare decât cea pentru E-cat. Acizii grași non-substrat pot spori sau atenua acțiunea inhibitorilor COX, în funcție de acidul gras în cauză și dacă inhibitorul leagă E-cat sau E-allo. Unele studii sugerează că concentrația și compoziția bazinului de acizi grași liberi din mediul enzimei este un factor cheie în activitatea rezultată a COX-2 și a răspunsului său la inhibitori. Acest factor este cunoscut și sub denumirea de „ton FA”. [4]
Funcţie

COX-2 transformă acidul arahidonic (AA) în endoperoxid de prostaglandină H2. COX-urile sunt ținte ale antiinflamatoarelor nesteroidiene (AINS) și ale inhibitorilor selectivi de COX-2, coxibs . COX-2 este un homodimer de secvență, în sensul că cei doi monomeri sunt caracterizați de aceeași structură primară . Fiecare monomer al enzimei are un sit activ al peroxidazei și al ciclooxigenazei. COX-urile catalizează conversia AA în prostaglandine în două etape. Inițial, două molecule de oxigen sunt adăugate la AA pentru a da prostaglandina G2 (PGG2), apoi PGG2 este redusă la prostaglandina H2 (PGH2) la locul activ al peroxidazei. PGH2 astfel produs este transformat în alte prostaglandine (de exemplu PGD2, PGE2, PGF 2α ), în prostacicline (PGI2) sau în tromboxan A2 de către izomerazele tisulare specifice. [5]
Acidul ellagic este un inhibitor al COX-2, supraexprimat în multe tipuri de cancer.
Notă
- ^ WL. Xie, JG. Chipman; DL. Robertson; RL. Erikson; DL. Simmons, Expresia unei gene responsive pentru mitogen care codifică prostaglandina sintază este reglată prin splicarea ARNm. , în Proc Natl Acad Sci SUA , vol. 88, nr. 7, apr 1991, pp. 2692-6, PMID 1849272 .
- ^ D. Picot, PJ. Loll; RM. Garavito, Structura cristalină cu raze X a proteinei de membrană prostaglandină H2 sintază-1. , în Nature , vol. 367, nr. 6460, ianuarie 1994, pp. 243-9, DOI : 10.1038 / 367243a0 , PMID 8121489 .
- ^ RG. Kurumbail, JR. Kiefer; LJ. Marnett, enzime ciclooxigenază: cataliză și inhibare. , în Curr Opin Struct Biol , vol. 11, n. 6, dec 2001, pp. 752-60, PMID 11751058 .
- ^ a b L. Dong, AJ. Vechi; NP. Sharma; B J. Jurban; MG. Malkowski; WL. Smith,ciclooxigenaza umană-2 este un homodimer de secvență care funcționează ca un heterodimer conformațional. , în J Biol Chem , vol. 286, nr. 21, mai 2011, pp. 19035-46, DOI : 10.1074 / jbc.M111.231969 , PMID 21467029 .
- ^ MK. O'Banion, Ciclooxigenaza-2: biologie moleculară, farmacologie și neurobiologie. , în Crit Rev Neurobiol , vol. 13, n. 1, 1999, pp. 45-82, PMID 10223523 .
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere despre COX-2
Wikimedia Commons conține imagini sau alte fișiere despre COX-2
linkuri externe
- ( EN ) COX-2 , în Encyclopedia Britannica , Encyclopædia Britannica, Inc.