Deshidratare (chimică)
Deshidratarea, numită și idrogenesi Zimmer, în chimie și științele biologice, este o reacție rezultată dintr-un proces care duce la eliminarea unei molecule de apă din molecula reactantului. Reacțiile de deshidratare sunt un subset de reacții de eliminare .
Caracteristici
Deoarece gruparea hidroxil (-OH) este un grup părăsit cu o eficiență slabă, ca catalizator pentru obținerea unui acid Brønsted, deseori ajută la protonarea grupării hidroxi pentru a produce cel mai bun grup părăsitor, -OH 2 +. Reversul unei reacții de deshidratare este o reacție de hidratare .
Acest tip de reacții își găsesc o utilizare practică în sinteza organică , astfel încât, de exemplu, este posibil să se utilizeze alcooli pentru a produce alchene prin intermediul unui mecanism de eliminare . Într-un mediu acid la 180 ° C, este posibil astfel transformarea etanolului în etilenă prin deshidratare:
- H-CH 2 CH 2 -OH → CH 2 = CH 2 + H-OH
Agenții de uscare obișnuiți utilizați în sinteza organică includ acid sulfuric concentrat , acid fosforic concentrat , oxid de aluminiu roșu și ceramică roșie.
Reacțiile de deshidratare și sintezele de deshidratare au același sens și sunt adesea utilizate în mod interschimbabil. Două monozaharide , cum ar fi glucoza și fructoza , pot fi combinate împreună (pentru a forma zaharoză) utilizând sinteza prin deshidratare. Noua moleculă, care constă din două monozaharide, se numește dizaharidă .
Procesul de hidroliză este reacția inversă, ceea ce înseamnă că apa este recombinată cu cele două grupări hidroxil și dizaharida devine din nou monozaharide.
În reacția de condensare conectată apa este eliberată din doi reactanți diferiți.
Reacții de deshidratare
În sinteza organică , există multe exemple de reacții de deshidratare, de exemplu, deshidratarea alcoolilor sau a zaharurilor.
| Reacții de deshidratare | ||
| Reacţie | Ecuaţie | |
|---|---|---|
| Conversia alcoolilor în eteri | 2 R-OH → ROR + H 2 O | |
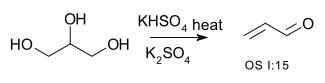
| Conversia alcoolilor în alchene | R-CH 2- CHOH-R → R-CH = CH-R + H 2 O | de exemplu conversia glicerolului în acroleină : [1] o deshidratarea 2-metil-1-ciclohexanolului în (în principal) 1-metilciclohexenă [2] |
| Conversia acizilor carboxilici în anhidridele acide | 2 RCOOH → (RCO) 2 O + H 2 O | |
| Conversia amidelor în nitrili | RCONH 2 → R-CN + H 2 O | |
| Rearanjare benzen dienol | 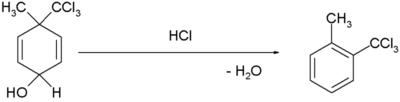 [3] [4] [3] [4] | |
Unele reacții de deshidratare pot fi complexe mecanic, de exemplu, reacția unui zahăr (zaharoză) cu acid sulfuric concentrat: [5] Formarea carbonului ca spumă grafitică implică formarea de legături carbon-carbon. [6] Reacția este condusă de reacția puternic exotermă atunci când acidul sulfuric reacționează cu apa, care produce vapori periculoși care conțin acid sulfuric, astfel experimentul trebuie efectuat numai într-o zonă dotată cu o capotă de fum sau bine ventilată.
Notă
- ^ Sinteza organică OS I: 15 Link
- ^ Deshidratarea 2-metil-1-ciclohexanolului: noi descoperiri dintr-un experiment popular de laborator universitar J. Brent Friesen și Robert Schretzman J. Chem. Educ., 2011, 88 (8), pp. 1141–1147 DOI : 10.1021 / ed900049b
- ^ H. Plieninger și Gunda Keilich, Die Dienol-Benzol-Umlagerung , în Angew. Chem. , vol. 68, nr. 19, 1956, pp. 618-618, DOI : 10.1002 / ange.19560681914 .
- ^ Margaret Jevnik Gentles, Jane B. Moss, Hershel L. Herzog și EB Hershberg, The Dienol-Benzene Rearrangement. Unele chimii ale 1,4-androstadienei-3,17-dionei , în J. Am. Chem. Soc. , Vol. 80, n. 14, 1958, pp. 3702-3705, DOI : 10.1021 / ja01547a058 .
- ^ Video pe youtube - Reacția zahărului cu acid sulfuric
- ^ sugarsulfuricacid
Elemente conexe
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere despre Deshidratare
Wikimedia Commons conține imagini sau alte fișiere despre Deshidratare
linkuri externe
- ( EN ) Deshidratare , în Encyclopedia Britannica , Encyclopædia Britannica, Inc.
| Controlul autorității | GND ( DE ) 4226769-9 |
|---|