Oxidarea Oppenauer
Oxidarea Oppenauer este o reacție secundară de oxidare a alcoolilor la cetone .
Alcoolul este oxidat cu izopropoxid de aluminiu în exces de acetonă . Oxidarea este foarte selectivă pentru alcoolii secundari și nu oxidează alte grupe funcționale sensibile , cum ar fi aminele și sulfurile .
Un exemplu de aplicare poate fi găsit în chimia farmaceutică, pentru a sintetiza compuși steroizi de interes clinic. Procesul vede colesterolul ca primul său termen, care este transformat în pregnenolonă prin scindarea oxidativă a lanțului lateral. Pregnenolonul este un precursor al androgenilor, estrogenilor, progestogenilor, corticosteroizilor și moleculelor care au structural nucleul ciclopentanoperhidrofenantrenului , comun hormonilor, dar prezintă funcție anabolică sau antiinflamatoare. Reacția Oppenauer are ca substrat hidroxilul secundar plasat în poziția 3 pe inelul pregnenolon A (sau derivații acestuia, funcționalizați diferit), care este oxidat la cetonă. Cu toate acestea, izopropoxidul de aluminiu nu este doar un reactiv oxidant, ci și un compus bazic și poate provoca schimbări prototrope interne. Compuși precum colosterol, pregnenolon și analogi, care au o legătură olefinică în poziția 5, pot suferi o deplasare a legăturii duble, cu formarea unei cetone α, β-nesaturate.
Mecanism de reacție
Mecanismul de reacție al oxidării Oppenauer este după cum urmează:
În prima etapă a mecanismului, alcoolul (1) interacționează cu aluminiul pentru a forma complexul (3), care este deprotonat în a doua etapă de un ion alcoxid (4) pentru a forma un intermediar alcoxid (5). În cea de-a treia etapă, atât acetona (7) cât și substratul alcoolic sunt legate de aluminiu. complexul este activat prin mutarea ionului hidrură al carbonului din α al alcoolului în carbonil carbon al acetonei printr-o stare de tranziție care implică 6 atomi (8). După deplasarea ionului hidrură, se formează cetona dorită. [1]
Beneficii
Avantajele oxidării Oppenauer sunt multiple. unul dintre avantaje este că folosește reactivi ieftini și netoxici. condițiile de reacție sunt foarte agreabile, deoarece substratul este de obicei încălzit în amestecuri de acetonă / benzen . Un alt avantaj al oxidării Oppenauer față de alte tehnici (cum ar fi utilizarea PCC ) este că alcoolii secundari sunt oxidați mai repede decât alcoolii primari. Mai mult, nu există o metodă alternativă de oxidare de către aldehide și acizi (spre deosebire de oxidarea Jones). [1]
Variante ale reacției
Reacția Wettstein-Oppenauer
În reacția Wettstein-Opppenauer, descoperită de Wettstein în 1945, Δ 5–3β-hidroxi steroizi sunt oxidați la Δ 4,6-3-ceto steroizi cu benzoquinonă ca acceptor de legătură de hidrogen . Această reacție este utilizată pentru prepararea de Δ 4,6-3-ceto steroizi într-o singură etapă.
Modificările lui Woodward
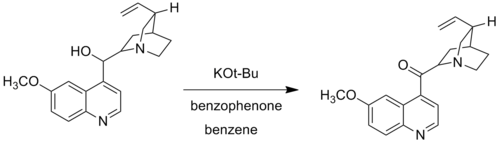
În modificările Woodward, alcoxidul de aluminiu este înlocuit cu terț-butoxidul de potasiu. Modificarea lui Woodward a oxidării Oppenauer, numită și „oxidarea Oppenauer-Woodward”, este utilizată atunci când anumite grupări de alcool nu sunt oxidate în condițiile standard de reacție Oppenauer. De exemplu, Woodward folosește terț-butoxidul de potasiu și benzofenona pentru oxidarea de la chinolină la chinolonă, deoarece sistemul tradițional de alumină catalitică nu reușește să oxideze chinolinele, deoarece formează un complex de coordonare pe azot (baza Lewis) cu aluminiu. [2]
Alte modificări
Au fost raportate modificări majore ale catalizatorului de alcool de aluminiu. De exemplu, un catalizator puternic a fost raportat de Mamoke și colaboratorii săi pentru oxidarea corvusului la corvone (un membru al familiei terpenoide ) cu randament excelent (94%). [3]
Aplicații sintetice
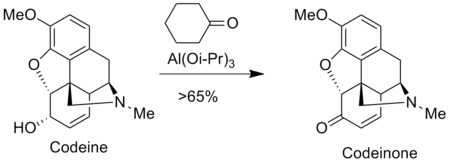
Oxidarea Oppenauer este utilizată pentru producerea de analgezice în industria farmaceutică, cum ar fi morfina și codeina . de exemplu, codeinona este preparată prin oxidarea Oppenauer din codeină. [4]
Oxidarea Oppenauer este, de asemenea, utilizată pentru sinteza hormonală . Progesteronul este produs din oxidarea de către Oppenauer a pregnolonei . [5]
O ușoară variantă de oxidare Oppenauer este utilizată pentru a sintetiza derivați steroizi . De exemplu, a fost dezvoltată o variație catalitică eficientă a reacției care utilizează ruteniu pentru oxidarea 3-hidroxi- steroizilor 5-nesaturați din derivații corespunzători 4-en-3-oni.
Oxidarea Oppenauer este utilizată și pentru sinteza lactonelor din 1,4 și 1,5 dioli . [6]
Efecte colaterale
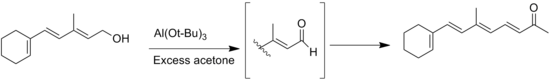
O reacție secundară obișnuită este condensarea aldolică catalizată de bază a produselor aldeice având α-hidrogeni utilizați pentru a favoriza β-hidroxi aldehidele nesaturate sau α, ß-hidroxi aldehide. [7]
O altă reacție secundară este reacția Tischenko a produselor aldeice fără α-hidrogeni. Această reacție poate fi evitată preventiv folosind numai solvenți anhidri . O altă reacție secundară este migrarea legăturii duble în timpul oxidării alcoolului alilic al substratului. [1] O altă reacție secundară generală este migrarea dublei legături în timpul oxidării substraturilor alcoolice alilice . [8]
Notă
- ^ a b c EJ Corey și Nicolaou, KC, Aplicații strategice ale reacțiilor numite în sinteza organică , Elsevier, 2005, ISBN 978-7-03-019190-8 .
- ^ RB Woodward, NL Wendler și FJ Brutschy, Quininone1 , în J. Am. Chem. Soc. , Vol. 67, nr. 9, 1945, p. 1425, DOI : 10.1021 / ja01225a001 .
- ^ T Ooi, H Otsuka, T Miura, H Ichikawa și K Maruoka, oxidare practică Oppenauer (OPP) a alcoolilor cu un catalizator de aluminiu modificat , în Organic Letters , vol. 4, nr. 16, 2002, pp. 2669-72, DOI : 10.1021 / ol020094c , PMID 12153205 .
- ^ Stéphane Caron, Robert W. Dugger, Sally Gut Ruggeri, John A. Ragan și David H. Brown Ripin, Oxidări pe scară largă în industria farmaceutică , în Chem. Rev. , vol. 106, nr. 7, 2006, pp. 2943-89, DOI : 10.1021 / cr040679f , PMID 16836305 .
- ^ P Dewick, Medicinal Natural Products: A Biosynthetic Approach , 2nd, Wiley & Sons, 2001, p. 243, ISBN 0-471-49640-5 .
- ^ L. Eignerova și A. Kasal, Intramolecular hydride shift in Oppenauer oxidation of some dihydroxy steroids , in Collect. Ceh. Chem. Comun. , vol. 41, nr. 4, 1976, pp. 1056-1065, DOI : 10.1135 / cccc19761056 .
- ^ NA Milas, FX Grossi, SE Penner și S. Kahn, The Synthesis of 1- [ciclohexen-1'-il] -3-Methyl-1,3,5-Octatrien-7-One (C 15 Ketone) 1 , în Journal of the American Chemical Society , vol. 70, nr. 3, 1948, p. 1292, DOI : 10.1021 / ja01183a522 .
- ^ R. Reich și JFW Keana, Oppenauer Oxidations Using 1-Methyl-4-Piperidone as the Hydride Acceptor , în Synthetic Communications , vol. 2, nr. 5, 1972, p. 323, DOI : 10.1080 / 00397917208061988 .
- ^ Richard Reich și John FW Keana, Oppenauer Oxidations Using 1-Methyl-4-Piperidone as the Hydride Acceptor , in Synth. Comun. , vol. 2, nr. 5, 1972, pp. 323-325, DOI : 10.1080 / 00397917208061988 .
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere despre Oppenauer Oxidation
Wikimedia Commons conține imagini sau alte fișiere despre Oppenauer Oxidation






![Oxidarea opozantă a unui derivat de steroizi. [9]](http://upload.wikimedia.org/wikipedia/commons/thumb/3/36/Wiki-oppenaure-mxa2.tif/lossy-page1-350px-Wiki-oppenaure-mxa2.tif.jpg)