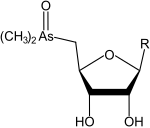
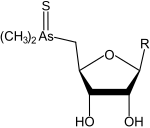
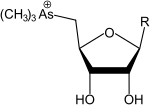
Arsenozuccheri
Arsenozuccheri sunt compuși organici compuși din 3 părți diferite: [1]
- un nucleu 5-deoxipentozic;
- o grupare arsinoil (–AsR 2 (= O)), arsinotioil (–AsR 2 (= S)) sau arsonio (-As + R 3 ) legată de carbonul 5 al inelului. În acest grup, arsenicul poate fi trivalent sau pentavalent, poate fi legat de un atom de oxigen (ossoarsenozuccheri), de un atom de sulf (tioarsenozuccheri) și / sau de mai multe grupări metil (arsinoil dimetilat dacă 2, arsonio trimetilat dacă 3);
- un lanț legat de carbonul 1 al inelului, care poate fi constituit din grupe funcționale foarte variate.
Cele mai frecvente zaharuri de arsenic sunt zaharurile dimetilate de oxo-arsenic cu arsenic pentavalent și, în special, cele 4 principale sunt glicerol , fosfat , sulfat și arsenosugari sulfonat . [1]
Acești compuși constituie forma predominantă de arsen în alge , dar sunt prezenți și în moluștele erbivore și gastropodele în cantități semnificative. [2]
Nomenclatură
Deoarece structura arsenozuccheri este relativ complexă, numele lor IUPAC sunt foarte lungi și impracticabile. Din acest motiv, în literatura de specialitate s-au făcut încercări de nomenclatură prescurtată, dar nu există una oficială.
În anii optzeci , japonezii Morita și Shibata [3] [4] au început să folosească cifre romane pentru a identifica arsenozuccheri (împreună cu alte specii de arsenic); această convenție a fost apoi urmată de alți autori. [5] În 1994 Kevin Francesconi [5] a propus ca cei 4 arsenozuccheri principali să fie numiți cu un nume comun care, deși nu este exact din punct de vedere chimic, ar putea identifica principalele lor caracteristici structurale: chiar și astăzi acești compuși sunt numiți glicerol arsenozucchero , fosfat , sulfat și sulfonat .
În 2005 , pentru prima dată, a fost propus un sistem mai general de nomenclatură. În articolul lor publicat în Analytical Chemistry , [6] Nischwitz și Pergantis au folosit abrevieri care conțin principalele informații structurale ale compușilor:
- numărul de grupări metil legate de arsenic: „DM” (dimetil) sau „TM” (trimetil);
- dacă arsenul este legat de un atom de sulf , se adaugă „tio”;
- nucleul arsenoribofuranozidic este indicat cu „AsSugar” (dar poate fi omis dacă în context vorbim doar de arsenozuccheri);
- în cele din urmă, se adaugă un nume corespunzător grupului funcțional caracteristic al lanțului lateral legat de carbonul 1 al inelului ("Sulfat", "Sulfonat" etc.).
De exemplu, arsenic trimetilat 3- [5'-deoxi-5 '- (trimetilarsoniu) -β-ribofuranoziloxi] -2-hidroxipropilen glicol prin aceste convenții este pur și simplu numit TMAsSugarGlycerol.
În sfârșit, în 2011, Jörg Feldmann [2] a făcut distincția între As III , As V și arsonio folosind respectiv formele DMA III -sugar- nume (de exemplu, DMA III -sugar-glicerol), DMA V -sugar- substantiv (de exemplu, DMA V -zahăr-glicerol) sau TMA-zahăr- denumire (de ex. TMA-zahăr-glicerol).
Lista arsenozuccheri
Sunt enumerați toți arsenozuccheri descoperiți până în prezent, raportând numele comun conform nomenclaturii propuse de Nischwitz și Pergantis [6] , numele complet și referințele bibliografice (ale primei descoperiri a compusului sau a numelui folosit).
Zaharuri dimetilate osoase
| R. | Denumirea comună | Numele complet | Ref. |
|---|---|---|---|
| | DMAsSugarGlycerol | 3- [5'-deoxi-5 '- (dimetilarsinoil) -β-ribofuranoziloxi] -2-hidroxipropilen glicol | [1] [7] |
 | DMA Zahar Fosfat | 3- [5'-deoxi-5 '- (dimetilarsinoil) -β-ribofuranoziloxi] -2-hidroxipropil 2,3-hidroxipropil fosfat | [1] [7] |
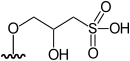 | DMAsSulfonat de zahăr | Acid 3- [5'-deoxi-5 '- (dimetilarsinoil) -β-ribofuranoziloxi] -2-hidroxipropansulfonic | [1] [7] |
 | DMAsSulfat de zahăr | 3- [5'-deoxi-5 '- (dimetilarsinoil) -β-ribofuranoziloxi] -2-hidroxipropil hidrogen sulfat | [1] [7] |
 | DMAsSugarAminoSulfonate | Acid 2-amino-3- [5-deoxi-5- (dimetilarsinoil) -β-D-ribofuranoziloxi] propen-1-sulfonic | [1] [8] |
| | DMAsSugarHydroxy | 5-dimetilarsinoil-β-ribofuranozol | [1] [9] |
| | DMAsSugarMethoxy | 5-deoxi-5- (dimetilarsinoil) -β-D-ribozid metilic | [1] [10] |
 | DMAsSugarCarboxyl | Acid 3- (5'-deoxi-5'-dimetilarsinoil-β-D-riboziloxi) -2-hidroxipropanoic | [1] [11] |
 | DMAsSugarCarbamate | N - (5'-deoxi-5'-dimetilarsinoil-β-D-riboziloxicarbonil) glicină | [1] [11] |
 | DMAsSugarMannitol | 1- O - [5'-deoxi-5 '- (dimetilarsinoil) -β-D-ribozil] manitol | [1] [10] |
 | DMAsSugarAdenine | 5'-dimetilarsinoil-adenozină | [6] [11] |
 | DMAsSugarCarboxyl-2 | Acid 2- [5-deoxi-5- (dimetilarsinoil) -β-ribofuranoziloxi] -acetic | [9] [12] |
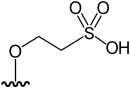 | DMAsSulfonat de zahăr-2 | Acid 2- [5-deoxi-5- (dimetilarsinoil) -β-ribofuranoziloxi] -etan sulfonic | [12] |
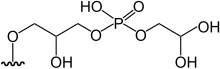 | 3- [5'-deoxi-5 '- (dimetilarsinoil) -β-ribofuranoziloxi] -2-hidroxipropil 2, di-hidroxietil fosfat | [9] | |
 | [10] [13] | ||
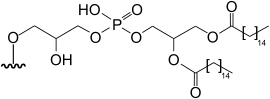 | dipalmitoilglicerofosfo-2-hidroxipropil-5-deoxi-5- (dimetilarsinoil) -β-ribofuranozidă | [13] [14] |
Tioarsenozuccheri dimetilati
| R. | Denumirea comună | Numele complet | Ref. |
|---|---|---|---|
| | DMThioAsSugarGlycerol | [6] | |
 | DMThioAsSugarFosfat | [6] | |
 | DMThioAsSugarSulfonate | [6] [15] | |
 | DMThioAsSulfat de zahăr | [6] [15] |
Arsenozuccheri trimetilati
| R. | Denumirea comună | Numele complet | Ref. |
|---|---|---|---|
| | TMA Zahar Glicerol | 3- [5'-deoxi-5 '- (trimetilarsoniu) -β-ribofuranoziloxi] -2-hidroxipropilen glicol | [6] [16] |
 | TMAsSulfat de zahăr | 3 '- [5-deoxi-5- (trimetilarsoniu) -β-D-riboziloxi] -2'-hidroxipropil sulfat | [6] [10] |
 | TMA Zahar Fosfat | 3- [5'-deoxi-5 '- (trimetilarsoniu) -β-ribofuranoziloxi] -2-hidroxipropil 2,3-hidroxipropil fosfat | [6] |
 | TMAsSulfonat de zahăr | Acid 3- [5'-deoxi-5 '- (trimetilarsoniu) -β-ribofuranoziloxi] -2-hidroxipropansulfonic | [6] |
 | TMAsSugarAminoSulfonate | [17] | |
| | TMAsSugarHydroxy | 5-trimetilarsoniu-β-ribofuranoză | [1] [9] |
| | TMAs ZaharMetoxi | metil- (5-deoxi-5-trimetilarsoniu) -β-ribofuranozidă | [12] |
Alte arsenozuccheri
| R. | Numele complet | Ref. |
|---|---|---|
| | 5-deoxi-5- (dimetilarsinoil) -2,3- O -izopropiliden-β-D-ribozid metilic | [10] |
 | 2 ', 3'-izopropilidendioxipropil 5-deoxi-5-dimetil-arsinoil-2,3- O -izopropiliden-β-D-ribozid | [11] |
| | 2 ', 3'-dihidroxipropil 5-deoxi-5-dimetilarsinoil-2,3- O -izopropiliden-β-D-ribozid | [11] |
 | 2 ', 3'-izopropilidendioxipropil 5-deoxi-5-dimetilarsinoil-2,3- O -izopropiliden-β-D-ribozid | [11] |
| R. | Numele complet | Ref. |
|---|---|---|
 | [14] [18] | |
| | dimetil (metil-2,3- O -izopropiliden-5-deoxi-β-D-ribofuranoză-5-il) arsină | [19] |
În cele din urmă, există arsenozuccheri care nu se încadrează în niciuna dintre categoriile prezentate mai sus.
| Imagine | Numele complet | Ref. |
|---|---|---|
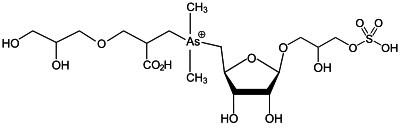 | [10] | |
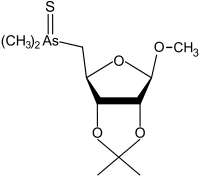 | metil-2,3- O -izopropiliden-5-deoxi-5-dimetil-tioarsinoil-β-D-ribofuranozidă | [19] |
 | 5-dimetilarsinoil-β-ribofuranoză (Francesconi în recenzia sa din 2004 [5] contestă acest nume, sugerând că compusul „ar putea fi considerat și un dihidroxi furan substituit”; acest lucru este confirmat de revizuirea Niegel din 2010, [1] care îl definește ca „derivat al arsenozuccheri” Numindu-l „dimetilarsinoilhidroxifuran”) | [20] |
Distribuție

Arsenozuccheri sunt prezenți în principal în alge (aproximativ 78% din fracțiunea de arsenic) și constituie o fracțiune semnificativă de arsenic și în moluștele marine și gastropode (aproximativ 23%); dimpotrivă, acestea sunt prezente în concentrații foarte mici în pește și orez . [2] Au fost găsite și în organismele terestre ( licheni , ciuperci , râme și unele specii de plante), dar în general cele marine conțin mai mulți dintre acești compuși decât cei terestri sau de apă dulce. [1]
Concentrația lor variază de la urme (de exemplu, toate trimetil arsonio arsenozuccheri [2] ) la µg / g; [1] în general, distribuția și concentrația lor în alge marine depinde în mare măsură de clasa taxonomică: arsenosugarul, glicerina și sulfonatul , de exemplu, au fost izolate pentru prima dată în 1981 din alga brună Ecklonia radiata . [21] în timp ce în alga brună Hizikia fusiforme , sulfatul de arsenosugar a fost determinat ca principalul compus arsenic. [8] În cele din urmă, în algele roșii ( Rhodophyta ) și algele verzi ( Chlorophyta ) cele mai prezente arseno-zaharuri sunt glicerina și fosfatul . [22]
Caracteristici fizice și chimice
Moleculele de arsenozuccheri au în general un caracter cationic și polar datorită grupului (CH 3 ) 2 As = O și din acest motiv sunt solubile în apă (cu excepția derivatului palmitoil al fosfatului de arsenozucchero [13] ). [1] Cu toate acestea, proprietățile lor acide depind aproape exclusiv de agliconă , [1] iar pentru cei 4 arsenozuccheri principali ordinea acidității este următoarea: sulfat > sulfonat > fosfat > glicerol (care nu conține o grupă acidă). [23] Acestea se caracterizează printr-o stabilitate chimică relativ scăzută (mai mică decât arsenobetaina ), iar degradarea lor are loc de preferință într-un mediu de stimulare acidă sau gastrică (probabil favorizat de activitatea enzimatică sau microbiană). [1]
Zaharul tioarseno este mai puțin polar [24] și mai puțin stabil [1] decât ossoarsenozuccheri.
Metabolism și toxicitate

Se crede că arsenozuccheri sunt sintetizați în organismele marine pornind de la arsenic anorganic (preluat din apa de mare ) prin procese de alchilare oxidativă ca mecanism de detoxifiere: [25] [26] acest lucru pare a fi adevărat doar în prezența unui arsenic scăzut conținut, în timp ce la concentrații mari se formează, de asemenea, monometilarsonat (MA) și dimetilarsinat (DMA), iar la concentrații foarte mari (100 µg Ca l −1 ) există o acumulare de arsenic toxic datorită încetării proceselor de detoxifiere. [27] De asemenea, se poate întâmpla ca o etapă intermediară între arsenic anorganic și arsenosugari să fie formarea de arsenolipide. [26] [28] În cele din urmă, când algele mor, arsenatul și DMA sunt transformate în arsenozuccheri. [29]
În ceea ce privește studiul metabolismului acestor compuși la om, principala problemă este marea variabilitate a comportamentului la diferiți indivizi. [2] [26] Studiul de toxicitate al arsenozuccheri este de mare interes pentru utilizarea alimentară ridicată a algelor, în special în țările asiatice : [30] în Japonia , de exemplu, consumul de alge poate duce la un aport de aproximativ 1 mg de arsenic pe zi [31] (algele conțin o cantitate de arsenic egală cu aproximativ 100 mg pe kg de greutate uscată [30] ), în timp ce doza zilnică tolerată de arsenic stabilită de liniile directoare ale Organizației Mondiale a Sănătății este de 0,002 mg pe kilogram greutate corporală (deci aproximativ 0,15 mg pentru o persoană de 75 kg). [32] Cu toate acestea, până în prezent nu există informații definitive cu privire la toxicitatea acestor compuși, [1] care, prin urmare, nu sunt acoperite individual de Autoritatea Europeană pentru Siguranța Alimentară . [33] S-a constatat că glicerina zahărului arsenic nu are citotoxicitate, [34] [35] în timp ce arsenosugarii cu arsenic trivalent au, în general, o activitate citotoxică mai mare decât arsenosugarii cu arsenic pentavalent, [30] dar nu a fost încă posibil să se realizeze un general concluzie asupra întregii clase de compuși. [2]
În general, nu s-au detectat cantități semnificative de arsenozuccheri în urina umană după ingestia de alge [36] sau probe sintetice ale acestor compuși, [37] prin urmare se știe că sunt metabolizate. Metaboliții identificați sunt în principal DMA, dar și MA și DMAE ( dimetilarsinoiletanol ), [36] [37] prin transformări metabolice necunoscute pornind de la dimetiloxarseno zaharuri (unele etape au fost propuse de Feldmann în 2011 [2] ), iar în acest proces pot de asemenea, verificați reducerile speciilor de arsenic trivalent sau tiolările de oxigen ale arsenogrupului. Se știe că DMA are o toxicitate mai mare decât arsenosugarul, [2] și chiar și formele reduse și tiolate sunt potențial mai toxice, deoarece sunt capabile să se lege de grupările sulfhidril de proteine și peptide . [38] Mai mult, principalii metaboliți (DMA, MA și DMAE) coincid cu cei care provin din arsenic anorganic, având astfel un efect similar; din acest motiv, arsenozuccheri sunt considerați ca fiind specii potențial toxice [2] [26] (în ciuda faptului că, după cum afirmă Francesconi, „datele limitate cu privire la toxicitatea arsenozuccheri până în prezent indică o toxicitate scăzută” [26] ).
Studiile asupra posibilelor efecte cancerigene ale acestor substanțe au fost efectuate și prin analiza urinei oilor cu o dietă bazată pe alge (animale care au un metabolism pentru acești compuși similar cu cel al oamenilor, deoarece aceiași metaboliți găsiți în urina umană au au fost identificate.): chiar dacă nu există probleme speciale de sănătate la acești indivizi, viața lor relativ scurtă (4-6 ani) nu face posibilă evaluarea riscului de cancer cauzat de arsenozuccheri. [2]
Metode de determinare
Necesitatea studierii metabolismului arsenozuccheri implică necesitatea de a avea tehnici capabile să determine acești compuși, [1] putându-i distinge de numeroasele specii de arsenic prezente în organismele marine (la concentrații foarte diferite), dintre care multe au substanțe chimice similare. și proprietăți fizice. [20]
Absența standardelor comerciale sau a materialelor de referință pentru acești compuși complică și mai mult analiza probelor. [1] [20] În mod normal, standardele sunt preparate prin extracție din probe de alge, urmate de diferite purificări cromatografice ; sinteza chimică a unor ossoarsenozuccheri este posibilă din punct de vedere tehnic, dar lungă și complexă, în timp ce tioarsenozuccheri și trimetilarsenozuccheri sunt preparați pornind de la zaharuri dimetiloxoarseno. [1]
Proba de tratament
Nu există o etapă de tratare a probelor codificată oficial (pretratare și extracție). Poate exista (deși nu este necesar) un pretratament care constă într-una din următoarele proceduri: îngheț și liofilizare; clătirea probelor solide cu apă Milli-Q, uscarea, măcinarea și omogenizarea; extragerea probelor pulverizate cu acetonă ; filtrarea și diluarea probelor de urină. [1]
Cu toate acestea, toate procedurile de tratare a probelor constau într-o extracție : [1] cea mai utilizată este extracția cu solvent, care implică utilizarea apei și a metanolului ca solvenți (puri sau în amestecuri), exploatând polaritatea acestor compuși. [5] În cazul utilizării hidroxidului de tetrametilamoniu sau hidroxidului de sodiu , sulfatul de arsenosugar este mai labil decât celelalte trei arsenosugare principale. [39] Extracția este însoțită de sonicare sau agitație mecanică și se face în general de 2 până la 5 ori. Mai puțin utilizate sunt extracția cu microunde (este o tehnică foarte agresivă și implică riscul degradării sau alterării compușilor) și extracția accelerată a solventului (care are avantajul că este semi-automată). [40] [41] Niciuna dintre aceste extracții nu este cantitativă; pentru a îmbunătăți acest aspect, au fost propuse „metode chimico-enzimatice pentru degradarea structurii celulozei algelor” de care sunt legate arsenozuccheri. [40]
În câteva cazuri, extracția este urmată de o etapă suplimentară de purificare, prin extracție în fază solidă , cromatografie off-line sau utilizarea precolonilor înainte de analiza cromatografică propriu-zisă. [1]
Analiza instrumentală
Analiza instrumentală a probelor pentru determinarea arsenozuccheri constă în cuplarea unei tehnici de separare pentru discriminarea diferitelor specii de arsen ( cromatografie lichidă ) și a unui detector cu specificitate și sensibilitate bună. [1]
În ceea ce privește separarea, nu există nicio tehnică cromatografică capabilă să separe toate speciile de arsen. [20] Din acest motiv, este o practică obișnuită să analizăm folosind diferite mecanisme cromatografice: [1]
- schimb de ioni : este cel mai răspândit (în special cel de schimb de anioni), deoarece exploatează faptul că arsenozuccheri în soluție sunt în general prezenți sub formă ionică. Ca eluant pentru schimbul de anioni (AE) dihidrogen fosfat de amoniu, se utilizează carbonat de amoniu sau bicarbonat de amoniu , în timp ce pentru schimbul de cationi (CE, utilizat practic numai pentru arsenosugar glicerol ) se utilizează formatul piridiniu . Temperatura utilizată este în jur de 30-40 ° C;
- fază inversă (RP): folosește coloane C18 și este deosebit de potrivit pentru tioarsenozuccheri. Aceasta implică utilizarea agenților de împerechere a ionilor pentru a separa speciile încărcate și neutre în aceeași perioadă; cei utilizați în mod tipic sunt ioni tetraalchilamoniu la pH neutru sau ușor acid (pentru cuplare anionică) și 1- butilsulfonat la pH 3 (pentru cuplare cationică);
- excludere dimensională (SEC): garantează o toleranță ridicată la matrice, dar nu permite identificarea univocă a arsenozuccheri; din acest motiv este utilizat în mod normal ca tehnică de purificare și fracționare sau cuplat cu spectrometrie de masă tandem ;
- multidimensional : constă în trecerea probei prin diferite etape de separare, au fost utilizate SEC-AE-CE, SEC-AE-RP sau AE-CE.
Un aspect care trebuie luat în considerare întotdeauna pentru separare este că arsenozuccheri apar adesea ca perechi de diastereoizomeri . [14]
În ceea ce privește revelația, cu toate acestea, sunt utilizate următoarele tehnici, aproape întotdeauna cuplate în conformitate cu un sistem HPLC : [1]
- spectroscopie atomică : sunt mai sensibili decât tehnicile de spectrometrie de masă și au o bună selectivitate pentru arsenic, dar necesită o separare prealabilă a compușilor, deoarece dezvăluie arsenic total și sunt incapabili să distingă diferitele specii. Cel mai utilizat este ICP-MS , capabil să garanteze performanțe excelente în ceea ce privește sensibilitatea , gama dinamică liniară , robustețea și limitele de detecție ; este, de asemenea, posibil să adăugați o etapă de generare a hidrurii . Sensibilitatea poate fi îmbunătățită în continuare prin adăugarea unor cantități mici de metanol la faza mobilă, [42] dar, în general, concentrații medii până la mari de solvenți organici [43] sau tampoane saline [44] au o compatibilitate foarte limitată cu ICP-MS. Mai mult, este necesar să verificați dacă există interferență cu clorul ( 40 Ar 35 Cl + pe semnalul 75 As + ). [43] Alte tehnici spectroscopice utilizate sunt ICP-AES , [3] spectroscopie de fluorescență atomică [45] și fluorescență atomică cu generare de hidrură precedată de foto-oxidare UV , [45] digestie fotochimică UV [46] sau oxidare termică; [47]
- spectrometrie de masă organică: oferă informații structurale despre compuși. Electrospray (ESI) este utilizat în mod normal ca tehnică de ionizare, dar s-a folosit și bombardarea rapidă a atomilor (FAB). [48] Pe de altă parte, cvadrupolul (Q), timpul analizorului de zbor (TOF), capcana de ioni (IT) [49] și analizorul de rezonanță a ionului cu transformare Fourier ciclotronică sunt folosiți ca analizor de masă (FT- ICR). [50] Configurațiile instrumentale în masă tandem sunt foarte frecvente, în special quadrupolul triplu, cu disociere indusă de coliziune (CID);
- RMN : este utilizat numai pentru anumite aplicații (de exemplu, caracterizare sau verificare).
Notă
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad Niegel, op. cit.
- ^ a b c d e f g h i j Feldmann, op. cit.
- ^ A b (EN) Morita, M., Shibata, Y., Speciația compușilor de arsen în viața marină prin cromatografie lichidă de înaltă performanță combinată cu spectrometrie de emisie atomică cu plasmă de argon cuplat inductiv , în Științe analitice , vol. 3, nr. 6, The Japan Society for Analytical Chemistry, 1987, pp. 575-577, DOI : 10.2116 / analsci.3.575 .
- ^ (EN) Shibata, Y., Morita, M., Speciația arsenicului prin cromatografie lichidă de înaltă performanță în fază inversă, spectrometrie de masă cu plasmă cuplată inductiv în științe analitice , vol. 5, nr. 1, The Japan Society for Analytical Chemistry, 1989, pp. 107-109, DOI : 10.2116 / analsci.5.107 .
- ^ a b c d Francesconi, op. cit.
- ^ a b c d e f g h i j k ( EN ) Nischwitz, V., Pergantis, SA, Liquat Chromatography Online with Selected Reaction Monitoring Electrospray Spectrometry Mass pentru determinarea speciilor organoarsenice în extracte brute de materiale de referință marine , în Analitică Chimie , vol. 77, nr. 17, American Chemical Society, 2005, pp. 5551-5563, DOI : 10.1021 / ac050445b .
- ^ a b c d ( EN ) McSheehy, S., Marcinek, M., Chassaigne, H., Szpunar, J., Identificarea derivaților dimetilarsinoil-ribozidici în alge marine prin spectrometrie de masă în tandem electrospray asistat pneumatic , în Analytica Chimica Acta , vol. . 410, n. 1-2, Elsevier, 2000, pp. 71-84, DOI : 10.1016 / S0003-2670 (00) 00706-6 .
- ^ a b ( EN ) Edmonds, JS, Morita, M., Shibata, Y. ,, Izolarea și identificarea ribofuranozidelor care conțin arsen și arsenic anorganic din algele japoneze comestibile Hizikia fusiforme , în Journal of the Chemical Society, Perkin Transactions 1 , n. 0, RSC, 1987, pp. 577-580, DOI : 10.1039 / P19870000577 .
- ^ a b c d ( EN ) McSheehy, S., Szpunar, J., Lobinski, R., Haldys, V., Tortajada, J., Edmonds, JS, Characterization of Arsenic Species in Kidney of the Clam Tridacna derasa by Multidimensional Liquid Chromatography-ICPMS și Electrospray Time-of-Flight Tandem Mass Spectrometry , în Analytica Chimica Acta , vol. 74, nr. 10, RSC, 2002, pp. 2370-2378, DOI : 10.1021 / ac011136y .
- ^ a b c d e f ( EN ) Francesconi, KA, Edmonds, JS, Stick, RV, Skelton, BW, White, AH, Ribozide care conțin arsen din alga brună Sargassum lacerifolium : structură moleculară cu raze X a 2-amino Acidul -3- [5'-deoxi-5 '- (dimetilarsinoil) -ribosiloxi] propan-1-sulfonic , în Journal of the Chemical Society, Perkin Transactions 1 , n. 11, RSC, 1991, pp. 2707-2716, DOI : 10.1039 / P19910002707 .
- ^ a b c d e f ( EN ) Francesconi, KA, Edmonds, JS, Stick, RV, Compuși arsenici din rinichiul scoicii gigantice Tridacna maxima : izolarea și identificarea unui nucleozid care conține arsenic , în Journal of the Chemical Society , Tranzacțiile Perkin 1 , nr. 11, RSC, 1992, pp. 1349-1357, DOI : 10.1039 / P19920001349 .
- ^ a b c ( EN ) Nischwitz, V., Pergantis, SA, Cartarea speciilor de arsenic și identificarea unui nou arsenosugar în scoici gigantice Tridacna maxima și Tridacna derasa folosind tehnici spectrometrice de masă avansate , în Chimia mediului , vol. 4, nr. 3, CSIRO, 2007, pp. 187-196, DOI : 10.1071 / EN07009 .
- ^ a b c ( EN ) Morita, M., Shibata, Y., Isolation and identification of arseno-lipid from a brown alga, Undaria pinnatifida (Wakame) , in Chemosphere , vol. 17, n. 6, Elsevier, 1988, pp. 1147–1152, DOI : 10.1016 / 0045-6535 (88) 90180-4 .
- ^ a b c ( EN ) Edmonds, JS, Francesconi, KA, Stick, RV, Compuși de arsen din organisme marine , în Natural Product Reports , vol. 10, nr. 4, RSC, 1993, pp. 421-428, DOI : 10.1039 / NP9931000421 .
- ^ a b ( EN ) Kahn, M., Raml, R., Schmeisser, E., Vallant, B., Francesconi, KA, Goessler, W., Two Thio-Arsenosugars in Scallops Identified with HPLC - ICPMS and HPLC– ESMS , în chimia mediului , vol. 2, nr. 3, CSIRO, 1993, pp. 171-176, DOI : 10.1071 / EN05045 .
- ^ (EN) Francesconi, KA, Goessler, W., Panutrakul, S., Irgolic, KJ, Un roman arsenic conținând ribozid (arsenosugar) în trei specii de gastropod , în Știința mediului total , vol. 221, n. 2-3, Elsevier, 1998, pp. 139-148, DOI : 10.1016 / S0048-9697 (98) 00272-1 .
- ^ (EN) McSheehy, S., Pohl, P., Velez, D., Szpunar, J., Cromatografie lichidă multidimensională cu spectrometrie de masă plasmatică cuplată inductiv paralel și detectare electrospray MS / MS ca instrument pentru caracterizarea speciilor de arsen în alge , în chimia analitică și bioanalitică , vol. 372, nr. 3, Springer, 2002, pp. 457-466, DOI : 10.1007 / s00216-001-1182-x .
- ^ (EN) Mcadam, DP, Perera, AMA, Stick, RV, Sinteza de (R) -2 ', 3'-Dihidroxipropil 5-Deoxi-5-Dimetilarsinil-β-D-Ribozidă, care conține arsenic natural Carbohidrat , în Australian Journal of Chemistry , vol. 40, nr. 11, CSIRO, 1987, pp. 1901-1908, DOI : 10.1071 / CH9871901 .
- ^ a b ( EN ) Gyepes, A., Schäffer, R., Bajor, G., Woller, Á., Fodor, P., Sinteza și studiul cromatografic al metil-2,3- O -izopropiliden-5-dimetil- arsinoil-β-D-ribofuranozidă și metil-2,3- O -izopropiliden-5-deoxi-5-dimetil-tioarsinoil-β-D-ribofuranozidă , în poliedru , vol. 27, n. 12, Elsevier, 2008, pp. 2655-2661, DOI : 10.1016 / j.poly.2008.04.049 .
- ^ a b c d ( EN ) McSheehy, S., Pohl, P., Lobinski, R., Szpunar, J., Investigarea speciației arsenicului în materialul de referință pentru testarea stridiilor prin HPLC-ICP-MS multidimensională și spectrometrie de masă electrospray tandem ( ES-MS-MS) , în The Analyst , vol. 126, nr. 7, RSC, 2001, pp. 1055-1062, DOI : 10.1039 / b102225n .
- ^ (EN) Edmonds, JS, Francesconi, KA, Arseno-zaharuri din alge brun (Ecklonia radiata) ca intermediari în ciclul arsenicului într-un ecosistem marin , în Nature , vol. 289, nr. 5798, Nature Publishing Group, 1981, pp. 602-604, DOI : 10.1038 / 289602a0 .
- ^ (EN) Francesconi, KA, Edmonds, JS, Arsenic și organisme marine , în Progrese în chimie anorganică , vol. 44, Elsevier, 1996, pp. 147-189, DOI : 10.1016 / S0898-8838 (08) 60130-0 .
- ^ (EN) Madsen, CEO, Goessler, W., Pedersen, SN, Francesconi, KA, Caracterizarea unui extract de algă prin HPLC-ICP-MS și LC-electrospray MS pentru utilizare în studiile de speciație a arsenosugarului în Journal of Analytical Atomic Spectrometry , vol. 15, nr. 6, RSC, 2000, pp. 657-662, DOI : 10.1039 / B001418O .
- ^ ( EN ) Raml, R., Francesconi, KA, Goessler, W., Improved chromatographic separation of thio-arsenic compounds by reversed-phase high performance liquid chromatography-inductively coupled plasma mass spectrometry , in Journal of Chromatography A , vol. 1128, n. 1-2, Elsevier, 2006, pp. 164–170, DOI : 10.1016/j.chroma.2006.06.061 .
- ^ ( EN ) Edmonds, JS, Francesconi, KA, Arsenic-containing ribofuranosides: isolation from brown kelp Ecklonia radiata and nuclear magnetic resonance spectra , in Journal of the Chemical Society, Perkin Transactions 1 , n. 0, RSC, 1983, pp. 2375-2382, DOI : 10.1039/P19830002375 .
- ^ a b c d e ( EN ) Francesconi, KA, Arsenic species in seafood: Origin and human health implications , in Pure and Applied Chemistry , vol. 82, n. 2, IUPAC, 2010, pp. 373–381, DOI : 10.1351/PAC-CON-09-07-01 .
- ^ ( EN ) Geiszinger, A., Goessler, W., Pedersen, SN, Francesconi, KA, Arsenic biotransformation by the brown macroalga Fucus serratus , in Environmental Toxicology and Chemistry , vol. 20, n. 10, Wiley, 2001, pp. 2255-2262, DOI : 10.1002/etc.5620201018 .
- ^ ( EN ) Cooney, RV, Mumma, RO, Benson., AA, Arsoniumphospholipid in algae , in PNAS , vol. 75, n. 9, United States National Academy of Sciences, 1978, pp. 4262-4264, DOI : 10.1073/pnas.75.9.4262 .
- ^ ( EN ) Navratilova, J., Raber, G., Fisher, SJ, Francesconi, KA, Arsenic cycling in marine systems: degradation of arsenosugars to arsenate in decomposing algae, and preliminary evidence for the formation of recalcitrant arsenic , in Environmental Chemistry , vol. 8, n. 1, CSIRO, 2011, pp. 44–51, DOI : 10.1071/EN10107 .
- ^ a b c ( EN ) Andrewes, A., DeMarini, DM, Funasaka, K., Wallace, K., Lai, VWM, Sun, H., Cullen, WR, Kitchin, KT, Do Arsenosugars Pose a Risk to Human Health? The Comparative Toxicities of a Trivalent and Pentavalent Arsenosugar , in Environmental Science & Technology , vol. 38, n. 15, American Chemical Society, 2004, pp. 4140–4148, DOI : 10.1021/es035440f .
- ^ ( EN ) Shimbo, S., Hayase, A., Murakami, M., Hatai, I., Higashikawa, K., Moon, CS, Zhang, ZW, Watanabe, T., Iguchi, H., Ikeda, M., Use of a food composition database to estimate daily dietary intake of nutrient or trace elements in Japan, with reference to its limitation , in Food Additives and Contaminants , vol. 13, n. 7, Taylor & Francis, 1996, pp. 775-786, DOI : 10.1080/02652039609374465 .
- ^ WHO , Evaluation of certain food additives and contaminants (Thirty-third report of the Joint FAO/WHO Expert Committee on Food Additives) ( PDF ), in WHO Technical Report Series , vol. 776, Ginevra, EFSA, 1989.
- ^ Gruppo di esperti scientifici dell'EFSA sui contaminanti nella catena alimentare (CONTAM), Parere scientifico sull'arsenico negli alimenti ( PDF ), in EFSA Journal , vol. 7, n. 10, EFSA, 1996, p. 1351, DOI : 10.2903/j.efsa.2009.1351 .
- ^ ( EN ) Oya-Ohta, Y., Kaise, T., Ochi, T., Induction of chromosomal aberrations in cultured human fibroblasts by inorganic and organic arsenic compounds and the different roles of glutathione in such induction , in Mutation Research/Fundamental and Molecular Mechanisms of Mutagenesis , vol. 357, n. 1-2, Elsevier, 1996, pp. 123–129, DOI : 10.1016/0027-5107(96)00092-9 .
- ^ ( EN ) Sakurai, T., Review: Biological effects of organic arsenic compounds in seafood , in Applied Organometallic Chemistry , vol. 16, n. 8, Wiley, 2002, pp. 401–405, DOI : 10.1002/aoc.325 .
- ^ a b ( EN ) van Hulle, M., Zhang, C., Schotte, B., Mees, L., Vanhaecke, F., Vanholder, R., Zhang, XR, Cornelis, R., Identification of some arsenic species in human urine and blood after ingestion of Chinese seaweed Laminaria , in Journal of Analytical Atomic Spectrometry , vol. 19, n. 1, RSC, 2004, pp. 58-64, DOI : 10.1039/B307457A .
- ^ a b ( EN ) Francesconi, KA, Tanggaard, R., McKenzie, CJ, Goessler, W., Arsenic Metabolites in Human Urine after Ingestion of an Arsenosugar , in Clinical Chemistry , vol. 48, n. 1, American Association for Clinical Chemistry, 2002, pp. 92–101.
- ^ ( EN ) Raab, A., Wright, S., Jaspars, M., Meharg, A., Feldmann, J., Pentavalent Arsenic Can Bind to Biomolecules , in Angewandte Chemie International Edition , vol. 46, n. 15, Wiley, 2007, pp. 2594–2597, DOI : 10.1002/anie.200604805 .
- ^ ( EN ) Gamble, BM, Gallagher, PA, Shoemaker, JA, Parks, AN, Freeman, DM, Schwegel, CA, Creed, JT, An investigation of the chemical stability of arsenosugars in basic environments using IC-ICP-MS and IC-ESI-MS/MS , in The Analyst , vol. 128, n. 12, RSC, 2003, pp. 1458–1461, DOI : 10.1039/B306931A .
- ^ a b ( EN ) Gallagher, PA, Shoemaker, JA, Wei, SX, Brockhoff-Schwegel, CA, Creed, JT, Extraction and detection of arsenicals in seaweed via accelerated solvent extraction with ion chromatographic separation and ICP-MS detection , in Fresenius' Journal of Analytical Chemistry , vol. 369, n. 1, Springer, 2001, pp. 71-80, DOI : 10.1007/s002160000585 .
- ^ ( EN ) Gallagher, PA, Wei, X., Shoemaker, JA, Brockhoff, CA, Creed, JT, Detection of arsenosugars from kelp extracts via IC-electrospray ionization-MS-MS and IC membrane hydride generation ICP-MS , in Journal of Analytical Atomic Spectrometry , vol. 14, n. 12, RSC, 1999, pp. 1829-1834, DOI : 10.1039/A906249A .
- ^ ( EN ) Allain, P., Jaunault, L., Mauras, Y., Mermet, JM, Delaporte, T., Signal enhancement due to the presence of carbon-containing compounds in inductively coupled plasma mass-spectrometry , in Analytical Chemistry , vol. 63, n. 14, American Chemical Society, 1991, pp. 1497-1498, DOI : 10.1021/ac00014a028 .
- ^ a b ( EN ) McSheehy, S., Szpunar, J., Morabito, R., Quevauviller, P., The speciation of arsenic in biological tissues and the certification of reference materials for quality control , in Trends in Analytical Chemistry , vol. 22, n. 4, Elsevier, 2003, pp. 2370-2378, DOI : 10.1016/S0165-9936(03)00404-7 .
- ^ ( EN ) B'Hymer, C., Caruso, JA, Arsenic and its speciation analysis using high-performance liquid chromatography and inductively coupled plasma mass spectrometry , in Journal of Chromatography A , vol. 1045, n. 1-2, Elsevier, 2004, pp. 1–13, DOI : 10.1016/j.chroma.2004.06.016 .
- ^ a b ( EN ) Sánchez-Rodas, D., Geiszinger, A.; Gómez-Ariza, JL; Francesconi, KA, Determination of an arsenosugar in oyster extracts by liquid chromatography-electrospray mass spectrometry and liquid chromatography-ultraviolet photo-oxidation-hydride generation atomic fluorescence spectrometry , in The Analyst , vol. 127, n. 1, RSC, 2002, pp. 60-65, DOI : 10.1039/B107527F .
- ^ ( EN ) Šlejkovec, Z., van Elteren, JT, Woroniecka, UD, Underestimation of the total arsenic concentration by hydride generation techniques as a consequence of the incomplete mineralization of arsenobetaine in acid digestion procedures , in Analytica Chimica Acta , vol. 443, n. 2, Elsevier, 2001, pp. 277–282, DOI : 10.1016/S0003-2670(01)01223-5 .
- ^ ( EN ) Almela, C., Laparra, JM, Vélez, D., Barberá, R., Farré, R., Montoro, R., Arsenosugars in Raw and Cooked Edible Seaweed: Characterization and Bioaccessibility , in Journal of Agricultural and Food Chemistry , vol. 53, n. 18, American Chemical Society, 2005, pp. 7344–7351, DOI : 10.1021/jf050503u .
- ^ ( EN ) Pergantis, SA, Francesconi, KA, Goessler, W., Thomas-Oates, JE, Characterization of Arsenosugars of Biological Origin Using Fast Atom Bombardment Tandem Mass Spectrometry , in Analytical Chemistry , vol. 69, n. 23, American Chemical Society, 1997, pp. 4931–4937, DOI : 10.1021/ac9704422 .
- ^ ( EN ) Miguens-Rodriguez, M., Pickford, R., Thomas-Oates, JE, Pergantis, SA, Arsenosugar identification in seaweed extracts using high-performance liquid chromatography/electrospray ion trap mass spectrometry , in Rapid Communications in Mass Spectrometry , vol. 16, n. 5, Wiley, 2002, pp. 323–331, DOI : 10.1002/rcm.578 .
- ^ ( EN ) Pickford, R., Miguens-Rodriguez, M., Afzaal, S., Speir, P., Pergantis, SA, Thomas-Oates, JE, Application of the high mass accuracy capabilities of FT-ICR-MS and Q-ToF-MS to the characterisation of arsenic compounds in complex biological matrices , in Journal of Analytical Atomic Spectrometry , vol. 17, n. 3, RSC, 2002, pp. 173-176, DOI : 10.1039/B109842J .
Bibliografia
- ( EN ) Feldmann, J., Krupp, EM, Critical review or scientific opinion paper: Arsenosugars — a class of benign arsenic species or justification for developing partly speciated arsenic fractionation in foodstuffs? , in Analytical and Bioanalytical Chemistry , vol. 399, n. 5, Springer, 2011, pp. 1735–1741, DOI : 10.1007/s00216-010-4303-6 .
- ( EN ) Francesconi, KA, Kuehnelt, D., Determination of arsenic species: A critical review of methods and applications, 2000–2003 , in The Analyst , vol. 129, n. 5, RSC, 2004, pp. 373-395, DOI : 10.1039/B401321M .
- ( EN ) Niegel, C., Matysik, F.-M., Analytical methods for the determination of arsenosugars — A review of recent trends and developments , in Analytica Chimica Acta , vol. 657, n. 2, Elsevier, 2010, pp. 83-99, DOI : 10.1016/j.aca.2009.10.041 .
Voci correlate
Altri progetti
-
 Wikimedia Commons contiene immagini o altri file sugli arsenozuccheri
Wikimedia Commons contiene immagini o altri file sugli arsenozuccheri
Collegamenti esterni
- Arsenosugars sul sito dell'EVISA