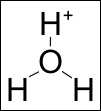
Hidroniu
| Ion hidroniu | |||
|---|---|---|---|
| Numele IUPAC | |||
| Ossonio | |||
| Caracteristici generale | |||
| Formula moleculară sau brută | H 3 O⁺ | ||
| Masa moleculară ( u ) | 19,02 g / mol | ||
| numar CAS | |||
| PubChem | 123332 | ||
| ZÂMBETE | [OH3+] | ||
| Informații de siguranță | |||
Ioniul de hidroniu este termenul învechit [1] folosit în trecut pentru a indica cationul de oxoniu, spus și fără echivoc hidroxoniu (hidroniu sau necorespunzător sau pur și simplu proton), cu formula brută reală H 3 O +, deoarece oxigenul formează trei legături covalente egale lungime și de unghiuri de 108 °, în timp ce al patrulea orbital hibrid sp 3 este umplut de o pereche electronică liberă sau cuplată [2] . Acest lucru face ca hidroxoniul cationic să fie un acid tipic Brønsted-Lowry .
Cationul este responsabil pentru caracterul acid al tuturor substanțelor dintr-un mediu apos și efectul său de nivelare . Acesta constă dintr - un cation derivat direct din formarea unei legături covalente între un ion H + (denumit idrone , care în soluție apoasă nu pot exista în stare liberă) și o moleculă de H2O . Este localizat în conformitate cu teoria disocierii lui Brønsted-Lowry a substanțelor amfotere și în toți acizii anorganici și organici, indiferent dacă sunt puternici sau slabi.
În concluzie, ionul hidroxoniu are o structură tetraedrică ; atomul de oxigen hibridizat sp 3 este plasat în centrul tetraedrului , cei trei atomi de hidrogen ocupă cele trei vârfuri ale bazei triunghiulare, în timp ce al patrulea orbital sp 3 este ocupat de o pereche de electroni fără legătură sau „ pereche singuratică ”, care este responsabil pentru majoritatea proprietăților fizico-chimice ale cationului în sine. Cele trei unghiuri de legătură HOH sunt de aproximativ 108 ° [3] . Marcarea experimentelor radioizotopice cu tritiu a arătat că cei trei atomi de hidrogen sunt echivalenți, adică atunci când disociază ionul oxoniu pentru a reveni la formarea apei, ionul H + schimbat nu este neapărat ceea ce a dobândit anterior. În soluție apoasă , cationul hidroxoniu stabilește legături de hidrogen solvatandosi cu alte trei molecule de apă, asumând cea mai complexă structură (și mai mult în acord cu datele experimentale) H 9 O 4 +. Mecanismul original Grotthuss realizează dinamica particulară și cinetica transferului de protoni într-o soluție apoasă.
Producerea cationilor de hidroxoniu: substanțe amfotere și acide
Cationul H 3 O + este prezent în mod natural în substanțele amfotere în soluție apoasă, cum ar fi anionul hidrogenocarbonat HCO 3 -, anionul monohidrogensulfat HSO 4 - și apa în sine (vezi apa autodissociazione ). Acesta derivă din „ echilibrul autoprotolizei , conform căruia aceste substanțe tind să piardă un proton tramutandosi în baza sa conjugată și eliberând un proton H +; aceasta nu poate exista liberă în soluție și, după cum sa menționat anterior, se leagă de apă formând un cation hidroxoniu.
Câteva exemple sunt:
Mai mult, chiar și acizii în soluție apoasă conțin ioni de hidroxoniu la concentrații diferite; din această valoare, exprimată ca [H 3 O +], atunci depinde de pH - ul substanțelor. Acizii puternici sunt ionizați (disociați) complet atunci când sunt dizolvați în apă și - deoarece toate reacțiile chimice sunt echilibrate - reacția lor de disociere este deplasată complet spre dreapta. Un exemplu este următorul:
Acizii definiți în schimb slabi dau naștere la reacții de echilibru de disociere într-o soluție apoasă cu formarea cationilor de hidroxoniu. Așa se întâmplă, de exemplu, tot „ oțetul , care este în esență o soluție apoasă diluată de acid acetic :
În cele din urmă, hidroxoniul cationic este prezent și în soluțiile de substanțe care nu au caracter acid, bazele , dar în concentrații absolut neglijabile, întrucât trebuie respectată întotdeauna valoarea produsului ionic al apei K W = [H 3 O + ] [OH -] care este egal cu 1,0 x 10 -14 M 2 la condiții standard .
Notă
- ^ Conform recomandărilor Diviziei de chimie anorganică a chimiei organice și a nomenclatorului IUPAC
- ^(RO) IUPAC Gold Book, „ioni de oxoniu”
- ^ Jian Tang și Takeshi Oka (1999). „Spectroscopie în infraroșu a H3O +: banda fundamentală v1.”. J. Mol. Spectroscopie. 196 (1): 120. Bibcode 1999JMoSp.196..120T. doi: 10.1006 / jmsp.1999.7844. PMID 10361062
Elemente conexe
Alte proiecte
-
 Wikționarul conține intrarea în dicționar „ hidroniu ”
Wikționarul conține intrarea în dicționar „ hidroniu ” -
 Wikimedia Commons conține imagini sau alte fișiere pe hydronium
Wikimedia Commons conține imagini sau alte fișiere pe hydronium
linkuri externe
- (EN) hydronium , al Enciclopediei Britannice , Encyclopædia Britannica, Inc.