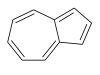
Azulene
| Azulene | |
|---|---|
| Numele IUPAC | |
| bicicleta [5.3.0] decapentaene | |
| Caracteristici generale | |
| Formula moleculară sau brută | C 10 H 8 |
| Masa moleculară ( u ) | 128,18 |
| Aspect | violet solid |
| numar CAS | |
| Numărul EINECS | 205-993-6 |
| PubChem | 9231 |
| ZÂMBETE | C1=CC=C2C=CC=C2C=C1 |
| Proprietăți fizico-chimice | |
| Solubilitate în apă | insolubil |
| Temperatură de topire | 97 ° C (370 K); sublimează |
| Temperatura de fierbere | 241 ° C (514 K); se descompune |
| Proprietăți termochimice | |
| Δ f H 0 (kJ mol −1 ) | 212.3 |
| Informații de siguranță | |
| Simboluri de pericol chimic | |
 | |
| Fraze H | 411 |
| Sfaturi P | 273 [1] |
Azulena (din spaniola azul , albastru deschis, albastru) este o hidrocarbură aromatică , izomer de naftalină . La temperatura camerei apare ca un solid cristalin de culoare intermediară între albastru-violet și negru, insolubil în apă.
Azulena este cunoscută încă din secolul al XV-lea ca un cromofor albastru obținut din distilarea cu abur a mușețelului . A fost descoperit în șarpe și pelin și a primit numele în 1863 de Septimus Piesse . Structura sa a fost raportată de Lavoslav Ružička , iar sinteza sa organică a fost realizată pentru prima dată în 1937 de către Placidius A. Plattner.
Unele terpenoide sunt prezente în natură, cum ar fi izomerii sesquiterpeni vetivazulenă (2-izopropil-4,8-dimetilazulenă) și guaiazulenă (7-izopropil-1,4-dimetilazulenă).
Structură și proprietăți
Molecula este plană și este compusă din două inele condensate, unul cu 5 atomi de carbon, celălalt cu 7. Face parte din clasa topologică a hidrocarburilor aromatice care nu alternează. [2] [3]
Atât culoarea, cât și remarcabilul moment dipolar de 1,08 D [4] de azulenă, în contrast puternic cu naftalina incoloră și apolară, se datorează structurii sale: cu transferul unei perechi de electroni din inelul cu 7 atomi în cel la 5, ambele inele sunt stabilizate deoarece sunt aromate cu 6 π electroni; acest fenomen creează un exces de sarcină negativă pe inelul cu 5 atomi și un exces de sarcină pozitivă pe inelul 7. O altă caracteristică particulară a acestui compus este încălcarea regulii Kasha, deoarece prezintă fluorescență de la un nivel de energie electronică excitat (S 2 → S 0 ) cu energie mai mare decât prima stare electronică excitată S 1 . [5]
Cu toate acestea, este un compus metastabil . Pe o perioadă lungă de timp, de ordinul anilor, tinde să se rearanjeze, transformându-se în naftalina mai stabilă. [6]
Sinteza organică
Căile sintetice pentru azulen au fost mult timp un interes de interes datorită structurii sale neobișnuite. În 1939, prima încercare a fost raportată de S. Pfau și P. Plattner [7] pornind de la inden și diazoacetat de etil .
O altă sinteză implică inelul ciclopentadienei cu sintoni nesaturați cu cinci atomi de carbon. [8] Abordarea alternativă a cicloheptatrienei este cunoscută de ceva timp, a cărei metodă ilustrativă este prezentată mai jos: [9]

Utilizări
Este utilizat în principal ca vopsea și în industria cosmetică.
În chimia organometalică , azulena acționează ca un liant pentru centrele metalice cu stare de oxidare scăzută, care sunt, de asemenea, cunoscute pentru a forma complexe atât cu liganzi ciclopentadienil, cât și cu cicloheptatrienil . Unele complexe ilustrative sunt (azulene) Mo 2 (CO) 6 și (azulene) Fe 2 (CO) 5 . [10]
Notă
- ^ Sigma Aldrich; rev. din 03.11.2011
- ^ MB Smith și J. March, CHIMIE ORGANICĂ AVANȚATĂ A lui MARCH, ediția a VI-a, WILEY-INTERSCIENCE, p. 69, ISBN 13: 978-0-471-72091-1
ISBNnevalid ( ajutor ) . - ^ Dacă, în timp ce călătoriți printr-un ciclu, este marcat un C al hidrocarburii (cu un asterisc, de exemplu), fără a marca următorul ciclu, marcând următorul și așa mai departe, la sfârșit există două adiacente semnături (asteriscuri). În alternative, acest lucru nu se întâmplă.
- ^ Arthur G. Anderson și Bernard M. Steckler, Azulene. VIII. Un studiu al spectrelor de absorbție vizibile și momentele dipolice ale unor azene 1,2 cu 1 și 1,3 substituite , în Journal of the American Chemical Society , vol. 81, nr. 18, 1 septembrie 1959, pp. 4941-4946, DOI : 10.1021 / ja01527a046 . Adus la 11 iulie 2016 .
- ^ Nicolas Tétreault, Rajeev S. Muthyala și Robert SH Liu, Control of the Photophysical Properties of Polyatomic Molecules by Substitution and Solvation: The Second Excited Singlet State of Azulene , in The Journal of Physical Chemistry A , vol. 103, nr. 15, 1 aprilie 1999, pp. 2524-2531, DOI : 10.1021 / jp984407q . Adus la 11 iulie 2016 .
- ^ Carl Salter și James B. Foresman, Naphthalene și Azulene I: Semimicro Bomb Calorimetry and Quantum Mechanical Calculations , în Journal of Chemical Education , vol. 75, nr. 10, 1 octombrie 1998, p. 1341, DOI : 10.1021 / ed075p1341 . Adus la 11 iulie 2016 .
- ^ (EN) Alexander St. Pfau și Pl. A. Plattner, Zur Kenntnis der flüchtigen Pflanzenstoffe VIII. Synthese des Vetivazulens , în Helvetica Chimica Acta , vol. 22, n. 1, 1 ianuarie 1939, pp. 202-208, DOI : 10.1002 / hlca . 19390220126 . Adus la 11 iulie 2016 .
- ^ Klaus Hafner; Klaus-Peter Meinhardt (1990). „Azulene”. Org. Synth .; Col. Vol. 7, p. 15
- ^ Approach to the Blues: A Highly Flexible Route to the Azulenes Sébastien Carret, Aurélien Blanc, Yoann Coquerel, Mikaël Berthod, Andrew E. Greene, Jean-Pierre Deprés Angewandte Chemie International Edition Volumul 44, Numărul 32, Pagini 5130–33 2005 Rezumat
- ^ (EN) Melvyn R. Churchill, Transition Metal Complexes of Azulene and Related Ligands , in Progress in Inorganic Chemistry, John Wiley & Sons, Inc., 1 ianuarie 1970, pp. 53-98, DOI : 10.1002 / 9780470166123.ch2 , ISBN 9780470166123 . Adus la 11 iulie 2016 .
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere pe azulene
Wikimedia Commons conține imagini sau alte fișiere pe azulene
| Controlul autorității | Thesaurus BNCF 29640 · GND (DE) 4143826-7 |
|---|