Electron
| Electron | |
|---|---|
| Strălucire circulară generată de fluorescență din interacțiunea unui gaz cu un fascicul de electroni deviat într-o traiectorie circulară de un câmp magnetic [1] | |
| Clasificare | Particulă elementară |
| Familie | Fermiuni |
| grup | Leptones |
| Generaţie | Inainte de |
| Interacțiuni | Gravitațional , electromagnetic , slab |
| Simbol | și - , β - |
| Antiparticulă | Pozitron ( și + ) |
| Teorizat | Richard Laming (1838-1851) G. Johnstone Stoney (1874) |
| Descoperire | JJ Thomson (1897) |
| Proprietăți fizice | |
| Masa | |
| Viața medie | Grajd |
| Incarcare electrica | -1 și - 1,602176634 × 10 −19 C [5] |
| Sarcina de culoare | Nu |
| A învârti | ½ [6] |
Electronul este o particulă subatomică încărcată negativ despre care se crede că este o particulă elementară . [7]
Împreună cu protoni și neutroni , este o componentă a atomului și, deși contribuie cu mai puțin de 0,06% la masa sa totală, își caracterizează semnificativ natura și îi determină proprietățile chimice : legătura chimică covalentă se formează în urma redistribuirii densității electronilor între doi sau mai mulți atomi. [8] . Mișcarea electronului generează un câmp magnetic , în timp ce variația energiei și accelerarea acestuia determină emisia de fotoni ; este, de asemenea, responsabil pentru conducerea curentului electric și a căldurii .
Majoritatea electronilor prezenți în univers au fost produși de Big Bang , dar pot fi generați și prin dezintegrarea beta a izotopilor radioactivi și în coliziuni cu energie mare, în timp ce pot fi anihilați prin coliziune cu pozitroni sau absorbiți într-un proces de nucleosinteza.stelar .
Apariția electronicii și dezvoltarea conexă a tehnologiei informației au făcut ca electronul să fie protagonistul dezvoltării tehnologice a secolului al XX-lea . Proprietățile sale sunt exploatate în diverse aplicații, cum ar fi tuburi cu raze catodice , microscopuri electronice , radioterapie și lasere .
Istorie
Originea termenului
„Electron” provine din cuvântul grecesc ήλεκτρον (pronunțat électron ), al cărui sens este chihlimbar . Acest nume se datorează istoric faptului că chihlimbarul a jucat un rol fundamental în descoperirea fenomenelor electrice: în special, începând cu secolul al VII-lea î.Hr. , grecii antici erau conștienți de faptul că, prin frecare unui obiect chihlimbar sau ebonit cu o cârpă de lână , obiectul în cauză a dobândit capacitatea de a atrage corpusculi ușori spre sine, cum ar fi boabele de praf. Aceste dovezi experimentale au fost preluate în secolul al XVI-lea de William Gilbert , care a identificat numeroase substanțe , inclusiv diamant și sulf , care prezentau același comportament ca și chihlimbarul. El a dat numele de „forță electrică” forței care a atras corpusculii și a numit „ electrificat ” materialele care manifestau această proprietate.
Studiile asupra electricității și magnetismului au fost continuate în timpurile moderne de Benjamin Franklin și Michael Faraday printre alții și, în această perioadă, ideea a fost avansată în contextul atomismului că electricitatea ar putea fi alcătuită și din mici corpusculi indivizibili. [9] Ideea unei cantități fundamentale de încărcare electrică a fost introdusă de filosoful Richard Laming în 1838 pentru a explica proprietățile chimice ale atomului . [10] .
În 1874, fizicianul irlandez George Stoney a introdus conceptul de „unitate de încărcare fundamentală”. [11] În 1891 el le-a estimat valoarea și a inventat termenul „ electron” pentru a se referi la astfel de „unități” [12] (din combinația termenului „ electric” și sufixul -one, care va fi de asemenea folosit mai târziu pentru a desemna alte particule subatomice, cum ar fi protonul sau neutronul [13] [14] ), scriind:
| ( RO ) „... s-a făcut o estimare a cantității reale a acestei cele mai remarcabile unități fundamentale de electricitate, pentru care de atunci m-am aventurat să sugerez numele de electron ” | ( IT ) „... s-a făcut o estimare a cantității reale a acestei foarte fundamentale unități fundamentale de electricitate, pentru care de atunci îndrăznesc să sugerez numele de electron [15] ” |
| ( George Stoney ) | |
Descoperirea

Primele dovezi experimentale ale existenței acestei particule au venit în 1860 , când fizicianul și chimistul englez Sir William Crookes a efectuat experimente cu tubul Geissler , introducând două foi metalice și conectându-le la un generator de curent continuu cu potențial ridicat (aproximativ 30 000 V ). În timpul acestui experiment, Crookes a observat că a fost generată o lumină având o culoare diferită în funcție de gazul utilizat. Această emisie de lumină provine din catod (pol negativ) și curge spre anod (pol pozitiv).
În urma experienței Crookes, și fizicianul german Johann Wilhelm Hittorf în 1869, în timp ce se dedica unui studiu privind conductivitatea electrică a gazelor, a evidențiat o strălucire emisă de catod și a verificat că a crescut în intensitate odată cu scăderea presiunii gazului. . În 1876, fizicianul german Eugen Goldstein a arătat că razele acestei străluciri aruncă o umbră și le-a numit „ raze catodice ”. [16] În anii 1870, Crookes a dezvoltat primul tub catodic cu vidul împins în interior, [17] demonstrând că razele luminescente care apar în interiorul tubului transportă energie și se deplasează de la catod la anod. Mai mult, prin aplicarea unui câmp magnetic , el a reușit să devieze razele, demonstrând că fasciculul se comportă ca și când ar fi încărcat negativ. [18] [19] În 1879, Crookes a propus ideea că aceste proprietăți ar putea fi explicate prin ceea ce el a numit „materie radiantă ” și a sugerat că trebuie să fie o nouă stare a materiei , constând din molecule încărcate negativ , care sunt expulzate la nivel ridicat. viteza de la catod. [20]
Fizicianul englez de origine germană Arthur Schuster a continuat experimentele lui Crookes plasând plăci metalice paralele cu razele catodice și aplicând un potențial electric între ele. Câmpul a deviat razele către placa încărcată pozitiv, confirmând că razele au sarcină negativă. Măsurând cantitatea de deviere pentru o anumită intensitate a curentului electric , în 1890 Schuster a fost capabil să estimeze raportul dintre masă și încărcare a componentelor de raze catodice. Cu toate acestea, această estimare a fost considerată de încredere de către contemporanii săi, deoarece s-a dovedit a fi de mii de ori mai mare decât se aștepta. [18] [21]
La sfârșitul secolului al XIX-lea, numeroși fizicieni au susținut că electricitatea era alcătuită din unități discrete, cărora li s-au dat diferite nume, dar despre care nu existau dovezi experimentale convingătoare. În 1896, fizicianul britanic JJ Thomson , împreună cu colegii săi John S. Townsend și HA Wilson , [21] au efectuat o serie de experimente care au arătat că razele catodice erau alcătuite din particule unice, mai degrabă decât unde, atomi sau molecule pe măsură ce sunt. se credea anterior. [22] Thomson a estimat cu acuratețe sarcina și masa, constatând că particulele de raze catodice, pe care le-a numit „corpusculi”, aveau probabil o masă de mii de ori mai mică decât cea a ionului hidrogen (H + ), cel mai mare ion. Lumină cunoscută în acel moment. [22] [23] Thomson a arătat cum raportul încărcare / masă ( e / m ), egal cu 5.273 × 10 17 e / g , a fost independent de materialul catodic. El a arătat, de asemenea, cum particulele încărcate negativ produse de materiale radioactive, materiale încălzite și raze catodice erau toate trasabile la aceeași entitate. [22] [24] Denumirea „electron” a fost din nou propusă pentru identificarea unor astfel de particule de către fizicianul irlandez George F. Fitzgerald și de atunci numele a fost universal acceptat. [18] În timp ce studia mineralele fluorescente în mod natural în 1896, fizicianul francez Henri Becquerel a descoperit că acestea emit radiații fără intervenția unei surse externe de energie. Aceste materiale radioactive au devenit un subiect de mare interes pentru oamenii de știință, inclusiv fizicianul din Noua Zeelandă Ernest Rutherford , care a descoperit că emit particule, pe care le-a numit particule alfa și beta , pe baza capacității lor de a pătrunde în materie. [25] În 1900, Becquerel a arătat că razele beta emise de radiu pot fi deviate de un câmp electric și că raportul lor masă-încărcare era același cu cel al razelor catodice. [26] Astfel de dovezi experimentale au sugerat că electronii existau ca componente ale atomilor. [27] [28]

Încărcarea electronică a fost măsurată cu o mai mare precizie de către fizicienii americani Robert Millikan și Harvey Fletcher în experimentul lor de picătură de ulei din 1909, ale cărui rezultate au fost publicate în 1911. În acest experiment, un câmp electric a fost folosit pentru a frâna căderea, datorită gravitației, a o picătură de ulei încărcată electric. Datorită acestui aparat instrumental, a fost posibil să se măsoare sarcina electrică produsă de câțiva ioni (între 1 și 150) cu o marjă de eroare mai mică de 0,3%. S-a obținut o valoare egală cu −1.602 × 10 −19 C și, prin urmare, a fost posibil să se estimeze că masa electronului ar trebui să dețină 9.109 × 10 −31 kg . Un experiment similar a fost realizat anterior de grupul lui Thomson, [22] folosind nori de picături de apă încărcate generate de electroliză [21] și în 1911 de Abram Ioffe , care a obținut independent același rezultat ca Millikan folosind microparticule metalice încărcate, publicând rezultatele în 1913. [29] Cu toate acestea, picăturile de ulei au fost mai stabile decât picăturile de apă datorită ratei lor de evaporare lentă și, prin urmare, mai potrivite pentru efectuarea experimentelor precise pe o perioadă lungă de vreme. [30]
Pe la începutul secolului al XX-lea, s-a descoperit că, în anumite condiții, o particulă încărcată care se mișcă cu viteză mare provoacă o condensare a vaporilor de apă suprasaturați de-a lungul drumului său. În 1911, Charles Wilson a folosit acest principiu pentru a dezvolta prima cameră de nor , un instrument care vă permite să urmăriți și să fotografiați calea urmată de particulele încărcate, cum ar fi electronii rapizi. [31]
Teoria atomică

Începând cu 1914, experimentele fizicienilor Ernest Rutherford , Henry Moseley , James Franck și Gustav Hertz au stabilit definitiv că atomul este format dintr-un nucleu masiv încărcat pozitiv înconjurat de electroni cu masă mai mică. [32] În 1913, fizicianul danez Niels Bohr a postulat că electronii se află în stări de energie cuantificată , energia determinată de impulsul unghiular al orbitelor electronilor din jurul nucleului. Teoria avansată de Bohr a prezis, de asemenea, că electronii se pot deplasa între aceste stări (sau orbite) în urma absorbției sau emisiei unei cuantice de energie, un foton cu o frecvență specifică. Această teorie a putut explica apariția liniilor de emisie spectrală ale hidrogenului ca o consecință a conținutului său de energie prin încălzire sau prin trecerea unui curent electric. În ciuda acestui fapt, modelul lui Bohr nu a reușit să prezică intensitatea liniilor aferente și să explice structura spectrului atomilor mai complecși. [32]
Formarea legăturilor chimice între atomi a fost explicată în 1916 de Gilbert Newton Lewis , care a afirmat că legătura covalentă este generată prin împărțirea unei perechi de electroni între doi atomi, [33] în timp ce o descriere completă a formării acestor perechi și legăturile chimice au fost furnizate de Walter Heitler și Fritz London în 1923 datorită mecanicii cuantice. [34] În 1919, chimistul american Irving Langmuir a refăcut modelul static al atomului Lewis, presupunând că toți electronii erau distribuiți într-o serie de cochilii sferice aproximativ concentrice, toate cu grosime egală "; [35] aceste cochilii au fost la rândul lor împărțite în celule , fiecare dintre care conținea o pereche de electroni. Folosind acest model, Langmuir a explicat calitativ proprietățile chimice ale tuturor elementelor, [34] care se repetă după o ordine precisă stabilită de tabelul periodic . [36]
În 1924, fizicianul austriac Wolfgang Pauli a observat că structura stratificată a unui atom putea fi explicată printr-un set de patru parametri care defineau în mod unic starea cuantică a unui electron și că o singură stare nu putea fi ocupată de mai mult de un singur electron. (această lege este cunoscută sub numele de principiul excluderii Pauli ). [37] În ciuda intuiției sale, Pauli nu a putut explica sensul fizic al celui de-al patrulea parametru, care ar putea presupune doar două valori. Explicația teoretică a acestui parametru se datorează fizicienilor olandezi Samuel Goudsmit și George Uhlenbeck , care au sugerat că un electron, pe lângă momentul unghiular asociat orbitei sale, poate avea propriul moment unghiular intrinsec. [32] [38] Conceptul de spin a fost astfel introdus și cu această descoperire a fost posibilă și explicarea separării liniilor spectrale observate cu un spectrograf de înaltă definiție. [39]
Mecanica cuantică și fizica modernă

În 1929, fizicianul francez Louis de Broglie a câștigat Premiul Nobel pentru fizică pentru că a descoperit că electronii, pe lângă lumină , se caracterizează și printr-o natură dublă, un corpuscular și o undă. [40] Această nouă proprietate, prezentată pentru prima dată în disertația sa din 1924 intitulată Recherches sur la théorie des quanta (Cercetarea teoriei cuantice) este cunoscută sub numele de dualism undă-particulă și implică posibilitatea observării fenomenelor de interferență între electroni în condiții adecvate:
| ( RO ) „Electronul nu mai poate fi conceput ca o singură granulă mică de electricitate; trebuie asociat cu un val și acest val nu este un mit; lungimea de undă a acestuia poate fi măsurată și interferențele sale prezise. " | ( IT ) «Electronul nu mai poate fi conceput ca un singur bob mic de energie electrică, trebuie să fie asociat cu o undă și această undă nu este mit; lungimea de undă a acestuia poate fi măsurată și interferența sa poate fi prezisă. [41] " |
| ( Louis de Broglie ) | |
Interferența este o proprietate a tuturor undelor: de exemplu, în cazul luminii, dacă o foaie cu fante paralele este interpusă între o sursă de lumină și un ecran iluminat de această sursă, lumina produsă de sursă trece prin aceste fante și este proiectată. pe ecran producând figuri bandate pe ecran. În 1927, efectele interferenței cu un fascicul de electroni au fost observate de către fizicianul englez George Paget Thomson cu o peliculă subțire de metal și de către fizicienii americani Clinton Davisson și Lester Germer , care au studiat fenomenul de împrăștiere a electronilor incident pe o placă de nichel monocristalină . [42] Niels Bohr în același an a inclus ipoteza lui de Broglie și aceste dovezi experimentale în principiul complementarității , conform căruia o descriere completă a electronului și a luminii nu se poate referi doar la natura sa de undă sau doar la particula sa de natură, ci trebuie neapărat să includă ambele. [43] De fapt, natura undelor electronului se manifestă, de exemplu, în fenomenul de interferență, în timp ce natura corpusculară determină un fascicul de electroni să întoarcă un mic vârtej poziționat de-a lungul căii sale.
Succesul prezicerii lui de Broglie a condus la publicarea ecuației Schrödinger , formulată în 1926 de Erwin Schrödinger , care descrie evoluția temporală a unei stări cuantice (și, prin urmare, a funcției sale de undă ). [44] În loc să caute o soluție care să determine poziția unui electron în timp, această ecuație a fost utilizată pentru a prezice probabilitatea de a găsi un electron într-un volum finit sau infinitesimal de spațiu. Din această abordare a luat naștere ramura fizicii numită „ mecanica cuantică ”, care a garantat posibilitatea obținerii teoretic a nivelurilor de energie ale unui electron din atomul de hidrogen în acord cu datele experimentale. [45] Odată ce spinul și interacțiunea dintre mai mulți electroni au fost luate în considerare, mecanica cuantică a reușit să reconstruiască tendința proprietăților chimice tipice ale elementelor din tabelul periodic . [46]
În 1928, pe baza lucrării lui Wolfgang Pauli, Paul Dirac a formulat un model al electronului în concordanță cu teoria specială a relativității , aplicând considerații relativiste și de simetrie formulării hamiltoniene a mecanicii cuantice pentru un electron într-un câmp electromagnetic; acest tratament a condus la formularea ecuației Dirac . [47] Pentru a rezolva problemele ecuației sale relativiste (în primul rând existența soluțiilor de energie negativă), în 1930 Dirac însuși a dezvoltat un model al vidului ca o mare infinită de particule cu energie negativă, care mai târziu a fost numită mare de Dirac . Acest lucru ne-a permis să prezicem existența pozitronului , antiparticula corespunzătoare a electronului, [48] care a fost descoperită experimental în 1932 de Carl David Anderson [49] . Anderson a propus să numească electronii negatroni și să folosească termenul de electroni pentru a indica generic una dintre variantele particulelor încărcate atât pozitiv cât și negativ. Această utilizare a termenului negatroni este încă folosită ocazional, chiar și sub forma prescurtată negatone . [50] [51]
Electronii din marea Dirac au fost introduși cu scopul de a preveni pierderea nelimitată de energie a electronilor reali observați. În acest context, fotonii (adică cuantele radiației electromagnetice) pot fi absorbiți de electronii mării, permițându-le să scape din ea. Ca rezultat net, electronii încărcați negativ și găurile încărcate pozitiv sunt generate în mare. Un gol poate fi reocupat de electronul care pierde energie, eliberând un alt foton în acest fel. [52]
În 1947, Willis Lamb , lucrând în colaborare cu studentul Robert Retherford, a descoperit că anumite stări cuantice ale electronului din atomul de hidrogen, care ar fi trebuit să aibă aceeași energie, au fost deplasate una față de cealaltă și această abatere a fost numită deplasarea lui Lamb . Cam în același timp, Polykarp Kusch , în colaborare cu Henry M. Foley , a descoperit că momentul magnetic al electronului este puțin mai mare decât a prezis ecuația Dirac. Această mică diferență a fost numită ulterior „moment magnetic anormal de dipol de electroni”. Pentru a rezolva această problemă și alte probleme, la sfârșitul anilor 1940, Sin-Itiro Tomonaga , Julian Schwinger și Richard P. Feynman au dezvoltat o teorie avansată numită electrodinamică cuantică . [53]
Acceleratoare de particule
Odată cu dezvoltarea acceleratoarelor de particule în prima jumătate a secolului XX, fizicienii au început să aprofundeze proprietățile particulelor subatomice. [54] Proprietățile particulelor elementare ale electronului au făcut din această particulă o sondă perfectă pentru explorarea structurii nucleelor atomice. Prima încercare reușită de a accelera electronii folosind inducția electromagnetică a fost făcută de Donald William Kerst în 1942: primul său betatron a atins energiile de 2.3 MeV , în timp ce următoarele au ajuns la i 300 MeV . [55] În 1947 , radiația sincrotronului cu un sincrotron de 70 MeV de la General Electric ; această radiație a fost cauzată de accelerația electronilor care, într-un câmp magnetic, ating viteze apropiate de cele ale luminii. [56]
Primul accelerator de particule de mare energie a fost ADONE , cu un fascicul de particule de energie egal cu 1,5 GeV ; această structură, operațională din 1968, [57] a accelerat electroni și pozitroni în direcții opuse, dublând practic energia produsă în coliziunile lor comparativ cu cea obținută în coliziuni de electroni cu o țintă fixă. [58] Marele colizor electroni-pozitroni (LEP) de la CERN, care a funcționat între 1989 și 2000, a realizat energii de coliziune egale cu 209 GeV și a făcut măsurători importante în ceea ce privește modelul standard . [59] [60] Large Hadron Collider (LHC), cel mai recent accelerator de la CERN, înlocuiește electronii cu hadroni , deoarece aceștia din urmă sunt mai puțin supuși pierderii de energie datorată radiației sincrotrone și, prin urmare, raportului dintre energia dobândită de particulei și energia cheltuită pentru a o obține este mai mare. [61]
Caracteristici
Electronul are o masă de repaus de 9.1093837015 (28) × 10 −31 kg , egală cu aproximativ 1 ⁄ 1836 din cea a protonului și o sarcină egală cu −1.602176634 × 10 −19 C (exact). Este cea mai ușoară particulă subatomică stabilă cunoscută dintre cele cu sarcină electrică [62] . Încărcarea electrică este încărcarea elementară schimbată în semn și rotirea are o valoare pe jumătate întregi, deci electronul este un fermion [63] . El aparține primei generații de leptoni [63] și este supus interacțiunii gravitaționale , slabe și electromagnetice . Antiparticulele sale sunt pozitronul, care diferă doar în sarcina electrică opusă.
Clasificare
În modelul standard al fizicii particulelor , electronii aparțin grupului de particule subatomice numite leptoni , despre care se crede că sunt particule elementare și au o masă mai mică decât orice altă particulă încărcată cunoscută. Electronul aparține primei generații de particule fundamentale, în timp ce a doua și a treia generație conțin alte leptoni încărcați, muonul și tau , care au sarcină și spin identice, dar o masă de repaus mai mare. Electronul și toți leptonii diferă de celelalte componente fundamentale ale materiei (care sunt quarcii , alcătuind protoni și neutroni) prin faptul că nu sunt afectați de forța puternică de interacțiune nucleară. [64]
Proprietate
Proprietăți fundamentale
Masa de repaus a unui electron este de aproximativ 9.109 × 10 −31 kg sau 5.485 × 10 −4 u care, conform principiului echivalenței masei și energiei , corespunde unei energii de repaus de 0,511 MeV , cu un raport la masa protonului de aproximativ 1 în 1836. Măsurătorile astronomice au arătat că raportul dintre masele protonului și electronul a rămas constant timp de cel puțin jumătate din vârsta universului , așa cum s-a prezis în model standard. [65]
Electronul are o sarcină electrică de −1.602 × 10 −19 C , care se numește „ sarcină elementară ” și este utilizată ca unitate standard pentru sarcina particulelor subatomice. În limitele erorii experimentale, valoarea sarcinii electronice este aceeași cu cea a protonului, dar cu semnul opus. [66] Valoarea sarcinii elementare este indicată cu simbolul e , în timp ce electronul este indicat în mod obișnuit cu simbolul e - , unde semnul minus indică faptul că această particulă are o sarcină negativă; în mod similar, pentru pozitron , care are aceeași masă ca electronul și are o sarcină opusă, este folosit ca simbol e + . [67]
Electronul nu are sub-structuri cunoscute [7] [68] și este descris ca un punct material , [63] deoarece experimentele efectuate cu capcana Penning au arătat că limita superioară pentru raza particulelor este de 10 - 22 de metri . [69] Există, de asemenea, o constantă fizică, raza clasică a electronului , care corespunde unei valori de 2,8179 × 10 −15 m ; totuși, această constantă derivă dintr-un calcul care neglijează efectele cuantice prezente. [70] [71] Se crede că electronul este stabil deoarece, deoarece particula are o sarcină unitară, decăderea sa ar încălca legea conservării sarcinii electrice . [72] Limita inferioară experimentală pentru durata de viață a electronilor este 4,6 × 10 26 ani, cu un interval de încredere de 90%. [73]
Proprietăți cuantice
În mecanica cuantică electronul poate fi tratat atât ca undă, cât și ca particulă, în conformitate cu dualismul undă-particulă . [74] În formalismul funcțiilor de undă, electronul este descris matematic de o funcție cu valori complexe , funcția de undă . Il quadrato del valore assoluto della funzione d'onda rappresenta una densità di probabilità , cioè la probabilità che l'elettrone sia osservato nell' intorno di una determinata posizione. [75] [76] Da tale distribuzione si può calcolare l' incertezza della posizione dell'elettrone. Un calcolo analogo si può fare sulla quantità di moto dell'elettrone. Le incertezze sulla posizione e la quantità di moto sono legate dal principio di indeterminazione di Heisenberg .
Gli elettroni sono particelle identiche , ovvero non possono essere distinte l'una dall'altra per le loro proprietà fisiche intrinseche: è possibile cambiare la posizione di una coppia di elettroni interagenti senza che si verifichi un cambiamento osservabile nello stato del sistema. La funzione d'onda dei fermioni , di cui gli elettroni fanno parte, è antisimmetrica: il segno della funzione d'onda cambia quando la posizione dei due elettroni viene scambiata, [77] ma il valore assoluto non varia con il cambio di segno e il valore della probabilità resta immutato. Questo differenzia i fermioni dai bosoni , che hanno una funzione d'onda simmetrica. [75]
Il momento angolare intrinseco è caratterizzato dal numero quantico di spin , pari a 1/2 in unità di ħ , [67] e l'autovalore dell'operatore di spin è √3⁄2 ħ. [78] Il risultato di una misura della proiezione dello spin su ognuno degli assi di riferimento può inoltre valere soltanto ±ħ⁄2. [79] Oltre allo spin, l'elettrone ha un momento magnetico intrinseco, allineato al suo spin, che ha un valore approssimativamente simile al magnetone di Bohr , [80] [81] che è una costante fisica che vale 9,27400949(80) × 10 −24 J / T . La proiezione del vettore di spin lungo la direzione della quantità di moto definisce la proprietà delle particelle elementari conosciuta come elicità . [82]
L'evoluzione temporale della funzione d'onda di una particella è descritta dall' equazione di Schrödinger , [83] che nel caso di un sistema di elettroni interagenti mostra una probabilità nulla che una coppia di elettroni occupi lo stesso stato quantico: questo fatto è responsabile del principio di esclusione di Pauli , il quale afferma che due elettroni del sistema non possono avere i medesimi numeri quantici. Tale principio è alla base di molte proprietà dei sistemi con molti elettroni, in particolare genera la loro configurazione all'interno degli orbitali atomici . [75]
Proprietà relativistiche
Quando un elettrone si muove con velocità prossima a quella della luce è necessario ricorrere alla teoria della relatività speciale per descriverne il moto. Secondo tale teoria, la massa relativistica dell'elettrone aumenta dal punto di vista di un osservatore esterno, e di conseguenza è necessaria una forza sempre più intensa per mantenere costante l'accelerazione. In questo modo un elettrone non può mai raggiungere la velocità della luce nel vuoto c , essendo richiesta un'energia infinita. Tuttavia, se un elettrone che si muove a una velocità prossima a quella della luce entra in un mezzo dielettrico, per esempio l' acqua , in cui la velocità della luce è significativamente minore di quella dell'elettrone, l'interazione con esso può generare un fronte d'onda di luce causato dall' effetto Čerenkov . Tale effetto è simile al boom sonico , che accade quando un oggetto supera la velocità del suono .
L'effetto della relatività speciale è descritto da una quantità nota come fattore di Lorentz , definita da:
dove è la velocità della particella e l'energia cinetica associata a un elettrone che si muove con velocità è:
dove m e è la massa a riposo dell'elettrone. Per esempio, l' acceleratore lineare di Stanford (SLAC) può accelerare un elettrone a circa 51 GeV. [84] Questo fornisce un valore per vicino a 100 000, dal momento che la massa a riposo dell'elettrone è circa 0,51 MeV/c 2 . La quantità di moto relativistica è 100 000 volte la quantità di moto dell'elettrone prevista dalla meccanica classica alla stessa velocità. [85]
Dal momento che l'elettrone ha anche un comportamento ondulatorio, a una data velocità esso ha una caratteristica lunghezza d'onda di de Broglie . Questa è data da λ e = h / p dove h è la costante di Planck e p è la quantità di moto. [41] Per un elettrone con energia di 51 GeV, come quelle raggiunte dall'acceleratore SLAC, la lunghezza d'onda è di circa 2,4 × 10 −17 m , piccola a sufficienza per esplorare la scala infinitesima del nucleo atomico e dei protoni. [86]
Proprietà quantistiche relativistiche
La teoria dei campi quantistica interpreta i fenomeni di interazione fra gli elettroni e la radiazione elettromagnetica in termini di scambi di particelle generate nel vuoto dalle fluttuazioni quantistiche. Ad esempio, secondo l' elettrodinamica quantistica , gli elettroni e il campo elettromagnetico interagiscono fra loro puntualmente tramite lo scambio di fotoni e particelle virtuali aventi vita breve e non direttamente osservabili. Le fluttuazioni quantistiche creano continuamente nel vuoto coppie di particelle virtuali, fra le quali vi sono l'elettrone e il positrone, che si annichilano in breve tempo senza poter essere misurate effettivamente. [87] In base al principio di indeterminazione di Heisenberg , la variazione dell'energia necessaria a produrre la coppia di particelle e la loro vita media non si possono conoscere contemporaneamente, [88] [89] tuttavia se la vita media è estremamente breve l'incertezza riguardo all'energia è molto ampia, e il processo e la fluttuazione possono avvenire senza violare la conservazione dell'energia.
La presenza delle particelle virtuali, sebbene non direttamente osservabile, è responsabile tuttavia della differenza delle caratteristiche dell'elettrone al variare della scala di energie dei processi in cui è coinvolto. [90] Le correzioni virtuali sono all'origine di correzioni divergenti di tipo logaritmico della massa dell'elettrone rispetto al valore nominale classico. [91] La rimozione di queste divergenze, alla base della teoria della rinormalizzazione, comporta una ridefinizione del concetto di costante fisica, che viene ad assumere nel contesto quantistico un valore differente in base alla scala di osservazione. Per esempio la carica elettrica dell'elettrone non è costante ed aumenta lentamente all'aumentare dell'energia dei processi in cui è coinvolto. [92] [93] [94]
Questo importante risultato delle teorie di campo quantistiche può essere interpretato come l'effetto di schermo prodotto dalle particelle virtuali. La presenza di un elettrone isolato permette attraverso il campo elettromagnetico di creare una coppia positrone-elettrone dal vuoto; il positrone virtuale appena creato, di carica positiva, sarà attratto dall'elettrone isolato, mentre l'elettrone virtuale ne sarà respinto. Questo fenomeno produce uno schermo positivo attorno all'elettrone isolato, la cui carica a grande distanza sarà quindi considerevolmente ridotta rispetto a quella a corta distanza. Una particella carica ad alta energia sarà in grado di penetrare lo schermo e per questo motivo entra in interazione con una carica elettrica efficace più alta. [95] In base a processi analoghi, anche la massa dell'elettrone tende a crescere quando le scale di energie crescono. Questo tipo di comportamento delle costanti fisiche è caratteristico di tutte le teorie che presentano un polo di Landau , come l'elettrodinamica quantistica. [96]
La mutua interazione fra fotoni e elettroni spiega anche la piccola deviazione dal momento magnetico intrinseco dell'elettrone dal magnetone di Bohr . [80] [97] [98] I fotoni virtuali, responsabili del campo elettrico, possono permettere infatti all'elettrone di avere un moto agitato nell'intorno della sua traiettoria classica, [99] che genera l'effetto globale di un moto circolare con una precessione . Questo moto produce sia lo spin che il momento magnetico dell'elettrone. [63] [100] Negli atomi, poi, la creazione di fotoni virtuali spiega lo spostamento di Lamb osservato nelle linee spettrali e il fenomeno del decadimento spontaneo di elettrone da uno stato eccitato a uno di energia inferiore. [101] Questo tipo di polarizzazione è stata confermata sperimentalmente nel 1997 usando l'acceleratore giapponese TRISTAN. [102]
Atomi e molecole
L'elettrone è responsabile delle proprietà chimiche fondamentali degli atomi e delle molecole . L'interazione elettromagnetica fra gli elettroni è infatti all'origine dei legami fra gli atomi e della struttura macroscopica della materia, oggetto di studio della chimica e della fisica dello stato solido .
Atomi
Gli elettroni sono i costituenti fondamentali degli atomi, assieme a protoni e neutroni . Essi sono confinati nella regione in prossimità del nucleo atomico e nel caso di un atomo neutro isolato sono in numero pari al numero atomico , cioè al numero di protoni contenuti nel nucleo. Se il numero di elettroni è differente dal numero atomico, l'atomo è detto ione e possiede una carica elettrica netta.
Secondo la meccanica classica , un elettrone in moto circolare uniforme attorno al nucleo, essendo accelerato, emetterebbe radiazione elettromagnetica per effetto Larmor , perdendo progressivamente energia e impattando infine sul nucleo. Il collasso degli atomi è smentito dall'osservazione sperimentale della stabilità della materia : per questo motivo il modello atomico di Bohr è stato introdotto nel 1913 per fornire una descrizione semiclassica nella quale un elettrone può muoversi soltanto su alcune determinate orbite non-radiative caratterizzate da precisi valori dell' energia e del momento angolare . Nello sviluppo successivo della meccanica quantistica , per rappresentare lo stato degli elettroni nell'atomo, la traiettoria classica è stata sostituita dalla funzione d'onda nota con il nome di orbitale atomico .

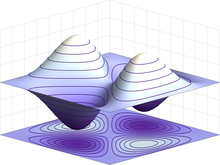
Ad ogni orbitale è associato uno degli stati energetici degli elettroni che interagiscono con il potenziale elettrico generato dal nucleo. Il valore della funzione d'onda associata a tali stati è fornito dalla soluzione dell' equazione d'onda di Schrödinger , che può essere risolta per l'atomo di idrogeno notando la simmetria radiale del potenziale elettrico indotto dal nucleo. Le soluzioni dell'equazione d'onda sono enumerate da numeri quantici che assumono un insieme discreto di valori, che rappresentano il valore di aspettazione dell'energia e del momento angolare, [103] in particolare:
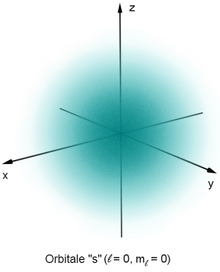
- il numero quantico principale n , che definisce il livello energetico e il numero totale di nodi della funzione d'onda radiale, considerando come nodo anche una superficie sferica a distanza infinita dal nucleo; può assumere valori interi non inferiori a 1; l'energia di un elettrone nell'atomo nei semplici modelli non relativistici dipende unicamente da questo numero;
- il numero quantico azimutale l , o numero quantico angolare , che definisce il momento angolare orbitale ; può assumere valori interi positivi compresi tra 0 ed n-1 e sulla base di questa osservabile è possibile determinare informazioni circa il numero di nodi non sferici e, indirettamente, sulla simmetria dell'orbitale;
- il numero quantico magnetico m l , che definisce la componente z del momento angolare orbitale; può assumere valori interi compresi tra + l e - l ed è responsabile della geometria degli orbitali;
- il numero quantico di spin m s , associato alla componente z dello spin dell'elettrone; può assumere solo due valori, +1/2 o -1/2 in unità di ħ.
Gli atomi con più elettroni richiedono una descrizione degli stati più complessa di quella dell' atomo di idrogeno , in quanto è necessaria l'introduzione di approssimazioni a causa dell'impossibilità di risolvere esattamente l'equazione di Schrödinger per via analitica. Le approssimazioni più utilizzate sono il metodo di Hartree-Fock , che sfrutta la possibilità di scrivere la funzione d'onda degli elettroni come un determinante di Slater , l' accoppiamento di Russell-Saunders e l' accoppiamento jj , che invece riescono ad approssimare l'effetto dovuto all' interazione spin-orbita nel caso di nuclei rispettivamente leggeri [104] e pesanti.
Per il principio di esclusione di Pauli , due o più elettroni non possono trovarsi nel medesimo stato, cioè non possono essere descritti dai medesimi numeri quantici. Questo fatto determina la distribuzione degli elettroni negli orbitali. Gli orbitali sono occupati dagli elettroni in modo crescente rispetto all'energia. Lo stato di momento angolare è definito dal numero quantico azimutale l ; dove il quadrato del valore assoluto del momento angolare è . Il numero quantico magnetico può assumere valori interi compresi tra - l e + l : il numero di tali valori è il numero delle coppie di elettroni, con valore di spin opposto, che possiedono il medesimo numero quantico azimutale. Ad ogni livello energetico corrisponde un numero crescente di possibili valori del numero quantico azimutale, a ogni valore del numero quantico azimutale corrispondono 2l + 1 valori di m l , ea ogni valore di m l corrispondono i due valori possibili di spin.
All'interno della nuvola elettronica è possibile che un elettrone effettui una transizione da un orbitale a un altro principalmente attraverso l'emissione o l'assorbimento di fotoni (cioè di quanti di energia [105] ), ma anche in seguito alla collisione con altre particelle o tramite l' effetto Auger . [106] Quando un elettrone acquista un'energia pari alla differenza di energia con uno stato non occupato all'interno degli orbitali, esso effettua una transizione in tale stato. Una delle applicazioni più importanti di tale fenomeno è l' effetto fotoelettrico , in cui l'energia fornita da un fotone è tale da separare l'elettrone dall'atomo. [107] Inoltre, dal momento che l'elettrone è carico, il suo moto attorno al nucleo, che in una descrizione semiclassica è circolare uniforme , produce unmomento di dipolo magnetico proporzionale al momento angolare orbitale. Il momento magnetico totale di un atomo è equivalente alla somma vettoriale dei momenti di dipolo magnetici e di spin di tutti i suoi elettroni e dei costituenti del nucleo. Il momento magnetico dei costituenti del nucleo è tuttavia trascurabile rispetto a quello degli elettroni. [108] L'interazione tra il momento di dipolo magnetico e il momento di spin è descritto dall' interazione spin-orbita , mentre l'interazione con un campo magnetico esterno è descritta dai limiti di Paschen-Back e Zeeman , a seconda che l'interazione spin-orbita sia rispettivamente trascurabile o meno rispetto al campo applicato.
Molecole e composti ionici
Nelle molecole gli atomi sono uniti dal legame chimico covalente , in cui uno o più elettroni sono condivisi fra due o più atomi. [109] In una molecola gli elettroni si muovono sotto l'influenza attrattiva dei nuclei e il loro stato è descritto da orbitali molecolari, più grandi e complessi di quelli di un atomo isolato, che in prima approssimazione si possono ottenere attraverso la sommatoria di più orbitali degli atomi considerati singolarmente. [110] Differenti orbitali molecolari hanno differenti distribuzioni spaziali di densità di probabilità: nel caso di una molecola costituita da due atomi, per esempio, gli elettroni che ne formano l'eventuale legame si troveranno con maggiore probabilità in una ristretta regione posta fra i due nuclei. [111]
Un composto ionico può essere definito come un composto chimico formato da ioni , aventi ciascuno una carica elettrica positiva o negativa, ma l'insieme di tali ioni ha carica elettrica complessiva neutra. Alla base dei composti ionici vi è il legame ionico , di natura elettrostatica , che si forma quando le caratteristiche chimico-fisiche dei due atomi sono nettamente differenti e vi è una notevole differenza di elettronegatività . Per convenzione si suole riconoscere un legame ionico tra due atomi quando la differenza di elettronegatività Δχ è maggiore di 1,9. Al diminuire di tale differenza cresce il carattere covalente del legame.
Interazione con le forze fondamentali
L'elettrone genera un campo elettrico che esercita una forza attrattiva su particelle con una carica positiva (come il protone) e una forza repulsiva su particelle con carica negativa. L'intensità di tale forza è determinata dalla legge di Coulomb . Un elettrone in movimento genera un campo magnetico : tale proprietà prende il nome di " induzione elettromagnetica " ed è responsabile ad esempio della generazione del campo magnetico che permette il funzionamento del motore elettrico . [112] Tramite la legge di Ampère tale movimento rispetto all'osservatore può essere messo in relazione al campo magnetico generato. In generale, i campi elettrici e magnetici prodotti da cariche o correnti elettriche sono calcolati risolvendo le equazioni di Maxwell . Il campo elettromagnetico di una particella carica in movimento è espresso tramite il potenziale di Liénard-Wiechert , anche quando la velocità della particella è prossima a quella della luce.
Quando un elettrone è in moto in corrispondenza di un campo magnetico è soggetto alla forza di Lorentz , la quale esercita una variazione della componente della velocità dell'elettrone perpendicolare al piano definito dal campo magnetico e dalla velocità iniziale dell'elettrone e la forza centripeta che viene generata costringe l'elettrone a seguire una traiettoria elicoidale . L'accelerazione che deriva da questo moto curvilineo, nel caso di velocità relativistiche, causa una radiazione di energia da parte dell'elettrone sotto forma di radiazione di sincrotrone . [113] [114] [115] L'emissione di energia causa a sua volta un rinculo dell'elettrone, conosciuto come forza di Abraham-Lorentz-Dirac , che rallenta il moto dell'elettrone; questa forza è generata da un effetto di retroazione del campo dell'elettrone su sé stesso. [116]
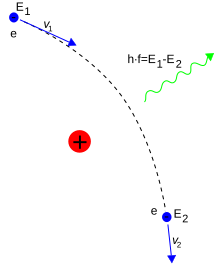
In elettrodinamica quantistica , l'interazione elettromagnetica tra le particelle è trasmessa dai fotoni : un elettrone isolato nello spazio vuoto che non subisce un'accelerazione non è in grado di emettere o di assorbire un fotone reale, poiché così facendo violerebbe le leggi di conservazione dell'energia e della quantità di moto . Invece i fotoni virtuali possono trasferire la quantità di moto tra due particelle cariche ed è questo scambio di fotoni virtuali che genera, per esempio, la forza di Coulomb. [117] L'emissione di energia può avvenire quando un elettrone viene deviato da una particella carica, come per esempio un protone; l'accelerazione dell'elettrone porta all'emissione della radiazione di bremsstrahlung , detta anche radiazione di frenamento. [118]
Una collisione anelastica tra un fotone e un elettrone libero produce l' effetto Compton : questo urto è associato a un trasferimento dell'energia e della quantità di moto tra le particelle, che porta alla variazione della lunghezza d'onda del fotone incidente. [119] Il valore massimo di questa variazione della lunghezza d'onda è h / m e c ed è noto come lunghezza d'onda Compton e per l'elettrone vale 2,43 × 10 −12 m . [120] Se la lunghezza d'onda della luce incidente è sufficientemente lunga (come ad esempio quella della luce visibile , che ha una lunghezza d'onda che va da 0,4 × 10 −6 a 0,7 × 10 −6 m ), la variazione della lunghezza d'onda dovuta all'effetto Compton diventa trascurabile e l'interazione tra radiazione e particelle può essere descritta tramite lo scattering Thomson . [121]
La forza dell'interazione elettromagnetica tra due particelle cariche è data dalla costante di struttura fine α che è una quantità adimensionale formata dal rapporto di due contributi energetici: l'energia elettrostatica di attrazione o repulsione data dalla separazione di una lunghezza d'onda Compton e dall'energia a riposo della carica. Il suo valore è 7,297353 × 10 −3 , che è possibile approssimare con la frazione 1/137. [122]
Quando elettroni e positroni collidono si annichilano l'un l'altro, originando due o più fotoni dei raggi gamma . Se invece la quantità di moto dell'elettrone e del positrone è trascurabile si può formare il positronio prima che il processo di annichilamento porti alla formazione di due o tre fotoni dei raggi gamma con un'energia totale di 1,022 MeV . [123] [124] D'altra parte i fotoni molto energetici possono trasformarsi in un elettrone e in un positrone tramite un processo chiamato produzione di coppia , ma questo avviene solo in presenza di una particella carica nelle vicinanze, come un nucleo atomico. [125] [126]
Nella teoria dell' interazione elettrodebole la componente sinistrorsa della funzione d'onda dell'elettrone forma un doppietto di isospin debole con il neutrino elettronico , cioè a causa dell'interazione elettrodebole il neutrino si comporta come un elettrone. Ciascuna componente di questo doppietto può subire l'interazione della corrente debole carica tramite l'emissione o l'assorbimento di un bosone W e può essere trasformata nell'altra componente. La carica è conservata durante questo processo poiché anche il bosone W porta una carica che annulla ogni variazione netta durante la reazione. Le interazioni della corrente debole carica sono responsabili del decadimento beta negli atomi radioattivi . Sia l'elettrone che il neutrino possono subire l'interazione della corrente debole neutra tramite uno scambio di bosoni Z e questo è responsabile dello scattering elastico tra elettrone e neutrino. [127]
Elettroni nei corpi macroscopici

Se un corpo ha un numero di elettroni maggiore o minore rispetto a quelli necessari per bilanciare la carica positiva dei nuclei, esso presenterà una carica elettrica netta: nel caso di un eccesso di elettroni, il corpo è carico negativamente, mentre nel caso di un difetto di elettroni, il corpo è carico positivamente; se invece il numero di elettroni e il numero di protoni sono uguali, le loro cariche si annullano a vicenda e il corpo è dunque elettricamente neutro. Un corpo macroscopico può sviluppare una carica elettrica ad esempio attraverso lo sfregamento, per via dell' effetto triboelettrico . [131]
Gli elettroni indipendenti che si muovono nel vuoto sono detti elettroni liberi e anche gli elettroni nei metalli hanno un comportamento simile a quelli liberi. Il flusso di carica elettrica dovuto al moto degli elettroni liberi o in un materiale è detto corrente elettrica . I materiali sono classificati in base alla resistenza che oppongono al passaggio di corrente: si dividono in conduttori , semiconduttori e isolanti (o dielettrici).
In generale, ad una data temperatura, ciascun materiale ha una conducibilità elettrica che determina il valore della corrente quando è applicato un potenziale elettrico . Esempi di buoni conduttori, cioè materiali capaci di far scorrere facilmente al proprio interno elettricità , sono i metalli come il rame e l' oro , mentre vetro e plastica sono cattivi conduttori. I metalli sono spesso anche buoni conduttori di calore. Nonostante questo, al contrario della conducibilità elettrica, la conducibilità termica è quasi indipendente dalla temperatura; ciò è espresso matematicamente dalla legge di Wiedemann-Franz , [132] la quale afferma che il rapporto fra la conduttività termica e la conduttività elettrica è proporzionale alla temperatura.
Cristalli e struttura a bande
Le proprietà di conduzione di un solido cristallino sono determinate dagli stati quantistici degli elettroni, la cosiddetta struttura elettronica a bande . Nel caso di solidi amorfi , cioè senza struttura cristallina, la descrizione è più complessa.
Nei solidi cristallini gli atomi sono disposti regolarmente in un reticolo . La simmetria di tale distribuzione spaziale permette di semplificare il calcolo degli stati energetici degli elettroni nel cristallo e ricavare la struttura a bande. Con questa descrizione è possibile approssimare il comportamento degli elettroni nei solidi con quello di elettroni liberi, ma con una diversa massa, detta massa efficace . [133] Un elettrone all'interno di un reticolo cristallino è descritto da una funzione d'onda detta funzione di Bloch , alla quale è associato un vettore detto quasi-impulso o impulso cristallino , che è l'analogo della quantità di moto per gli elettroni liberi. L'analogia con gli elettroni liberi è particolarmente adeguata per alcuni valori di impulso cristallino, per i quali si ha una relazione di dispersione quadratica, come nel caso libero. [134]
Nei solidi gli elettroni sono trattati come quasiparticelle poiché, a causa dell'interazione reciproca e con gli atomi del reticolo, assumono delle proprietà diverse da quelle degli elettroni liberi. Inoltre, nei solidi si introduce una quasiparticella, detta lacuna , che descrive la "mancanza" di un elettrone. Tale particella ha una sua massa efficace ed ha carica positiva, uguale in valore assoluto a quella dell'elettrone.
Nei materiali isolanti gli elettroni rimangono confinati in prossimità dei loro rispettivi nuclei. Al contrario, i metalli hanno una struttura elettronica a bande, alcune delle quali sono parzialmente riempite dagli elettroni. La presenza di queste bande permette agli elettroni nei metalli di muoversi come elettroni liberi o delocalizzati; essi non sono associati a uno specifico atomo e quindi, quando è applicato un campo elettrico, si muovono liberamente come un gas, chiamato gas di Fermi . [132] Un'altra categoria di materiali è quella dei semiconduttori , in cui la conducibilità può variare di molto fra i valori estremi di conduzione e isolante. [135]
A causa delle collisioni fra elettroni e atomi la velocità di deriva degli elettroni in un conduttore è dell'ordine di pochi millimetri per secondo. Ciò nonostante, la velocità di propagazione di un segnale elettrico, cioè la velocità con la quale si propaga la variazione di corrente in un conduttore, è tipicamente di circa il 75% della velocità della luce. [136] Questo accade perché i segnali elettrici si propagano come onde, con una velocità dipendente dalla costante dielettrica del materiale. [137]
Il disordine termico nel reticolo cristallino del metallo causa un aumento della resistività del materiale, producendo quindi la dipendenza dalla temperatura per la corrente elettrica. [138]
Superconduttività
Quando alcuni materiali sono raffreddati al di sotto di una certa temperatura critica , avviene una transizione di fase a causa della quale essi perdono la resistività alla corrente elettrica, in un processo noto come superconduttività . Nella teoria BCS , gli elettroni sono legati in coppie che entrano in uno stato quantistico noto come condensato di Bose-Einstein . Tali coppie, dette coppie di Cooper , si accoppiano nel loro moto per mezzo delle vibrazioni di reticolo chiamate fononi , evitando le collisioni con gli atomi che normalmente causano la resistività elettrica [139] (le coppie di Cooper hanno un raggio di circa 100 nm , quindi si possono scavalcare a vicenda). [140] La teoria BCS non descrive tutti i materiali superconduttori, e non esiste ancora un modello teorico in grado di spiegare completamente la superconduttività ad alta temperatura .
Altri effetti
Gli elettroni all'interno dei solidi conduttivi, che sono a loro volta trattati come quasi-particelle, quando sono strettamente confinati intorno a temperature vicine alle zero assoluto si comportano globalmente come due nuove differenti quasi-particelle: gli spinoni e gli oloni . [141] [142] Il primo trasporta spin e momento magnetico, mentre il secondo la carica elettrica. Gli elettroni possono, secondo la teoria di Eugene Paul Wigner , formare essi stessi una struttura cristallina, disponendosi nei punti di un reticolo. Tale stato della materia è detto cristallo di Wigner .
Formazione

Per spiegare gli istanti iniziali dell'evoluzione dell'universo è stata sviluppata la teoria del Big Bang , che è la più accettata dalla comunità scientifica. [143] Nel primo millisecondo dell'esistenza dell'universo noto, la temperatura era di circa un miliardo di kelvin ei fotoni avevano un'energia media nell'ordine del milione di elettronvolt ; questi fotoni erano sufficientemente energetici da poter reagire l'un l'altro per formare coppie di elettroni e positroni:
dove è il fotone, è il positrone e è l'elettrone. Contemporaneamente le coppie elettrone-positrone si annichilivano e producevano fotoni energetici. I due processi erano in equilibrio durante la prima fase di evoluzione dell'universo, ma dopo 15 secondi la temperatura dell'universo calò sotto la soglia di formazione delle coppie di elettroni-positroni. La maggior parte degli elettroni e positroni rimasti si annichilirono e produssero raggi gamma che in breve tempo irradiarono l'universo. [144]
Per ragioni non ancora ben comprese, durante il processo di leptogenesi vi era un numero maggiore di elettroni rispetto a quello dei positroni, [145] perciò circa un elettrone ogni miliardo sopravvisse durante il processo di annichilazione. Questo eccesso era analogo a quello dei protoni sugli antiprotoni , in una condizione nota come asimmetria barionica , perciò la carica netta presente nell'universo risultava nulla. [146] [147] I protoni ei neutroni superstiti iniziarono a interagire in un processo noto come nucleosintesi primordiale , durato fino a circa 5 minuti dopo l'istante iniziale, in cui si assistette alla formazione dei nuclei degli isotopi di idrogeno , elio e in minima parte litio . [148] I neutroni rimasti subirono il decadimento beta , con una vita media di circa quindici minuti, con la formazione di un protone, un elettrone e un antineutrino:
dove è il neutrone, è il protone e è l'antineutrino elettronico. Per i successivi 300 000-400 000 anni gli elettroni liberi erano troppo energetici per legarsi ai nuclei atomici; [149] passato questo periodo, seguì un processo di ricombinazione, in cui gli elettroni si legarono ai nuclei atomici per formare atomi elettricamente neutri ea causa di ciò l'universo divenne trasparente alla radiazione elettromagnetica. [150]
Circa un milione di anni dopo il Big Bang, si iniziò a formare la prima generazione di stelle ; [150] all'interno di queste stelle, la nucleosintesi portò alla produzione di positroni derivanti dalla fusione di nuclei atomici e queste particelle di antimateria si annichilirono immediatamente con gli elettroni formando raggi gamma. Ciò portò a una continua riduzione nel numero di elettroni ea un corrispettivo aumento di neutroni; nonostante questo il processo di evoluzione stellare portò alla sintesi di isotopi radioattivi i quali potevano decadere con un decadimento di tipo beta , emettendo in questo modo un elettrone e un antineutrino dal nucleo. [151]
Alla fine della sua vita, una stella di massa superiore di 20 volte la massa solare può subire un collasso gravitazionale e formare un buco nero ; [152] in base alle leggi della fisica classica , questo oggetto stellare massivo esercita un'attrazione gravitazione così grande da impedire a qualsiasi cosa, anche alla radiazione elettromagnetica, di potergli sfuggire una volta che è stato superato il raggio di Schwarzschild . Si pensa tuttavia che gli effetti quantistici possano permettere l'emissione di una radiazione di Hawking a tale distanza, infatti si ritiene che sull' orizzonte degli eventi di questi oggetti vengano prodotte coppie virtuali di elettroni e positroni e quando esse vengono formate in prossimità dell'orizzonte degli eventi, la distribuzione spaziale casuale di queste particelle può permettere a una particella della coppia di apparire all'esterno dell'orizzonte grazie all' effetto tunnel . Il potenziale gravitazionale del buco nero può fornire l'energia sufficiente per trasformare la particella virtuale in una particella reale, facendo in modo da diffonderla nello spazio, [153] mentre all'altra particella della coppia è stata fornita energia negativa e ciò comporta una perdita netta di energia del buco nero. La velocità della radiazione di Hawking cresce con il diminuire della massa e questo comporta l'evaporazione del buco nero che alla fine esplode. [154]
Un altro modo di formazione degli elettroni è dato dall'interazione dei raggi cosmici con gli strati alti dell'atmosfera: i raggi cosmici sono particelle che viaggiano nello spazio con energie anche dell'ordine dei 3 × 10 20 eV [155] e, quando esse collidono con le particelle presenti nell'alta atmosfera terrestre , vi è la produzione di una cascata di particelle, tra le quali pioni e muoni , [156] con questi ultimi che sono i responsabili di più della metà della radiazione cosmica osservata a Terra. Il decadimento del pione porta alla formazione dei muoni tramite il seguente processo:
mentre a suo volta il muone può decadere formando elettroni:
Osservazioni sperimentali

Le prime osservazioni degli elettroni come particella, hanno sfruttato fenomeni elettrostatici o la produzione di raggi catodici . Oggi si eseguono esperimenti in laboratorio in cui vengono osservati elettroni sia per lo studio delle proprietà di queste particelle, sia per studiare le proprietà di corpi macroscopici.
In condizioni di laboratorio, l'interazione di elettroni individuali possono essere osservate con l'uso di rilevatori di particelle , che permettono misure precise di specifiche proprietà come energia, spin e carica elettrica [158] . Lo sviluppo della trappola ionica quadrupolare ha permesso di contenere particelle in piccole regioni dello spazio per lunghi periodi. Questo ha permesso la misura precisa delle proprietà particellari. Per esempio in una misurazione si è riusciti a contenere un singolo elettrone per un periodo di dieci mesi. [159] Il momento magnetico di un elettrone fu misurato con una precisione di 11 cifre significative, che, nel 1980, è la misura migliore di una costante fisica. [160]
La prima immagine video della distribuzione di energia di un elettrone è stata catturata da un team dell'università di Lund in Svezia, nel febbraio 2008. Gli scienziati hanno usato flash estremamente piccoli di luce, che hanno permesso di osservare il moto di un elettrone per la prima volta. [161] [162]
Tramite la misura dell'energia irradiata da elettroni, gran parte delle misure spettroscopiche sono collegati allo studio degli elettroni liberi o legati, misurando l'energia dei fotoni emessi.
Per esempio, nell'ambiente ad alta energia come la corona di una stella, gli elettroni liberi formano un plasma che emette energia per gli effetti di Bremsstrahlung . Il gas elettronico può formare delle oscillazioni di plasma, ovvero oscillazioni regolari della densità degli elettroni, e queste possono produrre emissioni di energia che possono essere rilevate usando i radiotelescopi . [163]
Nel caso di atomi e molecole, un elettrone confinato a muoversi attorno a un nucleo può transire fra i diversi livelli energetici di questo consentiti, assorbendo o emettendo fotoni di frequenza caratteristica. Per esempio, quando un atomo è irraggiato da una sorgente con uno spettro continuo, appariranno delle distinte linee spettrali per la radiazione trasmessa. Ciascun elemento o molecola esibisce un insieme caratteristico proprio di serie di linee spettrali, che lo distinguono dagli altri atomi, come per esempio il noto caso delle serie dello spettro dell'atomo di idrogeno . Lo studio dell'intensità e la larghezza di queste linee permette di indagare le proprietà fisico-chimiche delle sostanze in analisi. [164] [165]
La distribuzione di elettroni nei materiali solidi può essere visualizzata dallo spettroscopio ARPES ( Angle resolved photoemission spectroscopy , ovvero spettroscopia fotoelettrica angolarmente risolta). Questa tecnica si basa sull' effetto fotoelettrico per misurare il reticolo reciproco , una rappresentazione matematica della struttura periodica di un cristallo. ARPES può essere usato per determinare la direzione, la velocità e la diffusione di elettroni nel materiale. [166]
Applicazioni

I fasci di elettroni sono usati nella saldatura di materiali, [168] permettendo di raggiungere densità di energia superiori ai 10 7 W·cm −2 nello stretto diametro focale di 0,1-1,3 mm e spesso non richiedono un materiale di riempimento. Questa tecnica di saldatura deve essere eseguita nel vuoto, in modo tale che gli elettroni non interagiscano con l'aria prima di raggiungere il bersaglio e può essere usata per unire materiali conduttori che altrimenti sarebbero difficili da saldare. [169] [170]
La litografia a fasci di elettroni (EBL) è un metodo per stampare i semiconduttori a risoluzioni più basse del micron . [171] Questa tecnica è limitata dagli alti costi, basse performance, dalla necessità di operare con fascio nel vuoto e dalla tendenza degli elettroni a essere diffusi nei solidi. L'ultimo problema limita la risoluzione a circa 10 nm . Per questa ragione, l'EBL è principalmente usata per la produzione di un piccolo numero di circuiti integrati specializzati. [172]
La lavorazione con fasci di elettroni è usata per irradiare i materiali in modo da cambiare le loro proprietà fisiche o per la sterilizzazione medica e la produzione di cibo. [173] Nella radioterapia , i fasci di elettroni generati da acceleratori lineari sono usati per il trattamento di tumori superficiali: dato che un fascio di elettroni può penetrare solamente uno spessore limitato prima di essere assorbito, tipicamente intorno a 5 cm per elettroni di energia nel range 5– 20 MeV , la radioterapia è utile per il trattamento di lesioni della cute come il carcinoma basocellulare . Un fascio di elettroni può essere usato per integrare il trattamento di aree che sono state irraggiate da raggi X . [174] [175]
Gli acceleratori di particelle usano campi elettrici per far raggiungere agli elettroni e alle loro antiparticelle alte energie. Nel momento in cui queste particelle passano in una regione in cui c'è campo magnetico, questi emettono radiazione di sincrotrone . L'intensità di questa radiazione dipende dallo spin e questo può permettere la polarizzazione dei fasci di elettroni in un processo noto come effetto Sokolov-Ternov . [176] La polarizzazione di fasci di elettroni può essere molto utile per numerosi esperimenti. La radiazione di sincrotrone può anche essere usata per raffreddare il fascio di elettroni, in modo da ridurre la quantità di moto persa dalle particelle. Una volta che le particelle sono state accelerate sino alla energia richiesta, i fasci separati di elettroni e positroni sono portati alla collisione e la risultante emissione di radiazione è osservata dai rivelatori di particelle ed è studiata dalla fisica particellare. [177]
Produzione di immagini

Gli elettroni possono essere utilizzati anche per ottenere immagini microscopiche grazie ai microscopi elettronici , che indirizzano un fascio focalizzato direttamente sul campione. A causa dell'interazione del fascio con il materiale, alcuni elettroni cambiano le loro proprietà, come una variazione della direzione, della fase relativa e dell'energia. Registrando questi cambiamenti del fascio elettronico, si possono produrre immagini a risoluzione atomica del materiale. [178] Questa elevata risoluzione, maggiore dei microscopi ottici (che è di circa 200 nm in luce blu), è possibile poiché i microscopi elettronici sono limitati dalla lunghezza d'onda di De Broglie degli elettroni (a titolo d'esempio, un elettrone ha una lunghezza d'onda di 0,0037 nm quando questo viene accelerato da un potenziale di 100 kV ). [179] [180] Il microscopio elettronico a trasmissione corretto in aberrazione è in grado di avere una risoluzione inferiore a 0,05 nm , che è sufficiente per risolvere i singoli atomi. [181] Queste caratteristiche tecniche rendono il microscopio elettronico uno strumento di laboratorio utile per le immagini ad alta risoluzione; a fronte di questi vantaggi, i microscopi elettronici sono strumenti molto costosi da mantenere.
Vi sono due tipi di microscopi elettronici: a trasmissione e a scansione . Il primo funziona in maniera analoga a una lavagna luminosa, ovvero il fascio di elettroni passa attraverso una parte del campione e viene successivamente proiettato tramite lenti su diapositive o su un CCD . Nel secondo invece l'immagine è prodotta con un fascio elettronico molto fine che scansione riga per riga una piccola regione del campione; l' ingrandimento varia da 100× a 1 000 000× o più per entrambi i microscopi. Un altro tipo di microscopio elettronico è quello a effetto tunnel sfrutta l' effetto tunnel quantistico degli elettroni che fluiscono da una punta conduttrice appuntita al materiale di interesse e può riprodurre immagini a risoluzione atomica delle superfici. [182] [183] [184]
Altre tecniche permettono di studiare la struttura cristallina dei solidi; una tecnica che sfrutta questo principio è la low energy electron diffraction (LEED) che permette di visualizzare su uno schermo fluorescente la figura di diffrazione di un cristallo utilizzando un fascio collimato di elettroni avente un'energia tra i 20 ei 200 eV . [185] Un altro metodo che sfrutta la diffrazione è la reflection high-energy electron diffraction (RHEED) che sfrutta la riflessione di un fascio di elettroni incidente a piccoli angoli in modo da caratterizzare la superficie del materiale di studio; l'energia tipica del fascio è tra 8 e 20 keV , mentre l'angolo di incidenza varia tra 1° e 4°. [186] [187]
Altre applicazioni
Nel laser a elettroni liberi , un fascio di elettroni a energia relativistica passa attraverso una coppia di ondulatori che contengono una serie di dipoli magnetici, i cui campi sono orientati in direzioni alternate; l'elettrone emette radiazione di sincrotrone che, a turno, interagisce coerentemente con lo stesso elettrone e ciò porta a un grosso aumento del campo di radiazione alla frequenza di risonanza . Il laser può emettere una radiazione elettromagnetica coerente ad alta radianza con un ampio intervallo di frequenze, che va dalle microonde ai raggi X morbidi. Questo strumento potrà essere utilizzato per l'industria, per le comunicazioni e per varie applicazioni mediche, come la chirurgia dei tessuti molli. [188]
Gli elettroni sono fondamentali per il funzionamento dei tubi catodici , che sono largamente usati nei dispositivi come computer e televisori . [189] In un tubo fotomoltiplicatore ogni fotone che colpisce il fotocatodo dà inizio a una cascata di elettroni che produce un impulso di corrente rivelabile. [190] I tubi a vuoto sfruttano il flusso di elettroni per manipolare i segnali elettrici e svolgono un ruolo importante nello sviluppo nell'elettronica; nonostante ciò essi sono stati in gran parte soppiantati dai dispositivi a semiconduttori come i transistor . [191]
Note
- ^ M. Born, RJ Blin-Stoyle; JM Radcliffe,Atomic Physics , Courier Dover , 1989, p. 26, ISBN 0-486-65984-4 .
- ^ Electron mass , su physics.nist.gov , NIST . URL consultato il 3 luglio 2019 . . La versione frazionaria è l'inverso del valore decimale (con un'incertezza di 4,4 × 10 −10 )
- ^ [1]
- ^ https://physics.nist.gov/cgi-bin/cuu/Value?mec2mev
- ^ La carica dell'elettrone è il negativo della carica elementare (che è la carica positiva del protone). Valore del CODATA accessibili tramite il NIST alla pagina carica elementare
- ^ ( EN ) IUPAC Gold Book, "electron"
- ^ a b Eichten e Peskin , pp. 811-814 .
- ^ Pauling , pp. 4-10 .
- ^ ( EN ) "The electron and the light-quant from the experimental point of view" ( PDF ), su nobelprize.org . URL consultato il 29 aprile 2014 .
- ^ Arabatzis , pp. 70-74 .
- ^ Dahl , p. 46.
- ^ Dahl , p. 188.
- ^ AH Soukhanov, Word Mysteries & Histories , Houghton Mifflin Company , 1986, p. 73, ISBN 0-395-40265-4 .
- ^ DB Guralnik, Webster's New World Dictionary , Prentice-Hall , 1970, p. 450.
- ^ GJ Stoney, Of the "Electron," or Atom of Electricity , in Philosophical Magazine , vol. 38, n. 5, 1894, pp. 418–420.
- ^ Dahl (1997:55–58).
- ^ RK DeKosky, William Crookes and the quest for absolute vacuum in the 1870s , in Annals of Science , vol. 40, n. 1, 1983, pp. 1-18, DOI : 10.1080/00033798300200101 .
- ^ a b c HM Leicester, The Historical Background of Chemistry , Courier Dover Publications , 1971, pp. 221-222, ISBN 0-486-61053-5 .
- ^ Dahl (1997:64–78).
- ^ P. Zeeman, Sir William Crookes, FRS , in Nature , vol. 77, n. 1984, 1907, pp. 1-3, Bibcode : 1907Natur..77....1C , DOI : 10.1038/077001a0 .
- ^ a b c Dahl (1997:99).
- ^ a b c d JJ Thomson, Cathode Rays , in Philosophical Magazine , vol. 44, 1897, p. 293.
- ^ R. Wilson, Astronomy Through the Ages: The Story of the Human Attempt to Understand the Universe , CRC Press , 1997, p. 138, ISBN 0-7484-0748-0 .
- ^ JJ Thomson, Nobel Lecture: Carriers of Negative Electricity ( PDF ), su nobelprize.org , The Nobel Foundation , 1906. URL consultato il 25 agosto 2008 (archiviato dall' url originale il 10 ottobre 2008) .
- ^ TJ Trenn, Rutherford on the Alpha-Beta-Gamma Classification of Radioactive Rays , in Isis , vol. 67, n. 1, 1976, pp. 61-75, DOI : 10.1086/351545 , JSTOR 231134 .
- ^ H. Becquerel, Déviation du Rayonnement du Radium dans un Champ Électrique , in Comptes Rendus de l'Académie des Sciences , vol. 130, 1900, pp. 809-815. ( FR )
- ^ Buchwald and Warwick (2001:90–91).
- ^ WG Myers, Becquerel's Discovery of Radioactivity in 1896 , in Journal of Nuclear Medicine , vol. 17, n. 7, 1976, pp. 579-582, PMID 775027 .
- ^ IK Kikoin, IS Sominskiĭ, Abram Fedorovich Ioffe (on his eightieth birthday) , in Soviet Physics Uspekhi , vol. 3, n. 5, 1961, pp. 798-809, Bibcode : 1961SvPhU...3..798K , DOI :10.1070/PU1961v003n05ABEH005812 . Pubblicazione originale in russo: И.К. Кикоин, М.С. Соминский, Академик А.Ф. Иоффе ( PDF ), in Успехи Физических Наук , vol. 72, n. 10, 1960, pp. 303-321.
- ^ RA Millikan, The Isolation of an Ion, a Precision Measurement of its Charge, and the Correction of Stokes' Law , in Physical Review , vol. 32, n. 2, 1911, pp. 349-397, Bibcode : 1911PhRvI..32..349M , DOI : 10.1103/PhysRevSeriesI.32.349 .
- ^ NN Das Gupta, SK Ghosh, A Report on the Wilson Cloud Chamber and Its Applications in Physics , in Reviews of Modern Physics , vol. 18, n. 2, 1999, pp. 225-290, Bibcode : 1946RvMP...18..225G , DOI : 10.1103/RevModPhys.18.225 .
- ^ a b c Smirnov , pp. 4-10 .
- ^ Gilbert N. Lewis, The Atom and the Molecule , in Journal of the American Chemical Society , vol. 38, n. 4, aprile 1916, pp. 762-786, DOI : 10.1021/ja02261a002 .
- ^ a b T. Arabatzis, K. Gavroglu, The chemists' electron , in European Journal of Physics , vol. 18, n. 3, 1997, pp. 150-163, Bibcode : 1997EJPh...18..150A , DOI : 10.1088/0143-0807/18/3/005 .
- ^ Irving Langmuir, The Arrangement of Electrons in Atoms and Molecules ( PDF ), in Journal of the American Chemical Society , vol. 41, n. 6, 1919, pp. 868-934 (archiviato dall' url originale il 30 marzo 2012) .
- ^ Eric R. Scerri, The Periodic Table , Oxford University Press US, 2007, pp. 205-226.
- ^ Michela Massimi, Pauli's Exclusion Principle, The Origin and Validation of a Scientific Principle , Cambridge University Press, 2005.
- ^ ( DE ) GE Uhlenbeck, S. Goudsmith, Ersetzung der Hypothese vom unmechanischen Zwang durch eine Forderung bezüglich des inneren Verhaltens jedes einzelnen Elektrons , in Die Naturwissenschaften , vol. 13, n. 47, 1925.
- ^ ( DE ) W. Pauli, Über die Gesetzmäßigkeiten des anomalen Zeemaneffektes , in Zeitschrift für Physik , vol. 16, n. 1, 1923, pp. 155-164.
- ^ The Nobel Prize in Physics 1929 , su nobelprize.org . URL consultato il 6 aprile 2012 .
- ^ a b Louis de Broglie, Nobel Lecture: The Wave Nature of the Electron ( PDF ), su nobelprize.org , The Nobel Foundation , 1929. URL consultato il 30 agosto 2008 .
- ^ Clinton Davisson, Nobel Lecture: The Discovery of Electron Waves ( PDF ), su nobelprize.org , The Nobel Foundation , 1937. URL consultato il 30 agosto 2008 .
- ^ ( EN ) Albert Einstein, Leopold Infeld, The Evolution of Physics , 1967, pp. 262-263, ISBN 978-0-671-20156-2 .
- ^ Erwin Schrödinger, Quantisierung als Eigenwertproblem , in Annalen der Physik , vol. 385, n. 13, 1926, pp. 437-490, Bibcode : 1926AnP...385..437S , DOI : 10.1002/andp.19263851302 . ( DE )
- ^ John S. Rigden, Hydrogen , Harvard University Press , 2003, pp. 59-86, ISBN 0-674-01252-6 .
- ^ Bruce Cameron Reed, Quantum Mechanics , Jones & Bartlett Publishers , 2007, pp. 275-350, ISBN 0-7637-4451-4 .
- ^ Paul AM Dirac, The Quantum Theory of the Electron , in Proceedings of the Royal Society of London A , vol. 117, n. 778, 1928, pp. 610 -624, DOI : 10.1098/rspa.1928.0023 .
- ^ , Paul AM Dirac, Nobel Lecture: Theory of Electrons and Positrons ( PDF ), su nobelprize.org , The Nobel Foundation , 1933. URL consultato il 1º novembre 2008 .
- ^ Carl D. Anderson, The Positive Electron , in Physical Review , vol. 43, n. 6, 1933, pp. 491–494, Bibcode : 1933PhRv...43..491A , DOI : 10.1103/PhysRev.43.491 .
- ^ Helge Kragh, Quantum Generations: A History of Physics in the Twentieth Century , Princeton University Press , 2002, p. 132, ISBN 0-691-09552-3 .
- ^ Frank Gaynor, Concise Encyclopedia of Atomic Energy , The Philosophical Library , 1950, p. 117.
- ^ Felix Finster, The principle of the fermionic projector , American Mathematical Soc., 2006, p. 16, ISBN 0-8218-3974-8 .
- ^ The Nobel Prize in Physics 1965 , su nobelprize.org , The Nobel Foundation . URL consultato il 4 novembre 2008 .
- ^ ( EN ) Wolfgang KH Panofsky, The Evolution of Particle Accelerators & Colliders ( PDF ), su slac.stanford.edu . URL consultato l'11 aprile 2010 .
- ^ ( EN ) Malcom W. Browne, Donald William Kerst Dies at 81; Built Particle Accelerators in 40's , su nytimes.com . URL consultato l'11 aprile 2010 .
- ^ Elder, Gurewitsch, Langmuir e Pollock , pp. 829-830 .
- ^ Hoddeson, Brown, Riordan e Dresden , pp. 25-26 .
- ^ Bernardini , pp. 156-183 .
- ^ ( EN ) Testing the Standard Model: The LEP experiments , su public.web.cern.ch . URL consultato l'11 aprile 2010 .
- ^ LEP reaps a final harvest , su cerncourier.com . URL consultato l'11 aprile 2010 .
- ^ ( EN ) Synchrotron Radiation ( PDF ), su asd.gsfc.nasa.gov .
- ^ Encyclopedia Britannica - Electron , su britannica.com . URL consultato il 26 luglio 2011 .
- ^ a b c d Curtis , p. 74.
- ^ Povh .
- ^ Murphy , pp. 1611-1613 .
- ^ Zorn , pp. 2566-2576 .
- ^ a b Raith e Mulvey , pp. 777-781 .
- ^ Gabrielse , pp. 030802(1-4).
- ^ Dehmelt , pp. 102-110 .
- ^ Meschede , p. 168.
- ^ Il raggio classico dell'elettrone è ottenuto nel seguente modo: si assume la carica dell'elettrone distribuita uniformemente all'interno di una sfera, che assume così un'energia potenziale elettrostaica. L'energia eguaglia l'energia a riposo dell'elettrone, definita dalla relatività ristretta come E=mc 2 . In elettrostatica l'energia potenziale di una sfera con raggio r e carica e è data da:
- ^ Steinberg , pp. 2582-2586 .
- ^ Yao , pp. 77-115 .
- ^ Tale risultato è mostrato attraverso l'importante esperimento della doppia fenditura , in cui si mostra la natura ondulatoria dell'elettrone, che attraversa le due fenditure contemporaneamente causando una figura di interferenza .
- ^ a b c Munowitz , pp. 162-218 .
- ^ La probabilità che la particella si trovi nell'intervallo al tempo t è:
- ^ Lo scambio di due elettroni comporta che la funzione d'onda diventi , dove le variabili e corrispondono rispettivamente alle posizioni del primo e del secondo elettrone.
- ^ L'equazione agli autovalori per l'osservabile di spin al quadrato è:
- ^ L'equazione agli autovalori per l'osservabile di spin nella direzione dell'asse z è
- ^ a b Odom , pp. 030801(1-4).
- ^ Il magnetone di Bohr è definito come:
- ^ Anastopoulos , pp. 261-262 .
- ^ La scrittura generale dell'equazione di Schrödinger è:
- ^ ( EN ) Special Relativity , su www2.slac.stanford.edu , slac.stanford.edu. URL consultato il 5 aprile 2010 .
- ^ Risolvendo per la velocità dell'elettrone, e usando l'approssimazione di grandi , si ottiene:
- ^ Adams , p. 215.
- ^ Gordon Kane, Are virtual particles really constantly popping in and out of existence? Or are they merely a mathematical bookkeeping device for quantum mechanics? , su scientificamerican.com . URL consultato il 9 aprile 2010 (archiviato dall' url originale il 10 agosto 2011) .
- ^ Nello specifico si ha che Δ E ·Δ t ≥ ħ
- ^ Taylor , p. 464.
- ^ John Gribbin, More to electrons than meets the eye , su newscientist.com , 25 gennaio 1997. URL consultato il 9 aprile 2010 .
- ^ Hitoshi Murayama, Supersymmetry Breaking Made Easy, Viable and Generic , Proceedings of the XLIInd Rencontres de Moriond on Electroweak Interactions and Unified Theories , La Thuile , 10–17 marzo 2006, arΧiv : 0709.3041 .
- ^ Mohr, Taylor e Newell, CODATA recommended values of the fundamental physical constants: 2006 , 2008, p. 646.
- ^ Murray Gell-mann, Murray Gell-mann: Selected Papers , World Scientific Series in 20th Century Physics, 2010, p. 3, ISBN 978-981-283-684-7 . URL consultato il 23 aprile 2012 (archiviato dall' url originale il 19 maggio 2012) .
- ^ La costante di struttura fine , che in unità naturali è legata alla carica elettrica dell'elettrone attraverso la formula:
- ^ Current advances: The fine-structure constant and quantum Hall effect , su physics.nist.gov . URL consultato il 23 aprile 2012 .
- ^ M. Göckeler, R. Horsley, V. Linke, P. Rakow, G. Schierholz, H. Stüben, Is there a Landau Pole Problem in QED? , 1997.
- ^ Schwinger , pp. 416-417 .
- ^ Huang , pp. 123-125 .
- ^ Foldy , pp. 29-36 .
- ^ Sidharth , pp. 497-506 .
- ^ Genz .
- ^ Levine , pp. 424-427 .
- ^ Numeri quantici e livelli energetici , su sapere.it . URL consultato il 17 marzo 2014 .
- ^ Per atomo leggero si intende un numero atomico minore di 30.
- ^ Mulliken , pp. 13-24 .
- ^ Burhop , pp. 2-3 .
- ^ Claus Grupen, Physics of Particle Detection , AIP Conference Proceedings, Instrumentation in Elementary Particle Physics, VIII , vol. 536, Istanbul, Dordrecht, D. Reidel Publishing Company, 28 giugno – 10 luglio, 1999, pp. 3-34, DOI : 10.1063/1.1361756 .
- ^ Jiles , pp. 280-287 .
- ^ Löwdin, Brändas e Kryachko , pp. 393-394 .
- ^ McQuarrie e Simon , pp. 280-287 .
- ^ Daudel , pp. 1310-1320 .
- ^ Crowell , pp. 129-152 .
- ^ Munowitz , p. 160.
- ^ Mahadevan, Narayan e Yi , pp. 327-337 .
- ^ La radiazione proveniente da elettroni non relativistici è a volte chiamata radiazione di ciclotrone .
- ^ Rohrlich , pp. 1109-1112 .
- ^ Georgi , p. 427.
- ^ Blumenthal , pp. 237-270 .
- ^ Il cambiamento della lunghezza d'onda Δ λ dipende dall'angolo di rinculo θ dalla seguente relazione:
- ^ ( EN ) Compton wavelength λ c , su physics.nist.gov . URL consultato l'11 aprile 2010 .
- ^ Chen, Maksimchuk e Umstadter , pp. 653-655 .
- ^ ( EN ) Fine-structure constant α , su physics.nist.gov . URL consultato l'11 aprile 2010 .
- ^ Beringer e Montgomery , pp. 222-224 .
- ^ Wilson e Buffa , p. 888.
- ^ Eichler , pp. 67-72 .
- ^ Hubbell , pp. 614-623 .
- ^ Chris Quigg, The Electroweak Theory , TASI 2000: Flavor Physics for the Millennium , Boulder , arXiv, 4-30 giugno 2000, p. 80, arΧiv : hep-ph/0204104v1 .
- ^ Rakov, Vladimir A.; Uman, Martin A., Lightning: Physics and Effects , Cambridge University Press, 2007, p. 4, ISBN 0-521-03541-4 .
- ^ Gordon R. Freeman, Triboelectricity and some associated phenomena , in Materials science and technology , vol. 15, n. 12, 1999, pp. 1454–1458.
- ^ Keith M. Forward, Daniel J. Lacks; R. Mohan Sankaran, Methodology for studying particle–particle triboelectrification in granular materials , in Journal of Electrostatics , vol. 67, n. 2-3, 2009, pp. 178–183, DOI : 10.1016/j.elstat.2008.12.002 .
- ^ Steven Weinberg, The Discovery of Subatomic Particles , Cambridge University Press, 2003, pp. 15–16, ISBN 0-521-82351-X .
- ^ a b JM Ziman, Electrons and Phonons: The Theory of Transport Phenomena in Solids , Oxford University Press, 2001, p. 260, ISBN 0-19-850779-8 .
- ^ Liang-fu Lou, Introduction to phonons and electrons , World Scientific, 2003, pp. 162,164, ISBN 978-981-238-461-4 .
- ^ ( EN ) Electrons in Crystals , su eng.fsu.edu . URL consultato il 13 aprile 2012 .
- ^ MK Achuthan, Bhat, KN, Fundamentals of Semiconductor Devices , Tata McGraw-Hill, 2007, pp. 49–67, ISBN 0-07-061220-X .
- ^ Peter Main, When electrons go with the flow: Remove the obstacles that create electrical resistance, and you get ballistic electrons and a quantum surprise , in New Scientist , vol. 1887, 12 giugno 1993, p. 30. URL consultato il 9 ottobre 2008 .
- ^ Glenn R. Blackwell, The Electronic Packaging Handbook , CRC Press, 2000, pp. 6.39–6.40, ISBN 0-8493-8591-1 .
- ^ Durrant, Quantum Physics of Matter: The Physical World , CRC Press, 2000, pp. 43, 71–78, ISBN 0-7503-0721-8 .
- ^ Staff, The Nobel Prize in Physics 1972 , su nobelprize.org , The Nobel Foundation, 2008. URL consultato il 13 ottobre 2008 .
- ^ Alan M. Kadin, Spatial Structure of the Cooper Pair , in Journal of Superconductivity and Novel Magnetism , vol. 20, n. 4, 2007, pp. 285–292, DOI : 10.1007/s10948-006-0198-z , arΧiv : cond-mat/0510279 .
- ^ Discovery About Behavior Of Building Block Of Nature Could Lead To Computer Revolution , su ScienceDaily.com , 31 luglio 2009. URL consultato il 1º agosto 2009 .
- ^ Yodchay Jompol, CJ Ford, JP Griffiths, I Farrer, GA Jones, D Anderson, DA Ritchie, TW Silk e AJ Schofield, Probing Spin-Charge Separation in a Tomonaga-Luttinger Liquid , in Science , vol. 325, n. 5940, 31 luglio 2009, pp. 597–601, DOI : 10.1126/science.1171769 , PMID 19644117 . URL consultato il 1º agosto 2009 .
- ^ Paul F. Lurquin, The Origins of Life and the Universe , Columbia University Press, 2003, p. 2, ISBN 0-231-12655-7 .
- ^ Joseph Silk, The Big Bang: The Creation and Evolution of the Universe , 3ª ed., Macmillan, 2000, pp. 110–112, 134–137, ISBN 0-8050-7256-X .
- ^ Vic Christianto, Thirty Unsolved Problems in the Physics of Elementary Particles ( PDF ), in Progress in Physics , vol. 4, 2007, pp. 112–114 (archiviato dall' url originale il 10 settembre 2008) .
- ^ Edward W. Kolb, The Development of Baryon Asymmetry in the Early Universe , in Physics Letters B , vol. 91, n. 2, 7 aprile 1980, pp. 217–221, DOI : 10.1016/0370-2693(80)90435-9 .
- ^ Eric Sather, The Mystery of Matter Asymmetry ( PDF ), su slac.stanford.edu . URL consultato il 12 aprile 2010 .
- ^ Scott Burles, Kenneth M. Nollett; Michael S. Turner, Big-Bang Nucleosynthesis: Linking Inner Space and Outer Space , su arxiv.org , arXiv, University of Chicago, 19 marzo 1999. URL consultato il 12 aprile 2010 .
- ^ AM Boesgaard, G. Steigman, Big bang nucleosynthesis – Theories and observations , in Annual review of astronomy and astrophysics , vol. 23, n. 2, 1985, pp. 319–378, DOI : 10.1146/annurev.aa.23.090185.001535 .
- ^ a b Rennan Barkana, The First Stars in the Universe and Cosmic Reionization , in Science , vol. 313, n. 5789, 18 agosto 2006, pp. 931–934, DOI : 10.1126/science.1125644 , PMID 16917052 .
- ^ EM Burbidge et al. , Synthesis of Elements in Stars , in Reviews of Modern Physics , vol. 29, n. 4, 1957, pp. 548-647, Bibcode : 1957RvMP...29..547B , DOI : 10.1103/RevModPhys.29.547 .
- ^ CL Fryer, Mass Limits For Black Hole Formation , in Astrophysical Journal , vol. 522, n. 1, 1999, pp. 413-418, Bibcode : 1999ApJ...522..413F , DOI : 10.1086/307647 , arXiv : astro-ph/9902315 .
- ^ MK Parikh, F. Wilczek, Hawking Radiation As Tunneling , in Physical Review Letters , vol. 85, n. 24, 2000, pp. 5042-5045, Bibcode : 2000PhRvL..85.5042P , DOI : 10.1103/PhysRevLett.85.5042 , PMID 11102182 , arXiv : hep-th/9907001 .
- ^ ( EN ) SW Hawking , Black hole explosions? , in Nature , vol. 248, 5443doi=10.1038/248030a0, 1974, pp. 30-31, Bibcode : 1974Natur.248...30H .
- ^ ( EN ) F. Halzen, D. Hooper, High-energy neutrino astronomy: the cosmic ray connection , in Reports on Progress in Physics , vol. 66, n. 7, 2002, pp. 1025-1078, Bibcode : 2002astro.ph..4527H , DOI : 10.1088/0034-4885/65/7/201 , arXiv : astro-ph/0204527 .
- ^ ( EN ) JF Ziegler, Terrestrial cosmic ray intensities , in IBM Journal of Research and Development , vol. 42, n. 1, 1998, pp. 117-139, DOI : 10.1147/rd.421.0117 .
- ^ ( EN ) Stuart Wolpert, Scientists solve 30-year-old aurora borealis mystery , su universityofcalifornia.edu , 24 luglio 2008. URL consultato il 12 aprile 2010 (archiviato dall' url originale il 17 agosto 2008) .
- ^ Murayama, Hitoshi (March 10–17, 2006). "Supersymmetry Breaking Made Easy, Viable and Generic". Proceedings of the XLIInd Rencontres de Moriond on Electroweak Interactions and Unified Theories. La Thuile, Italy. arXiv : 0709.3041 . —lists a 9% mass difference for an electron that is the size of the Planck distance.
- ^ Staff, The Nobel Prize in Physics 1989 , su nobelprize.org , The Nobel Foundation, 2008. URL consultato il 24 settembre 2008 .
- ^ Philip Ekstrom, The isolated Electron ( PDF ), in Scientific American , vol. 243, n. 2, 1980, pp. 91–101. URL consultato il 24 settembre 2008 .
- ^ Electron filmed for the first time ever , su physorg.com , physorg. URL consultato il 30 marzo 2012 .
- ^ ( EN ) J. Mauritsson et al. , Coherent Electron Scattering Captured by an Attosecond Quantum Stroboscope , in Physical Review Letters , vol. 100, 2008, p. 073003, DOI : 10.1103/PhysRevLett.100.073003 .
- ^ Donald A. Gurnett e RR Anderson, Electron Plasma Oscillations Associated with Type III Radio Bursts , in Science , vol. 194, n. 4270, 10 dicembre 1976, pp. 1159–1162, DOI : 10.1126/science.194.4270.1159 , PMID 17790910 .
- ^ WC Martin, Wiese, WL, Atomic Spectroscopy: A Compendium of Basic Ideas, Notation, Data, and Formulas , su physics.nist.gov , National Institute of Standards and Technology, maggio 2007. URL consultato l'8 gennaio 2007 .
- ^ Grant R. Fowles, Introduction to Modern Optics , Courier Dover Publications, 1989, pp. 227–233, ISBN 0-486-65957-7 .
- ^ Andrea Damascelli, Probing the Electronic Structure of Complex Systems by ARPES , in Physica Scripta , T109, 2004, pp. 61–74, DOI : 10.1238/Physica.Topical.109a00061 .
- ^ ( EN ) Image #: L-1975-02972 , su grin.hq.nasa.gov . URL consultato il 12 aprile 2010 (archiviato dall' url originale il 7 dicembre 2008) .
- ^ ( EN ) John Elmer, Standardizing the Art of Electron-Beam Welding , su llnl.gov . URL consultato il 12 aprile 2010 (archiviato dall' url originale il 20 settembre 2008) .
- ^ Schultz , pp. 2-3 .
- ^ Benedict , p. 273.
- ^ Faik S. Ozdemir,Electron beam lithography , Proceedings of the 16th Conference on Design automation , San Diego , IEEE Press, 25-27 giugno 1979, pp. 383-391. URL consultato il 12 aprile 2010 .
- ^ Madou , pp. 53-54 .
- ^ Jongen Yves, Arnold Herer, APS/AAPT Joint Meeting , American Physical Society, 2-5 maggio 1996. URL consultato il 12 aprile 2010 .
- ^ Beddar , p. 700.
- ^ Michael J. Gazda, Lawrence R. Coia, Principles of Radiation Therapy , su cancernetwork.com . URL consultato il 12 aprile 2010 .
- ^ La polarizzazione di un fascio di elettroni significa che lo spin di tutti gli elettroni punta in una direzione. In altre parole, la proiezione dello spin di tutti gli elettroni lungo il loro vettore della quantità di moto ha lo stesso segno.
- ^ Chao , pp. 155, 188.
- ^ D. McMullan, Scanning Electron Microscopy: 1928–1965 , su www-g.eng.cam.ac.uk , g.eng.cam.ac.uk, 1993. URL consultato il 9 febbraio 2012 .
- ^ HS Slayter, Light and electron microscopy , Cambridge University Press , 1992, p. 1, ISBN 0-521-33948-0 .
- ^ H. Cember,Introduction to Health Physics , McGraw-Hill Professional , 1996, p. 42–43, ISBN 0-07-105461-8 .
- ^ R. Erni, et al. , Atomic-Resolution Imaging with a Sub-50-pm Electron Probe , in Physical Review Letters , vol. 102, n. 9, 2009, p. 096101, Bibcode : 2009PhRvL.102i6101E , DOI : 10.1103/PhysRevLett.102.096101 , PMID 19392535 .
- ^ JJ Bozzola, LD Russell,Electron Microscopy: Principles and Techniques for Biologists , Jones & Bartlett Publishers, 1999, p. 12, 197-199, ISBN 0-7637-0192-0 .
- ^ SL Flegler, JW Heckman Jr., KL Klomparens, Scanning and Transmission Electron Microscopy: An Introductiom , Oxford University Press , 1995, pp. 43-45, ISBN 0-19-510751-9 .
- ^ JJ Bozzola, LD Russell, Electron Microscopy: Principles and Techniques for Biologists , 2ª ed., Jones & Bartlett Publishers, 1999, p. 9, ISBN 0-7637-0192-0 .
- ^ Oura , pp. 1-45 .
- ^ Ichimiya , p. 1.
- ^ Heppell , pp. 686-688 .
- ^ HP Freund, T. Antonsen, Principles of Free-Electron Lasers , Springer Verlag , 1996, pp. 1-30, ISBN 0-412-72540-1 .
- ^ JW Kitzmiller, Television Picture Tubes and Other Cathode-Ray Tubes: Industry and Trade Summary , DIANE Publishing, 1995, pp. 3-5, ISBN 0-7881-2100-6 .
- ^ N. Sclater, Electronic Technology Handbook , McGraw-Hill Professional , 1999, pp. 227–228, ISBN 0-07-058048-0 .
- ^ The History of the Integrated Circuit , su nobelprize.org . URL consultato il 10 febbraio 2012 .
Bibliografia
Testi generici
- Paolo Mazzoldi, Massimo Nigro e Cesare Voci, Fisica Volume II , 2ª edizione, Edises, 2000, ISBN 88-7959-152-5 .
- B. Povh, K. Rith e C. Scholz, Particelle e nuclei , Bollati Boringhieri, 1998, ISBN 88-339-5595-8 .
- ( EN ) Steve Adams, Frontiers: Twentieth Century Physics , CRC Press, 2000, ISBN 0-7484-0840-1 .
- ( EN ) Charis Anastopoulos,Particle Or Wave: The Evolution of the Concept of Matter in Modern Physics , Princeton University Press, 2008, ISBN 0-691-13512-6 .
- ( EN ) Theodore Arabatzis, Representing Electrons: A Biographical Approach to Theoretical Entities , University of Chicago Press, 2006, ISBN 0-226-02421-0 . URL consultato il 1º aprile 2010 .
- ( EN ) Gary F. Benedict, Nontraditional Manufacturing Processes , CRC Press, 1987, ISBN 0-8247-7352-7 .
- ( EN ) Eric HS Burhop, The Auger Effect and Other Radiationless Transitions , New York, Cambridge University Press , 1952, pp. 2–3.
- ( EN ) Alexander W. Chao, Maury Tigner, Handbook of Accelerator Physics and Engineering , World Scientific Publishing Company, 1999, ISBN 981-02-3500-3 .
- ( EN ) Benjamin Crowell, Electricity and Magnetism , Light and Matter, 2000, ISBN 0-9704670-4-4 .
- ( EN ) Lorenzo J. Curtis, Atomic Structure and Lifetimes: A Conceptual Approach , Cambridge University Press, 2003, ISBN 0-521-53635-9 . URL consultato il 1º aprile 2010 .
- ( EN ) Per F. Dahl, Flash of the Cathode Rays: A History of JJ Thomson's Electron , CRC Press, 1997, ISBN 0-7503-0453-7 . URL consultato il 1º aprile 2010 .
- ( EN ) Henning Genz,Nothingness: The Science of Empty Space , Da Capo Press, 2001, ISBN 0-7382-0610-5 .
- ( EN ) Howard Georgi, The New Physics , Cambridge University Press , 1989, ISBN 0-521-43831-4 .
- ( EN ) MC Gupta, Atomic and Molecular Spectroscopy , New Age Publishers, 2001, ISBN 81-224-1300-5 .
- ( EN ) Hermann Haken, Hans Christoph Wolf, WD Brewer, The Physics of Atoms and Quanta: Introduction to Experiments and Theory , Springer Verlag , 2005, ISBN 3-540-20807-0 .
- ( EN ) Lillian Hoddeson, Laurie Brown, Michael Riordan, Max Dresden, The Rise of the Standard Model: Particle Physics in the 1960s and 1970s , Cambridge University Press , 1997, ISBN 0-521-57816-7 .
- ( EN ) Kerson Huang, Fundamental Forces of Nature: The Story of Gauge Fields , World Scientific, 2007, ISBN 981-270-645-3 .
- ( EN ) A. Ichimiya, PI Cohen, Reflection High-energy Electron Diffraction , Cambridge University Press , 2004, ISBN 0-521-45373-9 .
- ( EN ) David Jiles, Introduction to Magnetism and Magnetic Materials , CRC Press, 1998, pp. 280–287, ISBN 0-412-79860-3 .
- ( EN ) Per Olov Löwdin, Erkki Erkki Brändas, Eugene S. Kryachko, Fundamental World of Quantum Chemistry: A Tribute to the Memory of Per-Olov Löwdin , Springer Verlag , 2003, ISBN 1-4020-1290-X .
- ( EN ) Marc J. Madou, Fundamentals of Microfabrication: the Science of Miniaturization , 2ª ed., CRC Press, 2002, ISBN 0-8493-0826-7 .
- ( EN ) Donald Allan McQuarrie, John Douglas Simon, Physical Chemistry: A Molecular Approach , University Science Books, 1997, ISBN 0-935702-99-7 .
- ( EN ) Dieter Meschede, Optics, light and lasers: The Practical Approach to Modern Aspects of Photonics and Laser Physics , Wiley-VCH, 2004, ISBN 3-527-40364-7 .
- ( EN ) Michael Munowitz,Knowing, The Nature of Physical Law , Oxford University Press, 2005, ISBN 0-19-516737-6 .
- ( EN ) K. Oura, VG Lifshits, AA Saranin, AV Zotov, M. Katayama, Surface Science: An Introduction , Springer Verlag , 2003, ISBN 3-540-00545-5 .
- ( EN ) Linus C. Pauling , The Nature of the Chemical Bond and the Structure of Molecules and Crystals: an introduction to modern structural chemistry , 3ª ed., Cornell University Press, 1960, ISBN 0-8014-0333-2 . URL consultato il 29 marzo 2010 .
- ( EN ) Wilhelm Raith, Thomas Mulvey, Constituents of Matter: Atoms, Molecules, Nuclei and Particles , CRC Press, 2001, p. 777–781, ISBN 0-8493-1202-7 .
- ( EN ) Helmut Schultz, Electron Beam Welding , Woodhead Publishing, 1993, ISBN 1-85573-050-2 .
- ( EN ) Boris M. Smirnov, Physics of Atoms and Ions , Springer Verlag , 2003, ISBN 0-387-95550-X . URL consultato il 23 gennaio 2012 .
- ( EN ) John Taylor, The New Physics , Cambridge University Press , 1989, ISBN 0-521-43831-4 .
- ( EN ) Jerry Wilson, Anthony Buffa, College Physics , 4ª ed., Prentice Hall, 2000, ISBN 0-13-082444-5 .
- ( EN ) Robert Wilson, Astronomy Through the Ages: The Story of the Human Attempt to Understand the Universe , CRC Press, 1997, ISBN 0-7484-0748-0 . URL consultato il 1º aprile 2010 .
Pubblicazioni scientifiche
- ( EN ) AS Beddar, Mobile linear accelerators for intraoperative radiation therapy [ collegamento interrotto ] ( abstract ), in AORN Journal , vol. 74, 2001, DOI : 10.1016/S0001-2092(06)61769-9 .
- ( EN ) R. Beringer, CG Montgomery, The Angular Distribution of Positron Annihilation Radiation , in Physical Review , vol. 61, n. 5-6, 1942, DOI : 10.1103/PhysRev.61.222 .
- ( EN ) C. Bernardini, AdA: The First Electron–Positron Collider , in Physics in Perspective , vol. 6, n. 2, 2004, Bibcode : 2004PhP.....6..156B , DOI : 10.1007/s00016-003-0202-y .
- ( EN ) GJ Blumenthal, Bremsstrahlung, Synchrotron Radiation, and Compton Scattering of High-Energy Electrons Traversing Dilute Gases , in Reviews of Modern Physics , vol. 42, 1970, DOI : 10.1103/RevModPhys.42.237 .
- ( EN ) S. Chen, A. Maksimchuk, D. Umstadter, Experimental observation of relativistic nonlinear Thomson scattering , in Nature , vol. 396, 1998, DOI : 10.1038/25303 .
- ( EN ) R. Daudel, RFW Bader, ME Stephens, DS Borrett, The Electron Pair in Chemistry , in Canadian Journal of Chemistry , vol. 52, 11 ottobre 1973, DOI : 10.1139/v74-201 . URL consultato il 7 aprile 2010 (archiviato dall' url originale l'8 gennaio 2014) .
- ( EN ) Hans Dehmelt, A Single Atomic Particle Forever Floating at Rest in Free Space: New Value for Electron Radius , in Physica Scripta , T22, 1988, DOI : 10.1088/0031-8949/1988/T22/016 .
- ( EN ) J. Eichler, Electron–positron pair production in relativistic ion–atom collisions , in Physics Letters A , vol. 347, n. 1-3, 14 novembre 2005, DOI : 10.1016/j.physleta.2005.06.105 .
- ( EN ) FR Elder, AM Gurewitsch, RV Langmuir, HC Pollock, Radiation from Electrons in a Synchrotron , in Physical Review , vol. 71, n. 11, 1947, DOI : 10.1103/PhysRev.71.829.5 .
- ( EN ) EJ Eichten, ME Peskin, New Tests for Quark and Lepton Substructure , in Physical Review Letters , vol. 50, n. 11, 1983, pp. 811–814, DOI : 10.1103/PhysRevLett.50.811 .
- ( EN ) LL Foldy, On the Dirac Theory of Spin 1/2 Particles and Its Non-Relativistic Limit , in Physical Review , vol. 78, 1950, DOI : 10.1103/PhysRev.78.29 .
- ( EN ) G. Gabrielse, D. Hanneke, T. Kinoshita, M. Nio, B. Odom, New Determination of the Fine Structure Constant from the Electron g Value and QED , in Physical Review Letters , vol. 97, 2006, DOI : 10.1103/PhysRevLett.97.030802 .
- ( EN ) TA Heppell, A combined low energy and reflection high energy electron diffraction apparatus , in Journal of Scientific Instruments , vol. 44, n. 9, 1967, Bibcode : 1967JScI...44..686H , DOI : 10.1088/0950-7671/44/9/311 .
- ( EN ) JH Hubbell, Electron positron pair production by photons: A historical overview , in Radiation Physics and Chemistry , vol. 75, n. 6, 2006, Bibcode : 2006RaPC...75..614H , DOI : 10.1016/j.radphyschem.2005.10.008 .
- ( EN ) I. Levine, D. Koltick, B. Howell, E. Shibata, J. Fujimoto, K. Tauchi, K. Abe, T. Abe, I. Adachi, Measurement of the Electromagnetic Coupling at Large Momentum Transfer , in Physical Review Letters , vol. 78, 1997, DOI : 10.1103/PhysRevLett.78.424 .
- ( EN ) R. Mahadevan, R. Narayan, I. Yi, Harmony in Electrons: Cyclotron and Synchrotron Emission by Thermal Electrons in a Magnetic Field , in Astrophysical Journal , vol. 465, 1996, DOI : 10.1086/177422 , arΧiv : astro-ph/9601073v1 .
- ( EN ) RS Mulliken, Spectroscopy, Molecular Orbitals, and Chemical Bonding , in Science , vol. 157, n. 3784, 1967, DOI : 10.1126/science.157.3784.13 , PMID 5338306 .
- ( EN ) MT Murphy, VV Flambaum, S. Muller, C. Henkel, Strong Limit on a Variable Proton-to-Electron Mass Ratio from Molecules in the Distant Universe , in Science , vol. 320, n. 5883, 20 giugno 2008, DOI : 10.1126/science.1156352 , PMID 18566280 . URL consultato il 5 aprile 2010 .
- ( EN ) B. Odom, D. Hanneke, B. D'Urso, G. Gabrielse, New Measurement of the Electron Magnetic Moment Using a One-Electron Quantum Cyclotron , in Physical Review Letters , vol. 97, 2006, DOI : 10.1103/PhysRevLett.97.030801 .
- ( EN ) F. Rohrlich, The self-force and radiation reaction , in American Journal of Physics , vol. 68, n. 12, 1999, DOI : 10.1119/1.1286430 .
- ( EN ) J. Schwinger, On Quantum-Electrodynamics and the Magnetic Moment of the Electron , in Physical Review , vol. 73, n. 4, 1948, DOI : 10.1103/PhysRev.73.416 .
- ( EN ) BG Sidharth, Revisiting Zitterbewegung , in International Journal of Theoretical Physics , vol. 48, 2008, DOI : 10.1007/s10773-008-9825-8 , arΧiv : 0806.0985 .
- ( EN ) RI Steinberg, K. Kwiatkowski, W. Maenhaut, NS Wall, Experimental test of charge conservation and the stability of the electron , in Physical Review D , vol. 61, n. 2, 1999, DOI : 10.1103/PhysRevD.12.2582 .
- ( EN ) WM Yao, Review of Particle Physics , in Journal of Physics G: Nuclear and Particle Physics , vol. 33, n. 1, luglio 2006, DOI : 10.1088/0954-3899/33/1/001 .
- ( EN ) JC Zorn, George E. Chamberlain, Vernon W. Hughes, Experimental Limits for the Electron-Proton Charge Difference and for the Charge of the Neutron , in Physical Review , vol. 129, n. 6, 1963, DOI : 10.1103/PhysRev.129.2566 .
Voci correlate
- Ambiti scientifici
- Particelle
- Aspetti chimici
- Elettrone spaiato
- Doppietto elettronico
- Trasferimento di elettroni
- Accettore di elettroni
- Donatore di elettroni
- Elettrone del guscio interno
- Elettrone solvatato
- Elettrone delocalizzato
- Configurazione elettronica
- Fenomeni fisici
- Costanti e unità di misura
Altri progetti
-
 Wikiquote contiene citazioni sull' elettrone
Wikiquote contiene citazioni sull' elettrone -
 Wikizionario contiene il lemma di dizionario « elettrone »
Wikizionario contiene il lemma di dizionario « elettrone » -
 Wikimedia Commons contiene immagini o altri file su elettrone
Wikimedia Commons contiene immagini o altri file su elettrone
Collegamenti esterni
- Elettrone , su Treccani.it – Enciclopedie on line , Istituto dell'Enciclopedia Italiana .
- Elettrone , su Vocabolario Treccani , Istituto dell'Enciclopedia Italiana .
- ( EN ) Elettrone , su Enciclopedia Britannica , Encyclopædia Britannica, Inc.
- Particle Data Group , su pdg.lbl.gov .
- Raggio di elettroni in campo elettrico e magnetico incrociato , su bigs.de (archiviato dall' url originale il 20 dicembre 2010) .
| Controllo di autorità | Thesaurus BNCF 3791 · LCCN ( EN ) sh85042423 · GND ( DE ) 4125978-6 · BNF ( FR ) cb13319069f (data) · NDL ( EN , JA ) 00561425 |
|---|