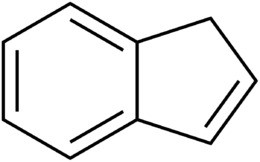
Indene
| Indene | |
|---|---|
| Numele IUPAC | |
| 1H-indenă | |
| Denumiri alternative | |
| Bicicletă [4.3.0] nona-1,3,5,7-tetraenă | |
| Caracteristici generale | |
| Formula moleculară sau brută | C 9 H 8 |
| Masa moleculară ( u ) | 116,16 g / mol |
| numar CAS | |
| Numărul EINECS | 202-393-6 |
| PubChem | 7219 |
| ZÂMBETE | C1C=CC2=CC=CC=C21 |
| Proprietăți fizico-chimice | |
| Densitate (g / cm 3 , în cs ) | 0,997 g / ml |
| Constanta de disociere a acidului la 298 K. | ~ 10 20,1 (în DMSO ) |
| Solubilitate în apă | insolubil |
| Temperatură de topire | -1,8 ° C |
| Temperatura de fierbere | 181,6 ° C |
| Informații de siguranță | |
| Simboluri de pericol chimic | |
| Fraze H | H226-H304 |
| Sfaturi P | P301 + P310-P331 |
Indena este o hidrocarbură policiclică inflamabilă cu formula chimică C 9 H 8 . Este compus dintr-un inel benzenic fuzionat cu inelul ciclopentenic . Este un lichid aromatic incolor, chiar dacă probele sunt adesea galbene pal, fenomen datorat oxidării parțiale a moleculei. Principala utilizare industrială a indenei este în producția de rășini termoplastice indene / cumarone .
Prezență în natură
Endenul apare în mod natural în fracțiunile de gudron de cărbune la fierbere în jurul valorii de 175-185 ° C. Poate fi obținut prin încălzirea acestei fracțiuni cu sodiu pentru a precipita solidul "sodiu-inden". Această etapă exploatează aciditatea slabă a indenei demonstrată de deprotonarea sa de sodiu metalic pentru a da derivatul indenil. Sodiu-indenă este reconvertită în indenă prin distilare cu abur . [2]
Reactivitate
Indena polimerizează ușor. Oxidarea acestuia cu acid dicromat duce la acid homoftalic ( acid o-carboxilfenilacetic ). Se condensează cu oxalat de etil în prezența etoxidului de sodiu pentru a forma esterul inden-oxalic și cu aldehide sau cetone în prezența alcalinelor pentru a forma benzofulvi . Acestea din urmă sunt foarte colorate. O indenă este, de asemenea, un precursor al anionului indenil, un ligand în chimia organometalică cu o anumită notorietate datorită „efectului indenil”.
Notă
- ^ Bordwell FG ,, Acidități de echilibru în soluție de dimetil sulfoxid ,, în Accounts of Chemical Research , vol. 21, 1988, pp. 456-463, DOI : 10.1021 / ar00156a004 .
- ^ Gerd Collin, Rolf Mildenberg, Mechthild Zander, Hartmut Höke, William McKillip, Werner Freitag, Wolfgang Imöhl „Resins, Synthetic” Ullmann's Encyclopedia of Industrial Chemistry Wiley-VCH, Weinheim, 2000.
Elemente conexe
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere pe indene
Wikimedia Commons conține imagini sau alte fișiere pe indene
linkuri externe
- W. v. Miller, Rohde, „Zur Synthese von Indenderivaten” , în Berichte der deutschen chemischen gesellschaft , vol. 23, 1890, p. 1881-1886, DOI : 10.1002 / cber.18900230227 .
- W. v. Miller, Rohde, Zur Synthese von Indenderivaten , în Berichte der deutschen chemischen Gesellschaft , vol. 23, 1890, pp. 1887–1902, DOI : 10.1002 / cber.18900230228 .
- IL Finar, Chimie organică , Longman Scientific & Technical, 1985, ISBN 0-582-44257-5 .
| Controlul autorității | GND ( DE ) 4161475-6 |
|---|