Hidrazone
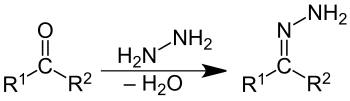
Hidrazonele sunt o clasă de compuși organici cu structură generală R 1 R 2 C = NNH 2 . Acestea sunt obținute prin reacția de adiție nucleofilă a hidrazinei cu o cetonă sau o aldehidă , cu eliminarea ulterioară a apei .
Hidrazonele stabile derivă de obicei din arilchetone , în timp ce alte cetone sau aldehide dau compuși neizolabili care suferă reacții ulterioare. [1]
Utilizări
Formarea hidrazonelor aromatice este utilizată pentru a măsura concentrația de aldehide și cetone cu greutate moleculară mică , de exemplu într-un flux de gaze. De exemplu, 2,4-dinitrofenilhidrazina acoperită pe un absorbant de silice este baza unui cartuș de adsorbție . Hidrazonele sunt apoi eluate și analizate prin HPLC cu un detector UV . În trecut, formarea unei 2,4-dinitrofenilhidrazonă a fost exploatată pentru a identifica aldehida sau cetona, după ce a cristalizat compusul obținut și a măsurat punctul său de topire .
Cianura de carbonil-p-trifluorometoxifenilhidrazonă (FCCP) este utilizată pentru decuplarea sintezei ATP și a reducerii oxigenului în fosforilarea oxidativă în biologia moleculară . Fenilhidrazina reacționează cu glucoza pentru a forma o osazonă .
Metodele de cuplare bazate pe hidrazonă sunt în biotehnologia medicală pentru a cupla medicamentele pentru a viza anticorpi , de exemplu anticorpi împotriva unui anumit tip de celule canceroase . Legătura pe bază de hidrazonă este stabilă la pH neutru (în sânge ), dar este rapid distrusă în mediul acid al lizozomilor celulei. Medicamentul este apoi eliberat în celulă, unde își îndeplinește funcția. [2]
Reacții
Hidrazonele reacționează cu I 2 într-un mediu de bază pentru a produce ioduri de vinil. Alte reacții care produc compuși vinilici sunt reacția Shapiro și reacția Bamford-Stevens . O hidrazonă se formează ca intermediar în reducerea Wolff-Kishner . O altă metodă utilizată pentru sintetizarea hidrazonelor este reacția Japp - Klingemann , care folosește β-cetoacizi sau β-cetoesteri și săruri de arildiazoniu .
N , N ' -dialchilhidrazone
În N , N ' -dialchilhidrazone [3] legătura dublă C = N poate fi hidrolizată , oxidată și redusă , legătura NN poate fi redusă pentru a forma amina liberă. Atomul de carbon al legăturii C = N poate reacționa cu nucleofilii organometalici . Atomul de hidrogen din alfa este de aproximativ zece ori mai acid decât cetona și, prin urmare, carbonul corespunzător este mai necleofil. De exemplu, deprotonarea cu diizopropilamidă de litiu produce un azaenolat care poate fi alchilat de halogenuri de alchil , așa cum a fost descris pentru prima dată de Elias James Corey și Dieter Enders în 1978. [4] [5] În sinteza asimetrică SAMP și RAMP acționează ca un auxiliar chiral cu o hidrazonă chirală intermediară. [6] [7] [8]
Notă
- ^ Michael B. Smith, Jerry March, March's Organic Organic Chemistry , ediția a 6-a, John Wiley & Sons, Inc., 2007, p.1284, ISBN 0-471-72091-7 .
- ^ Anna M. Wu și Peter D. Senter, Arming anticorpi: perspective și provocări pentru imunoconjugați , în Nature Biotechnology , vol. 23, n. 9, Nature Publishing Group, 7 septembrie 2005, pp. 1137-1146, DOI : 10.1038 / nbt1141 .
- ^ R. Lazny și A. Nodzewska, N, N-dialchilhidrazone în sinteză organică. De la N, N-dimetilhidrazone simple la auxiliari chirali susținuți , în Chemical reviews , vol. 110, nr. 3, 2010, pp. 1386–1434, DOI : 10.1021 / cr900067y .
- ^ EJ Corey, Aplicații ale N, N-dimetilhidrazonelor la sinteză. Utilizare în formarea de legături CC eficiente, pozițional și stereochimic selective; hidroliza oxidativă la compuși carbonilici , în Tetrahedron Letters , vol. 17, n. 1, ianuarie 1976, pp. 3-6, DOI : 10.1016 / S0040-4039 (00) 71307-4 .
- ^ EJ Corey și D. Enders, Herstellung und synthetische Verwendung von metalloerten Dimethylhydrazonen Regio- und stereoselektive Alkylierung von Carbonylverbindungen , în Chemische Berichte , vol. 111, nr. 4, aprilie 1978, pp. 1337-1361, DOI : 10.1002 / cber . 19781110413 .
- ^ D. Enders, alchilarea enantioselectivă a aldehidelor prin hidrazone chirale metalizate , în Tetrahedron Letters , vol. 18, nr. 2, 1977, pp. 191-194, DOI : 10.1016 / S0040-4039 (01) 92585-7 .
- ^ Dieter Enders, Peter Fey și Helmut Kipphardt, ( S ) - (-) - 1-Amino-2-metoximetilpirolidină (SAMP) și ( R ) - (+) - 1-amino-2-metoximetilpirolidină (RAMP), versatil chiral auxiliare , în Org. Sintetizator. , vol. 65, 1987, p. 173.
- ^ Dieter Enders, Helmut Kipphardt și Peter Fey, sinteze asimetrice folosind metoda SAMP- / RAMP-hidrazonă: ( S ) - (+) - 4-metil-3-heptanonă , vol. 65, 1987, p. 183.
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere despre Idrazone
Wikimedia Commons conține imagini sau alte fișiere despre Idrazone
linkuri externe
- ( RO ) IUPAC Gold Book, „hidrazone” , pe goldbook.iupac.org .
| Controlul autorității | NDL ( EN , JA ) 00575230 |
|---|