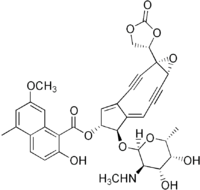
Zinostatină
| Zinostatină | |
|---|---|
| Numele IUPAC | |
| (1a S , 5 R , 6 R , 6a E ) -6 - {[(2 R , 3 R , 4 R , 5 R , 6 R ) -4,5-Dihidroxi-6-metil-3- (metilamino) tetrahidro-2H-piran-2-il] oxi} -1a- (2-oxo-1,3-dioxolan-4-il) -2,3,8,9-tetradehydro-1a, 5,6,9a- tetrahidrociclopenta [5,6] ciclonona [1,2-b] oxiren-5-il 2-hidroxi-7-metoxi-5-metil-1-naftoat | |
| Denumiri alternative | |
| Neocarzinostatină | |
| Caracteristici generale | |
| Formula moleculară sau brută | C 35 H 33 NU 12 |
| Masa moleculară ( u ) | 659,64 g / mol |
| numar CAS | |
| PubChem | 57125363 |
| ZÂMBETE | CC1C(C(C(C(O1)OC2C3CC#CC4C(O4)(C#CC3=CC2OC(=O)C5=C(C=CC6=C(C=C(C=C65)OC)C)O)C7COC(=O)O7)NC)O)O |
| Proprietăți fizico-chimice | |
| Solubilitate în apă | solubil în apă |
| Temperatură de topire | 260 ° C |
| Date farmacologice | |
| Grupa farmacoterapeutică | Citostatic |
| Date farmacocinetice | |
| Excreţie | Renal |
| Informații de siguranță | |
Zinostatina (cunoscută și sub numele de neocarzinostatină ) este un antibiotic , o alchenă aparținând familiei enediyne (adică compuși cu legături triple pe fiecare parte a unei legături duble), cu activitate antitumorală. Molecula este o polipeptidă , mai precis un apoproteina, alcătuit din două părți, o proteină cu o greutate moleculară de 10700, care conține 109 aminoacizi de acid reziduuri de 18 tipuri diferite, și un cromofor , labil, neproteic în natură, cu structură biciclică , responsabil de activitatea biologică a substanței. [1] Există două punți disulfură între cisteină din moleculă. Integritatea structurii, inclusiv conexiunea transversală a punților disulfură, este esențială pentru efectuarea activității biologice. [2]
Istorie
Zinostatina a fost izolată pentru prima dată din culturile de Streptomyces carzinostaticus, soiul F-41 și a fost imediat studiată pentru activitatea sa antineoplazică . Izolarea și caracterizarea ulterioară au avut loc datorită lui Ishida în 1965. [3] [4]
Farmacodinamica
Cromoforul moleculei este un agent foarte puternic, capabil să dăuneze ADN-ului. Este extrem de labilă, iar rolul apoproteinei este de a o proteja și de a o elibera în ADN-ul țintă. [5] Deschiderea epoxidului, în mediul reducător prezent în interiorul celulei, creează condițiile favorabile unei ciclizări Bergman, ducând la un radical intermediar și, în cele din urmă, la clivarea catenei duble de ADN. Ruperea catenelor de ADN apare de preferință la nivelul dezoxiribozei timinei. Studiile experimentale timpurii au arătat că zinostatina a fost foarte activă împotriva diferitelor tumori și leucemii care au cauzat ascită la șoareci și șobolani atunci când au fost administrate intraperitoneal. [6] [7] [8]
Farmacocinetica
După injecția intravenoasă , neocarzinostatina este bine absorbită și distribuită rapid în organism și apoi este excretată rapid în urină . Studiile experimentale efectuate pe șoareci au arătat că, după injectarea unei doze de 100 mg / kg intravenos, cele mai mari concentrații s-au găsit în țesutul renal cu niveluri scăzute în sânge , țesuturi tumorale, piele , stomac , plămâni , pancreas , timus. si tesutul muscular . În această neocarzinostatină seamănă cu distribuția tipică a bleomicinei, cu excepția stomacului și a pancreasului, unde atinge concentrații mari.
Toxicitate
Valorile LD50 la șoareci sunt de 1050 mg / kg pe cale orală și 0,96 mg / kg pe cale intravenoasă.
Utilizări clinice
Compusul a fost utilizat în tratamentul leucemiei și cancerelor , inclusiv a celor din stomac și pancreas. Un derivat de zinostatină conjugat cu un polimer stiren-acid maleic, cunoscut sub numele de zinostatină stimalamer (SMANCS), a fost utilizat ca perfuzie intra-arterială repetată în tratamentul hepatocarcinomului . [9] [10]
Chimie
Neocarzinostatina, în soluție apoasă , absoarbe radiațiile ultraviolete (UV) la o lungime de undă de 278 nm.
Notă
- ^ G. Albers-Schönberg, RS. Dewey; OD. Hensens; JM. Liesch; DAR. Napier; IH. Goldberg, Neocarzinostatin: caracterizare chimică și structură parțială a cromoforului neproteic. , în Biochem Biophys Res Commun , vol. 95, nr. 3, august 1980, pp. 1351-6, PMID 6448053 .
- ^ J. Meienhofer, H. Maeda; CB. Glaser; J. Czombos; K. Kuromizu, Structura primară a neocarzinostatinei, o proteină antitumorală. , în Știință , vol. 178, nr. 4063, noiembrie 1972, pp. 875-6, PMID 4563817 .
- ^ N. Ishida, K. Miyazaki; K. Kumagai; M. Rikimaru, Neocarzinostatin, un antibiotic antitumoral cu greutate moleculară mare. Izolarea, proprietățile fiziochimice și activitățile biologice. , în J Antibiot (Tokyo) , vol. 18, martie 1965, pp. 68-76, PMID 14326086 .
- ^ H. Maeda, K. Kumagai; N. Ishida, caracterizarea neocarzinostatinei. , în J Antibiot (Tokyo) , vol. 19, nr. 6, noiembrie 1966, pp. 253-9, PMID 6013238 .
- ^ 1H. Goldberg, T. Hatayama; LS. Kappen; DAR. Napier, ADN ca țintă pentru un antibiotic proteic: bază moleculară de acțiune. , în Mol Biol Biochem Biophys , voi. 32, 1980, pp. 308-22, PMID 6449657 .
- ^ K. Kumagi, Activitatea antitumorală a carzinostatinei. (Studii asupra substanțelor antibiotice din Actinomycetes. XLV). , în J Antibiot (Tokyo) , vol. 15, martie 1962, pp. 53-9, PMID 14036944 .
- ^ WT. Bradner, DJ. Hutchison, Neocarzinostatin (NSC-69856): un antibiotic antitumoral eficient împotriva leucemiei ascitice L1210 la șoareci. , în Cancer Chemother Rep , vol. 50, nr. 1, ianuarie-februarie 1966, pp. 79-84, PMID 5908739 .
- ^ H. Satoh, Ichimura H., Spectrul antitumoral al neocarzinostatinei pe hepatomele ascitei la șobolani , în Igaku no Ayumi , n. 74, 1970, pp. 499-500.
- ^ T. Okusaka, S. Okada; H. Ishii; M. Ikeda; H. Nakasuka; H. Nagahama; R. Iwata; H. Furukawa; K. Takayasu; Y. Nakanishi; M. Sakamoto, chimioterapie transarterială cu zinostatină stimalamer pentru carcinom hepatocelular. , în Oncologie , vol. 55, nr. 4, pp. 276-83, PMID 9663415 .
- ^ T. Okusaka, S. Okada; H. Ueno; M. Ikeda; R. Iwata; H. Furukawa; K. Takayasu; N. Moriyama; T. Sato; K. Sato, embolizare arterială transcateteră cu zinostatină stimalamer pentru carcinom hepatocelular. , în Oncologie , vol. 62, nr. 3, 2002, pp. 228-33, DOI : 10.59570 , PMID 12065870 .
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere pe zinostatină
Wikimedia Commons conține imagini sau alte fișiere pe zinostatină