HCC
| HCC | |
|---|---|
| Secțiunea longitudinală a ficatului unei femei de 50 de ani cu hepatită C internată pentru prezența ascitei și a durerii abdominale. Neoplazia voluminoasă, albicioasă și multilobulată, ocupă o mare parte a ficatului. | |
| Specialitate | oncologie |
| Clasificare și resurse externe (EN) | |
| ICD-O | 8170/3 |
| ICD-9 -CM | 155 |
| ICD-10 | C22.0 |
| OMIM | 114550 |
| Plasă | D006528 |
| MedlinePlus | 000280 |
| eMedicină | 278354 |
Carcinomul hepatocelular sau carcinomul hepatocelular (CEC sau HCC) sau mai rar hepatomul este cea mai frecventă formă de cancer hepatic . În lume este al optulea tip de neoplasm solid cel mai frecvent întâlnit. Decesele atribuite acestei forme de cancer sunt de un milion pe an [1] .
Epidemiologie
General
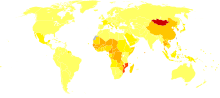
nu există date
mai puțin de 7,5
7.5-15
15-22,5
22.5-30
30-37,5
37,5-45
45-52,5
52,5-60
60-67,5
67,5-75
75-110
mai mult de 110
Se dezvoltă în principal la ficatul cirotic al oamenilor în jurul deceniilor a cincea și a șasea de vechime. Numai în SUA , există aproape 16.000 de cazuri pe an. [3] În Europa există 50 000 de cazuri (estimare bazată pe anul 2000), țările cele mai expuse riscului sunt Grecia , Franța și Anglia , în timp ce în Italia a existat o ușoară creștere. Incidența maximă este înregistrată în unele țări africane și în insulele Pacificului (incidența maximă constatată: 104 la 100.000, față de media 2-7 la 100.000), în țări precum China , Taiwan și Coreea există 150 de cazuri la fiecare milion de locuitori. [4] Țările cu cea mai mică incidență sunt Australia , India și America de Sud . [5]
Sex
Afectează bărbații mai frecvent (la bărbați este a cincea formă cea mai frecventă) decât femeile (raportul a fost calculat ca 4 la 1). [6]
Vârstă
În ceea ce privește vârsta, este mai frecventă în jur de 50-60 de ani, dar în unele țări africane și în China vârsta medie scade considerabil. Au existat cazuri în adolescență și chiar în copilărie, vârsta minimă a fost de doi ani. [7]
Simptomatologie
Deși în majoritatea industrializaților sunt diagnosticați în stadiile incipiente fără simptome (25% din cazuri) prin screeningul pacienților cirotici, cu progresul se constată durere în abdomen , scădere în greutate, ascită , dispepsie , balonare abdominală, anorexie , astenie , hepatomegalie , febră până la cel mai rar abdomen acut și dispnee .
În unele cazuri, în special la pacientul pediatric, se poate observa producția de beta-gonadotropină. [8]
Etiologie
Este adesea considerat a fi cauzat de boli hepatice preexistente, cum ar fi ciroza sau infecția cu hepatită virală . În unele state din Africa sau Asia , există o incidență ridicată legată de virusul hepatitei B [9] , C și G virus infecții. [10]
Alte cauze includ expunerea la aflatoxină , care lasă o amprentă moleculară, adică mutația unei gene. În plus, hemocromatoza și tirozinemia sunt alte afecțiuni asociate cu masa tumorii. Mai mult, alcoolismul a fost mult timp asociat cu starea de ciroză și, prin urmare, cu un risc crescut de cancer hepatic.
Factori de risc minori
Alți factori de risc includ sindromul Alagille [11] , boala Wilson [12] , citrullinemia , galactozemia , utilizarea excesivă de androgeni [13] , în timp ce gradul de risc legat de fumul de țigară . Același lucru este valabil și pentru malnutriție , foarte frecventă în țările endemice, și obezitatea asociată cu numeroase boli.
Punerea în scenă
Există mai multe clasificări cu privire la etapele tumorii:
Clasificarea TNM
Dintre diversele, cea mai răspândită este indicată cu acronimul TNM: acestea indică cele trei subforme pentru care „Tumora primitivă, ganglionii limfatici (nodul) și metastazele îndepărtate”, aflată acum la a șasea ediție [14] adoptată de AJCC (American Comitetul mixt pentru cancer) și UICC (Uniunea Internațională împotriva Cancerului), în timp ce varianta studiată în Japonia de LCSGJ (Grupul de studiu al cancerului hepatic din Japonia) sa dovedit a fi mai bună în stadiile incipiente ale cancerului. [15]
| Tumora primară | Ganglionii limfatici regionali | Metastaze la distanță |
|---|---|---|
| TX, nedeterminat | NX, nu poate fi determinat | MX, nedeterminabil |
| T0, nu este evidențiat | N0, absența metastazelor | M0, absență la distanță |
| T1, este prezentat un singur nodul | N1, prezența metastazelor | M1, prezența formelor la distanță |
| T2, noduli multipli (dimensiune mai mică de 5cm) | * | |
| T3, noduli multipli (mai mari de 5 cm) | * | |
| T4, care implică alte organe sau cu perforație peritoneului visceral | * |
În cele din urmă, etapele conform TNT ar fi:
| stadiu | TNM |
|---|---|
| THE | T1 - N0 - M0 |
| II | T2 - N0 - M0 |
| IIIA | T3 - N0 - M0 |
| IIIB | T4 - N0 - M0 |
| IIIC | T (orice formă) - N1 - M0 |
| IV | T (orice formă) - N (orice formă) - M1 |
Clasificarea CLIP
O altă clasificare este cea identificată în Italia prin CLIP (Cancer of the Liver Italian Program) care, comparativ cu celelalte, s-a dovedit a fi cea mai exactă [16] .
Acesta ia în considerare patru caracteristici, inclusiv clasificarea Child-Pugh , calculată după cum urmează:
| Demonstrație | Puncte 1 | Punctele 2 | Punctele 3 |
|---|---|---|---|
| Gradul de encefalopatie | Absența | 1-2 (ușoară) | 3-4 (moderat) |
| Ascita | Absența | Blând | Moderat |
| Albumină | Mai mare de 3,5 | 2,8 - 3,5 | Mai puțin de 2,8 |
| PT (în raport cu alungirea exprimată în secunde) | 1-4 | 4-6 | mai mare de 6 |
| Bilirubina | 1-2 | Pana la 3 | mai mare de 3 |
Scorul CLIP este apoi calculat după cum urmează:
| Caracteristică | 0 puncte | Puncte 1 | Punctele 2 |
|---|---|---|---|
| Clasa Child-Pugh | A (până la 6 puncte) | B (până la 9 puncte) | C (peste 9 puncte) |
| Noduli | Un singur nodul | Noduli multipli | Masiv (sau cu volum hepatic mai mare de 50%) |
| nivelul alfa-fetoproteinei | Mai puțin de 400 ng / ml | Egal sau mai mare de 400 ng / ml | * |
| Tromboza venei porte | Nu | da | * |
Alte tipuri de clasificare
TNM și CLIP nu sunt singurele luate în considerare, există cele din Okuda care a prezentat limitări considerabile [17] , și cea din Barcelona, care este în prezent cea mai utilizată de medici și în studiile clinice și care ia în considerare următoarele criterii:
• Numărul de răniți
• Volumul leziunilor
• Invazie vasculară
• Funcția hepatică
Diagnostic
După începerea unui istoric medical amănunțit și a unui examen fizic , este necesară confirmarea în timpul analizei histologice sau citologice. Când nu reușesc, se utilizează alte teste de diagnostic:
- Ecografia utilizată în screening o poate diferenția de tromboza non-neoplazică
- Tomografie computerizată spirală multislice
- Rezonanță magnetică
- Biopsia , luând în considerare posibilele complicații este utilizată atunci când valorile alfa-fetoproteinei sunt mai mici de 400 ng / ml
- Laparoscopie cu ultrasunete intraoperatorie
Arteriografia și scintigrafia hepatică utilizate odată au fost înlocuite acum cu teste mai specifice
Terapii
Tratamentul care oferă cele mai multe rezultate este chirurgical.
Terapia chirurgicală
Rezecția se efectuează în cazurile în care masa tumorală este mică sau în cazul unui singur nodul. [18] Dimensiunile nu trebuie să depășească 5 cm în cazul unui singur nodul, 3 cm în cazul mai multor noduli (maximum trei) conform indicațiilor criteriilor de la Milano și nu este însoțită de hipertensiune portală , [19] în în orice caz, persoanele cărora li se poate aplica acest tip de intervenție sunt mai mici de 18%. [20] Recent au fost aprobate noi criterii care sugerează prezența unei mase hepatice funcționale de mai puțin de 30% postoperator ca singură contraindicație a intervenției chirurgicale hepatice.
Hepatectomia reglementată trebuie să fie atentă la cantitatea posibilă de parenchim care trebuie eliminată, care nu trebuie să depășească 20%. Adesea, această practică este utilizată pentru a anticipa un posibil transplant ulterior [21], în timp ce posibilitatea tumorectomiei este exclusă. Supraviețuirea după procedurile de rezecție în cazurile de mase mari scade semnificativ, ajungând la 17% la 5 ani.
Transplant
Transplantul hepatic este de așteptat în cazurile de ciroză atât moderată, cât și severă [22], dar ambele oferă rareori rezultatele dorite.
În cazul evaluării unui posibil transplant hepatic, sunt necesare alte teste pentru a exclude implicarea altor organe, în astfel de cazuri se efectuează o scanare osoasă și în așteptarea efectuării operației, starea persoanei este monitorizată prin repetarea unor teste (ca în cazul RMN la fiecare trei luni). Lista urmărește condițiile „ MELD ” (Model pentru boala hepatică în stadiu final) modificate în timp pentru a se adapta la mortalitate (același sistem este utilizat în Italia).
„MELD” a fost conceput pentru a prezice prognosticul pacienților cu boli hepatice cronice. Astăzi este utilizat pentru evaluarea necesității transplantului de ficat în locul scorului Child-Pugh. Comparativ cu acesta din urmă, MELD are o gamă mai largă de valori și reprezintă, de asemenea, un mijloc de evaluare mai obiectiv. Se calculează utilizând trei variabile: creatinină, bilirubină serică, timp de protrombină (exprimat ca raport internațional normalizat INR).
Se calculează conform următoarei formule: MELD = 3,78 [Ln bilirubină serică (mg / dL)] + 11,2 [Ln EUR] + 9,57 [Ln creatinină serică (mg / dL)] + 6,43
- Dacă pacientul a fost dializat de două ori în ultimele 7 zile, atunci valoarea creatininei serice utilizate ar trebui să fie de 4,0
- Orice valoare mai mică primește o valoare 1 (adică dacă bilirubina este 0,8, se utilizează valoarea 1,0) pentru a preveni apariția scorurilor sub 0 (logaritmul natural al 1 este 0 și orice valoare mai mică de 1 ar produce un rezultat negativ ).
Terapia non-chirurgicală
Există multe tratamente non-chirurgicale testate:
- Radioterapia , utilizată rar din cauza efectelor nocive ale dozelor peste 30 Gy.
- Chemoembolizare (TACE)
- Radiembolizare (TARE)
- Ablație laser ( terapie laser termoablativă , termoterapie interstițială cu laser sau ablație termică percutanată), tehnică minim invazivă, bine tolerată de pacient, aplicabilă în absența indicațiilor pentru intervenția chirurgicală rezectivă și pentru a conține progresia bolii în așteptarea transplantului . [23] [24]
- Alcoolizarea (PEI), o procedură neinvazivă cu rezultate remarcabile, se efectuează cu o injecție percutanată de etanol. Efectele secundare includ febră și durere (dar apar rar).
- Frecvența radio (RF), cu rezultate superioare PEI în cazul maselor mici. [25]
- Terapia hormonală, dovedită în diferite studii, a arătat că administrarea tamoxifenului nu a adus niciun rezultat [26] , în timp ce somatostatina și octreotida sunt testate.
- Intervențiile nutriționale (aportul de vitamina K ) s-au dovedit ineficiente.
Chimioterapie
Au fost studiate asocieri între diferite chimioterapice antiblastice ( adriamicină , gemcitabină și oxaliplatină ). De asemenea, s-a încercat perfuzia intraarterială repetată cu stimalamer neocarzinostatină (SMANCS), un derivat al neocarzinostatinei conjugat cu un polimer stiren-acid maleic, dar rezultatele au fost modeste. [27] [28] Au fost obținute rezultate mai bune cu medicamentele de chimioterapie care inhibă neoangiogeneza tumorală; O singură moleculă de chimioterapie, sorafenib, este în prezent aprobată pentru utilizare clinică pentru tratamentul carcinomului hepatocelular avansat în absența cirozei hepatice Child-Pugh A sau ciroză, cu o creștere de aproximativ trei luni a supraviețuirii medii și a timpului până la progresia radiologică.
Complicații
Printre diferitele complicații posibile, apariția icterului și sindromul Budd-Chiari , în timp ce ruptura masei este rar văzută.
Prevenirea
Boala este parțial prevenită prin vaccinarea împotriva hepatitei B. Și în evitarea factorilor de risc precum expunerea la aflatoxine și alcoolismul cronic. Pacienții cu ciroză trebuie să evite consumul de alcool. În plus, screeningul pentru hemocromatoză poate fi util pentru unii pacienți pentru a identifica condițiile de risc [29] .
Prognoză
Această intrare sau secțiune despre patologie și oncologie nu citează sursele necesare sau cei prezenți sunt insuficienți . |
Începând cu 2014, studiile sunt încă deschise și necontrolate și nu toate cancerele au aceeași evoluție. Supraviețuirea depinde de mai mulți factori: numărul de noduli, țesutul hepatic funcțional și dimensiunea tumorii. La trei ani, supraviețuirea este de 55-75%, dar la cinci ani după diagnostic este, în general, foarte scăzută, de asemenea, deoarece boala este adesea descoperită când este deja extinsă. Supraviețuirea este mai bună dacă pacientul este tratat.
Pentru mase mai mici de 5 cm în clasa A, rata de supraviețuire este de 5 ani: după rezecția tumorii, 49%; după PEI, 48%; după embolizare , 44%; iar după transplant de ficat , 70%.
În caz de recurență (adică reapariția unei noi tumori după tratament / intervenție, distinctă de cea primară) sau de metastază , supraviețuirea pe cinci ani este redusă: după IEP, 5%; pentru metastaze 17-46% și pentru recurență (tumoră nouă), 5-50%.
Notă
- ^ Sun VC, Sarna L., Managementul simptomelor în carcinomul hepatocelular. , în Clin J Oncol Nurs. , vol. 12, 1973, pp. 759-66.
- ^ Estimările țării OMS privind bolile și leziunile , Organizația Mondială a Sănătății , 2009. Accesat la 11 noiembrie 2009 .
- ^ O estimare scăzută în comparație cu alte țări. Mortalitatea este de 2,9% din decesele provocate de cancer. Conform tabelelor de date privind utilizarea publică a mortalității din SUA, 1969–2004, Centrul Național pentru Statistici de Sănătate, Centre pentru Controlul și Prevenirea Bolilor 2006
- ^ Rustgi VK., Epidemiologia carcinomului hepatocelular. , în Gastroenterol Clin North Am. , vol. 16, decembrie 1987, pp. 545-51.
- ^ Wu PC. Carcinom hepatocelular: epidemiologie și patologie. Practica din Hong Kong. 1983; 5: 790-5.
- ^ Gianni Bonadonna, Gioacchino Robustelli Della Cuna, Pinuccia Valgussa, Oncological Medicine (ediția a VIII-a) p.1040 , Milano, Elsevier Masson, 2007, ISBN 978-88-214-2814-2 .
- ^ Fan ST, Wong J. Terblanche J. Churchill Livingstone; Londra: 1996. Carcinom hepatocelular în est, malignitate hepatobiliară; pp. 169–83.
- ^ Orphanet: carcinom hepatocelular , pe www.orpha.net. Adus pe 5 februarie 2019 .
- ^ Printre studiile efectuate pentru a demonstra legătura dintre hepatita B și carcinomul hepatocelular, care a fost efectuată pe mai mult de 22.000 în statul Taiwan Beasley RP, Hwang LY, Lin CC, Chien CS., Carcinom hepatocelular și virusul hepatitei B. Un studiu prospectiv pe 22 707 de bărbați din Taiwan. , în Lancet. , vol. 2, 1981, pp. 1129-1133.
- ^ Yuan JM, Govindarajan S, Ross RK, Yu MC., Infecție cronică cu virusul hepatitei G în raport cu carcinomul hepatocelular în rândul non-asiaticilor din județul Los Angeles, California. , în Rac. , vol. 86, 1999, pp. 936-43.
- ^ Kim B, Park SH, Yang HR, Seo JK, Kim WS, Chi JG., Carcinom hepatocelular care apare în sindromul alagille. , în Pathol Res Pract. , vol. 201, 2005, pp. 55-60.
- ^ Harada M .., boala Wilson și carcinom hepatocelular. , în Intern Med. , vol. 43, noiembrie 2004.
- ^ P Bhosale, J Szklaruk, PM Silverman, Stadializarea curentă a carcinomului hepatocelular: implicații imagistice , în Imagistica cancerului , vol. 6, 2006.
- ^ Zhou L, Rui JA, Wang SB, Chen SG, Qu Q., Clasificarea LCSGJ-T, ediția a VI-a sau a 5-a Etapa TNM nu a prezis în mod independent prognoza pe termen lung a carcinomului hepatocelular legat de HBV după hepatectomia radicală. , în J Surg Res. , Octombrie 2008.
- ^ Minagawa M, Ikai I, Matsuyama Y, Yamaoka Y, Makuuchi M., Stadializarea carcinomului hepatocelular: evaluarea sistemelor TNM japoneze și AJCC / UICC TNM într-o cohortă de 13.772 pacienți din Japonia , în Ann Surg. . , vol. 245, iunie 2007, pp. 909-22.
- ^ Huo TI, Hsia CY, Huang YH, Lin HC, Lee PC, Lui WY, Chiang JH, Chiou YY, Loong CC, Lee SD. Selectarea unui model de prognostic pe termen scurt pentru carcinomul hepatocelular: comparație între modelul pentru stadiu de boală hepatică (MELD), MELD-sodiu și cinci sisteme de stadializare a cancerului , în J Clin Gastroenterol. , 2009.
- ^ Pons F, Varela M, Llovet JM., Sisteme de stadializare în carcinom hepatocelular. , în HPB (Oxford). , vol. 7, 2005, pp. 35-41.
- ^ Choi GH, Han DH, Kim DH, Choi SB, Kang CM, Kim KS, Choi JS, Park YN, Park JY, Kim DY, Han KH, Chon CY, Lee WJ., Rezultat după rezecția curativă pentru un imens (> / = 10 cm) carcinom hepatocelular și semnificația prognostică a clasificării tumorale brute. , în Am J Surg. , 2009.
- ^ A spus A, Wells J., Managementul carcinomului hepatocelular. , în Minerva Med. , vol. 100, 2009, pp. 51-68.
- ^ Hung H., Modalități de tratament pentru carcinomul hepatocelular. , în Obiectivele de droguri împotriva cancerului Curr. , vol. 5, 2005, pp. 131-8.
- ^ Kamiyama T, Nakanishi K, Yokoo H, Kamachi H, Tahara M, Suzuki T, Shimamura T, Furukawa H, Matsushita M, Todo S., Recurrence Patterns After Hepatectomy of Hepatocellular Carcinoma: Implication of Milan Criteria Utilization. , în Ann Surg Oncol. , 2009.
- ^ Cunningham SC, Tsai S, Marques HP, Mira P, Cameron A, Barroso E, Philosophe B, Pawlik TM., Managementul carcinomului hepatocelular precoce la pacienții cu ciroză bine compensată. , în Ann Surg Oncol. , 2009.
- ^ Pacella CM, Francica G, Di Lascio FM, Arienti V, Antico E, Caspani B, Magnolfi F, Megna AS, Pretolani S, Regine R, Sponza M, Stasi R., Rezultatul pe termen lung al pacienților cirotici cu carcinom hepatocelular precoce tratat cu ablație laser percutanată cu ultrasunete: o analiză retrospectivă. , în J Clin Oncol. , 16: 2615-21, iunie 2009.
- ^ Pompili M, Pacella CM, Francica G, Angelico M, Tisone G, Craboledda P, Nicolardi E, Rapaccini GL, Gasbarrini G., Ablația laser percutanată a carcinomului hepatocelular la pacienții cu ciroză hepatică care așteaptă transplant hepatic. , în Eur J Radiol. , 74 (3): e6-e11, iunie 2010.
- ^ Orlando A, Leandro G, Olivo M, Andriulli A, Cottone M., Ablația termică prin radiofrecvență vs. injecție percutanată de etanol pentru carcinom hepatocelular mic în ciroză: meta-analiză a studiilor controlate randomizate. , în Am J Gastroenterol. , vol. 104, februarie 2009, pp. 514-24.
- ^ Roxburgh P, Evans TR., Terapia sistemică a carcinomului hepatocelular: Facem progrese? , în Adv Ther. 2008 , vol. 25, noiembrie 2008, pp. 1089-104 ..
- ^ T. Okusaka, S. Okada; H. Ishii; M. Ikeda; H. Nakasuka; H. Nagahama; R. Iwata; H. Furukawa; K. Takayasu; Y. Nakanishi; M. Sakamoto, chimioterapie transarterială cu zinostatină stimalamer pentru carcinom hepatocelular. , în Oncologie , vol. 55, nr. 4, pp. 276-83, PMID 9663415 .
- ^ T. Okusaka, S. Okada; H. Ueno; M. Ikeda; R. Iwata; H. Furukawa; K. Takayasu; N. Moriyama; T. Sato; K. Sato, embolizare arterială transcateteră cu zinostatină stimalamer pentru carcinom hepatocelular. , în Oncologie , vol. 62, nr. 3, 2002, pp. 228-33, DOI : 10.59570 , PMID 12065870 .
- ^ Prevenire , la nlm.nih.gov . Adus la 12 mai 2010 .
Bibliografie
- Gianni Bonadonna, Gioacchino Robustelli Della Cuna, Pinuccia Valgussa, Medicina oncologică (ediția a VIII-a) , Milano, Elsevier Masson, 2007, ISBN 978-88-214-2814-2 .
Elemente conexe
Alte proiecte
-
 Wikimedia Commons conține imagini sau alte fișiere despre carcinomul hepatocelular
Wikimedia Commons conține imagini sau alte fișiere despre carcinomul hepatocelular
linkuri externe
- A avea tupeu este o chestiune a creierului , pe avefegato.net . Accesat la 15 septembrie 2009. Arhivat din original la 9 august 2009 .
- Chirurgie hepatică , onirurgdelfegato.it .
- Aflați despre și preveniți bolile hepatice , pe malattiedelfegato.blogspot.com .
- Centru pentru studiul și tratamentul tumorilor hepatice , pe liverchirurgia.com .
- Chirurgie hepatobiliară, Spitalul San Raffaele, Milano https://www.hsr.it/structures/ospedale-san-raffaele/chirurgia-epatobiliare

